
6.气体吸收装置 某些反应过程中会产生刺激性或有毒的气体,我们必须除去,不可释放于空气中,以免 污染空气引起中毒。图1-10是几种常见的气体吸收装置。 图1-10气体吸收装置示例 (三)常用玻璃器皿的洗涤、干燥和保养 1.仪器的清洗 有机化学实验中,为了避免杂质混入反应物中,实验用仪器必须清洁干燥。清洗玻璃仪 器最简单常用的的方法就是用长柄毛刷(试管刷)蘸上皂粉或去污粉,刷洗润湿的器壁,直至 玻璃表面的污物除去为止,最后用自来水清洗。有时去污粉的微小粒子会粘附在玻璃器皿壁 上,不易被水冲走,此时可用2%盐酸摇洗一次,再用自来水清洗。当仪器倒置,器壁不挂 水珠时,即己洗净,可供一般实验需用。 为了使清洗工作简便有效,最好在每次实验结束后,立即清洗使用过的仪器。方法有: 铬酸洗液氧化性很强,对有机污垢破坏力很强。倾去器皿内的水,慢慢倒入洗液,转动 器皿,使洗液充分浸润不干净的器壁,数分钟后把洗液倒回洗液瓶中,再用自来水冲洗器皿。 若壁上沾有少量炭化残渣,可加入少量洗液,浸泡一段时间后再在小火上加热,直至冒出气 泡,炭化残渣可被除去。但当洗液颜色变绿,表示洗液已经失效,不能倒回洗液瓶中。 碱性残渣可用稀盐酸或稀疏酸溶解:酸性残渣可用稀的氢氧化钠溶液。 残渣为焦油状物,可选用丙酮、乙醚、甲苯浸泡,但要加盖以免溶剂挥发。此外也可用 NaOH的乙醇溶液洗涤。用有机溶剂作为洗涤剂时,必须回收重复使用。反对盲目使用各种 化学试剂和有机溶剂来清洗仪器。这样不仅造成浪费,而且还可能带来危险 有机实验室中常用超声波清洗器来洗涤玻璃仪器,既省时又方便。只要把用过的仪器, 放在配有洗涤剂的溶液中,接通电源,利用声波的振动和能量,即可达到清洗仪器的目的 清洗过的仪器,再用自来水漂洗干净即可。 若用于精制产品,或供有机分析用的仪器,则尚须用蒸馏水摇洗,以除去自来水冲洗时 带入的杂质。 2.仪器的干燥 晾干清洁的仪器倒置,水珠易流下,干燥得快。 烘干放入烘箱的仪器应除去软木塞或橡皮塞,带有磨口玻璃塞的仪器也应拔出塞子。 仪器口应向上,烘箔温度100一120℃。取出烘干仪器前最好使烘箱冷至室温。 吹干如急需用少量干燥仪器,可用气流干燥器或电吹风吹干。 3.仪器的保养 温度计温度计水银球部位玻璃很薄,容易打破,使用时要格外小心,不可用温度计当
11 6. 气体吸收装置 某些反应过程中会产生刺激性或有毒的气体,我们必须除去,不可释放于空气中,以免 污染空气引起中毒。图 1-10 是几种常见的气体吸收装置。 图 1-10 气体吸收装置示例 (三) 常用玻璃器皿的洗涤、干燥和保养 1. 仪器的清洗 有机化学实验中,为了避免杂质混入反应物中,实验用仪器必须清洁干燥。清洗玻璃仪 器最简单常用的的方法就是用长柄毛刷(试管刷)蘸上皂粉或去污粉,刷洗润湿的器壁,直至 玻璃表面的污物除去为止,最后用自来水清洗。有时去污粉的微小粒子会粘附在玻璃器皿壁 上,不易被水冲走,此时可用 2%盐酸摇洗一次,再用自来水清洗。当仪器倒置,器壁不挂 水珠时,即已洗净,可供一般实验需用。 为了使清洗工作简便有效,最好在每次实验结束后,立即清洗使用过的仪器。方法有: 铬酸洗液氧化性很强,对有机污垢破坏力很强。倾去器皿内的水,慢慢倒入洗液,转动 器皿,使洗液充分浸润不干净的器壁,数分钟后把洗液倒回洗液瓶中,再用自来水冲洗器皿。 若壁上沾有少量炭化残渣,可加入少量洗液,浸泡一段时间后再在小火上加热,直至冒出气 泡,炭化残渣可被除去。但当洗液颜色变绿,表示洗液已经失效,不能倒回洗液瓶中。 碱性残渣可用稀盐酸或稀硫酸溶解;酸性残渣可用稀的氢氧化钠溶液。 残渣为焦油状物,可选用丙酮、乙醚、甲苯浸泡,但要加盖以免溶剂挥发。此外也可用 NaOH 的乙醇溶液洗涤。用有机溶剂作为洗涤剂时,必须回收重复使用。反对盲目使用各种 化学试剂和有机溶剂来清洗仪器。这样不仅造成浪费,而且还可能带来危险。 有机实验室中常用超声波清洗器来洗涤玻璃仪器,既省时又方便。只要把用过的仪器, 放在配有洗涤剂的溶液中,接通电源,利用声波的振动和能量,即可达到清洗仪器的目的。 清洗过的仪器,再用自来水漂洗干净即可。 若用于精制产品,或供有机分析用的仪器,则尚须用蒸馏水摇洗,以除去自来水冲洗时 带入的杂质。 2. 仪器的干燥 晾干 清洁的仪器倒置,水珠易流下,干燥得快。 烘干 放入烘箱的仪器应除去软木塞或橡皮塞,带有磨口玻璃塞的仪器也应拔出塞子。 仪器口应向上,烘箱温度 100~120℃。取出烘干仪器前最好使烘箱冷至室温。 吹干 如急需用少量干燥仪器,可用气流干燥器或电吹风吹干。 3. 仪器的保养 温度计 温度计水银球部位玻璃很薄,容易打破,使用时要格外小心,不可用温度计当

搅拌棒使用,也不能测定超越温度计最高刻度的温度。温度计用后应使其慢慢冷却,特别是 在测量高温之后,切勿立即用冷水冲洗。使用过的温度计待其冷却后洗净擦干收好。 冷凝管冷凝管通水后较重,安装冷凝管时应将夹子夹紧冷凝管的重心处。洗涤冷凝管 时要用长毛刷。洗净后应直立倒置,便于晾干。 分液漏斗和滴液漏斗分液漏斗和滴液漏斗的活塞和盖子都是磨口的,若是非原配的, 就可能不严密而滴漏,所以使用时要注意保护它。各个漏斗之间也不要互相调换寒子。用后 一定要在活塞和磨口间垫上纸片,以免日久难以打开。分液漏斗和滴液漏斗用后必须拔出塞 子和活塞,擦净上面的润滑油,洗净后再放入烘箱烘干。 4.仪器的选择 1.塞子的选择橡皮塞塞得严密,但能被某些有机溶剂溶解,此时可改用软木塞。软 木塞的缺点是比较疏松,塞不严密。塞子的大小应恰好与仪器的颈口相适1/3,使瓶塞插入 瓶口部分不少于塞子高度的13,不大于2/3。软木塞钻孔前需在压塞机内压紧,防止在钻孔 时塞子裂开。在钻橡皮塞时,选择打孔器的口径应与管子口径相等,打孔器的前部最好涂上 肥皂水、甘油或凡士林使容易钻入。向孔内插玻璃管或温度计前,可用圆锉先将孔洞修光 再在玻管或温度计的前部敷以水或甘油,然后用手紧握靠近塞子处的玻管或温度计,逐渐旋 枯插入 2.仪器的选择选择仪器是根据反应物的体积、反应的条件及反应物或生成物的理化 性质来决定的。 (1)反应瓶的大小,应该是使反应体积不超过其容积的2/3,一般为12。 (2)回流反应一般采用圆底烧瓶和球形冷凝器:回流搅拌并需控制反应温度时用三颈瓶 (3)蒸馏操作需用蒸馏瓶:减压蒸馏采用减压蒸馏瓶(克氏蒸馏头接在圆底烧瓶上)。 (4)被蒸馏物的沸点低于130℃用直形冷凝器,高于130℃用空气冷凝器。 (5)选择温度计,一般根据反应温度选用高于反应温度10℃、20℃的温度计,水银温度 计适用于测量一30~300℃的物质。温度低于一38C时常用内装有机液体的低温温度计因水 银会凝固)。 五、有机化学实验室常用设备及使用 1.加热 一般情况下,化学反应的速度随温度的升高而加快。大体上反应温度每升高10℃,反应 速度就会增加一倍。此外,有机化学实验的许多基本操作如回流、蒸馏、溶解、重结晶、熔 融等都需要加热。 实验室常用的加热器具有煤气灯、酒精灯、电热套和封闭电炉等。但玻璃仪器一般很少 用火焰直接加热,为了保证加热均匀和操作安全,经常选用合适的热浴来进行间接加热。 水浴水浴(图1-11)是最安全和方便的热源,100℃以下的反应或后处理大多可用水浴 加热 加热套电加热套是由玻璃纤维包裹电热丝编织而成,外接调压变压器以调节加热温 度。它的优点是安全、方便。但一种规格加热器只适用于一定容积的烧瓶,故需配备几种尺
12 搅拌棒使用,也不能测定超越温度计最高刻度的温度。温度计用后应使其慢慢冷却,特别是 在测量高温之后,切勿立即用冷水冲洗。使用过的温度计待其冷却后洗净擦干收好。 冷凝管 冷凝管通水后较重,安装冷凝管时应将夹子夹紧冷凝管的重心处。洗涤冷凝管 时要用长毛刷。洗净后应直立倒置,便于晾干。 分液漏斗和滴液漏斗 分液漏斗和滴液漏斗的活塞和盖子都是磨口的,若是非原配的, 就可能不严密而滴漏,所以使用时要注意保护它。各个漏斗之间也不要互相调换塞子。用后 一定要在活塞和磨口间垫上纸片,以免日久难以打开。分液漏斗和滴液漏斗用后必须拔出塞 子和活塞,擦净上面的润滑油,洗净后再放入烘箱烘干。 4. 仪器的选择 1. 塞子的选择 橡皮塞塞得严密,但能被某些有机溶剂溶解,此时可改用软木塞。软 木塞的缺点是比较疏松,塞不严密。塞子的大小应恰好与仪器的颈口相适1/3,使瓶塞插入 瓶口部分不少于塞子高度的1/3,不大于2/3。软木塞钻孔前需在压塞机内压紧,防止在钻孔 时塞子裂开。在钻橡皮塞时,选择打孔器的口径应与管子口径相等,打孔器的前部最好涂上 肥皂水、甘油或凡士林使容易钻入。向孔内插玻璃管或温度计前,可用圆锉先将孔洞修光, 再在玻管或温度计的前部敷以水或甘油,然后用手紧握靠近塞子处的玻管或温度计,逐渐旋 转插入。 2. 仪器的选择 选择仪器是根据反应物的体积、反应的条件及反应物或生成物的理化 性质来决定的。 (1)反应瓶的大小,应该是使反应体积不超过其容积的2/3,一般为1/2。 (2)回流反应一般采用圆底烧瓶和球形冷凝器;回流搅拌并需控制反应温度时用三颈瓶。 (3)蒸馏操作需用蒸馏瓶;减压蒸馏采用减压蒸馏瓶(克氏蒸馏头接在圆底烧瓶上)。 (4)被蒸馏物的沸点低于130℃用直形冷凝器,高于130℃用空气冷凝器。 (5)选择温度计,一般根据反应温度选用高于反应温度 10℃、20℃的温度计,水银温度 计适用于测量-30~300℃的物质。温度低于-38℃时常用内装有机液体的低温温度计(因水 银会凝固)。 五、有机化学实验室常用设备及使用 1. 加热 一般情况下,化学反应的速度随温度的升高而加快。大体上反应温度每升高10℃,反应 速度就会增加一倍。此外,有机化学实验的许多基本操作如回流、蒸馏、溶解、重结晶、熔 融等都需要加热。 实验室常用的加热器具有煤气灯、酒精灯、电热套和封闭电炉等。但玻璃仪器一般很少 用火焰直接加热,为了保证加热均匀和操作安全,经常选用合适的热浴来进行间接加热。 水浴 水浴(图1-11)是最安全和方便的热源,100℃以下的反应或后处理大多可用水浴 加热。 加热套 电加热套是由玻璃纤维包裹电热丝编织而成,外接调压变压器以调节加热温 度。它的优点是安全、方便。但一种规格加热器只适用于一定容积的烧瓶,故需配备几种尺
寸的加热套(图1-12)。用加热套加热时必须注意温度控制,稍微疏忽就会使升温过高而影响 反应。 油浴油浴的构造也简单,在结晶皿或陶瓷皿中加入油并安置电热丝,然后再和调压变 压器连接。有时也应用电磁搅拌来保持油浴温度均匀(图1-13)。油浴所用的油有甘油、植物 油和石蜡油(适于150℃以下的加热)。最好使用硅油,可加热至250℃以上,但价格较责。油 浴使用方便安全,容器内的反应物受热均匀,加热温度范围广。 红外灯红外灯适用于加热较低温度的反应,亦比较安全。 砂浴当加热温度在250~350℃时应采用砂浴。但由于砂浴温度分布不均匀,且传热慢, 温度上升慢,散热又太快,所以使用范围有限。 盐浴用铁锅装等量比的硝酸钾及硝酸钠混合物即为盐浴。使用温度范围为220一 680℃。注意盐浴中切勿藏入水。用过后的盐浴冷却后保存于干燥器中 图1-11水浴锅 图1-12电热套 1.与调压变压器相连2.磁坩埚3.电热丝4.温度计 5.玻璃皿6。油7.磁找拌器8电磁搅拌干9.加热 图1-13油浴锅 2.冷却 根据一些实验对低温的要求,在操作中需使用致冷剂。以下几种情况下应使用冷却剂: (1)某些反应,其中间体在室温下是不稳定的,这时反应就应在特定的低温条件下进 行,如重氮化反应,一般在0~5℃下进行: (2)反应放出大量的热,需要降温米控制反应速度: (3)为了降低固体物质在溶剂中的溶解度,以加速结晶的析出: (4)为了减少损失,把一些沸点很低的有机物冷却: (5)高度真空蒸馏装置。 低于室温的反应、分离和提纯等可用水浴、冰水浴、冰盐浴。液氮或干冰和溶剂的混合 物则适用于极低温度进行的反应。在搅拌下将液氨慢慢倒入有机溶剂中直至形成油膏状即为 所需冷却剂,在使用时可随时添加液氮以保持冷却温度。干冰和有机溶剂亦可配制成冷却剂, 将干冰碎块加入溶剂中即可,操作时应经常添加干冰以保持冷却。常用的冷却剂见表1。 0
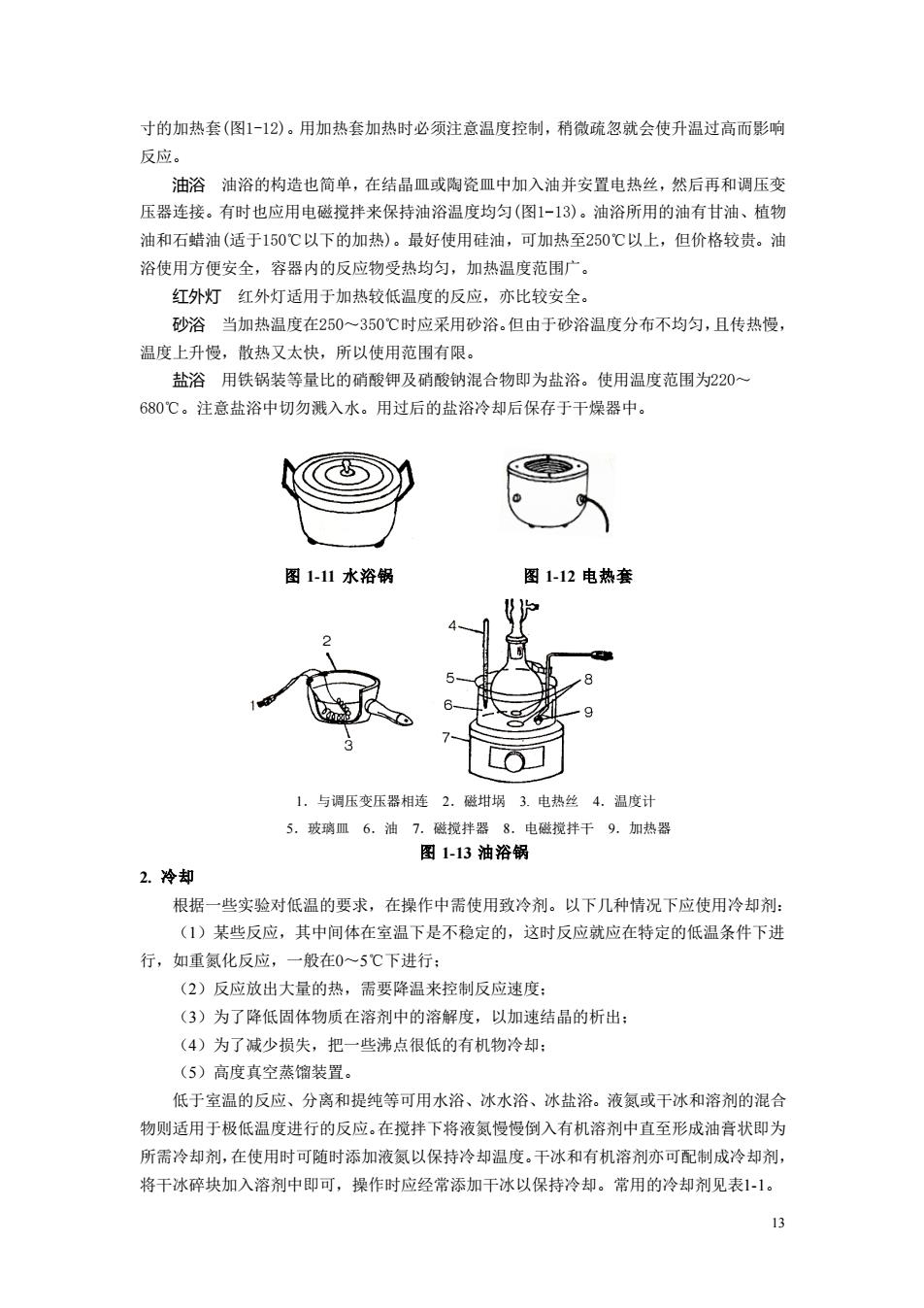
13 寸的加热套(图1-12)。用加热套加热时必须注意温度控制,稍微疏忽就会使升温过高而影响 反应。 油浴 油浴的构造也简单,在结晶皿或陶瓷皿中加入油并安置电热丝,然后再和调压变 压器连接。有时也应用电磁搅拌来保持油浴温度均匀(图1-13)。油浴所用的油有甘油、植物 油和石蜡油(适于150℃以下的加热)。最好使用硅油,可加热至250℃以上,但价格较贵。油 浴使用方便安全,容器内的反应物受热均匀,加热温度范围广。 红外灯 红外灯适用于加热较低温度的反应,亦比较安全。 砂浴 当加热温度在250~350℃时应采用砂浴。但由于砂浴温度分布不均匀,且传热慢, 温度上升慢,散热又太快,所以使用范围有限。 盐浴 用铁锅装等量比的硝酸钾及硝酸钠混合物即为盐浴。使用温度范围为220~ 680℃。注意盐浴中切勿溅入水。用过后的盐浴冷却后保存于干燥器中。 图 1-11 水浴锅 图 1-12 电热套 1.与调压变压器相连 2.磁坩埚 3. 电热丝 4.温度计 5.玻璃皿 6.油 7.磁搅拌器 8.电磁搅拌干 9.加热器 图 1-13 油浴锅 2. 冷却 根据一些实验对低温的要求,在操作中需使用致冷剂。以下几种情况下应使用冷却剂: (1)某些反应,其中间体在室温下是不稳定的,这时反应就应在特定的低温条件下进 行,如重氮化反应,一般在0~5℃下进行; (2)反应放出大量的热,需要降温来控制反应速度; (3)为了降低固体物质在溶剂中的溶解度,以加速结晶的析出; (4)为了减少损失,把一些沸点很低的有机物冷却; (5)高度真空蒸馏装置。 低于室温的反应、分离和提纯等可用水浴、冰水浴、冰盐浴。液氮或干冰和溶剂的混合 物则适用于极低温度进行的反应。在搅拌下将液氮慢慢倒入有机溶剂中直至形成油膏状即为 所需冷却剂,在使用时可随时添加液氮以保持冷却温度。干冰和有机溶剂亦可配制成冷却剂, 将干冰碎块加入溶剂中即可,操作时应经常添加干冰以保持冷却。常用的冷却剂见表1-1

表1·1常用冷却剂的组成及冷却温度 冷却剂 温度,℃ 碎冷(或冰.水 0 碎冰(3份)氯化钠1份) .20 干冰四氯化碳 .30 干冰乙而 干冰丙酮 78 液氮甲苯 95 干冰.了彩 -100 液氮-乙醚 116 液氨异 -160 液氮 196 3.干燥与干燥剂的使用 干燥是常用的除去固体、液体或气体中少量水分或少量有机溶剂的方法。例如很多有机 反应需要在绝对无水条件下进行,所用的原料及溶剂均应该是干燥的:某些化合物含有水分 在加热时会发生变质,故在燕馏或重结晶时也必须进行干燥:有机化合物在进行定性或定量 分析、波谱分析之前均需经干燥才会有准确结果:某些有机化合物会与少量水形成共沸混合 物或与水反应而影响产品纯度。因此,干燥是最常用而且十分重要的基本操作之一。 (1)干燥剂去水基本原理 有机化合物的干燥方法可分为物理方法和化学方法两种。物理方法有:烘干、晾干、吸 附、冷冻、分馏、共沸蒸馏等。近些年来,还常用离子交换树脂和分子筛等方法来进行干燥。 化学方法是利用干燥剂脱水,根据脱水作用可分为两类: 能与水可逆性结合,形成水合物,例如: CaCk+6 H20 -CaCk.6H20 与水发生不可逆的化学反应,生成新的化合物,如五氧化二磷、氧化钙、金属钠分别与 水反应生成磷酸、氢氧化钙和氢氧化钠。 (2)气体的干燥 要除去气体中的水,可使其通过充满无水氯化钙或固体氢氧化钾的干燥塔(图1-l4(), 或者通过装有浓硫酸的洗瓶(图1-14b)。 a干塔 洗 玻璃棉2.干燥剂3.浓硫 图1-14干燥塔和气体洗瓶
14 表 1-1 常用冷却剂的组成及冷却温度 冷却剂 温度,℃ 碎冷(或冰-水 碎冰(3 份)-氯化钠(1 份) 干冰-四氯化碳 液氮-氯苯 干冰-乙醇 干冰-丙酮 液氮-甲苯 干冰-乙醚 液氮-乙醚 液氮-异戊烷 液氮 0 -20 -30 -45 -72 -78 -95 -100 -116 -160 -196 3. 干燥与干燥剂的使用 干燥是常用的除去固体、液体或气体中少量水分或少量有机溶剂的方法。例如很多有机 反应需要在绝对无水条件下进行,所用的原料及溶剂均应该是干燥的;某些化合物含有水分 在加热时会发生变质,故在蒸馏或重结晶时也必须进行干燥;有机化合物在进行定性或定量 分析、波谱分析之前均需经干燥才会有准确结果;某些有机化合物会与少量水形成共沸混合 物或与水反应而影响产品纯度。因此,干燥是最常用而且十分重要的基本操作之一。 (1)干燥剂去水基本原理 有机化合物的干燥方法可分为物理方法和化学方法两种。物理方法有:烘干、晾干、吸 附、冷冻、分馏、共沸蒸馏等。近些年来,还常用离子交换树脂和分子筛等方法来进行干燥。 化学方法是利用干燥剂脱水,根据脱水作用可分为两类: 能与水可逆性结合,形成水合物,例如: CaCl2 + 6 H2O CaCl2 . 6H2O 与水发生不可逆的化学反应,生成新的化合物,如五氧化二磷、氧化钙、金属钠分别与 水反应生成磷酸、氢氧化钙和氢氧化钠。 (2)气体的干燥 要除去气体中的水,可使其通过充满无水氯化钙或固体氢氧化钾的干燥塔(图1-14(a)), 或者通过装有浓硫酸的洗瓶(图1-14(b))。 (a)干燥塔 (b)洗瓶 1.玻璃棉 2.干燥剂 3.浓硫酸 图 1-14 干燥塔和气体洗瓶

为了防止空气中的海气进入反应系统中,在空气的可能入口处需要装上填了干燥剂的干燥 管。常用的干燥剂为无水氯化钙。它容易吸收水分,但吸水后会结成块状将干燥管堵塞。故 每次用过后的干燥管应保存在干燥器中防止吸潮。如管中氯化钙已潮解 则需重新装管。 (3)固体有机化合物的干燥 重结晶得到的固体常带水分或有机溶剂,应根据化合物性质选择适当的方法进行干燥 晾干这是最简便的干燥方法。把要干燥的固体先放在瓷孔漏斗中的滤纸上,或在滤纸 上面压干,然后在一张滤纸上面薄薄地摊开,用另一张滤纸覆盖起来,让它在空气中慢慢地 晾干。 加热干燥对于热稳定的固体化合物可以放在烘箱内或红外灯下干燥,加热的温度切忌 超过该固体的熔点,以免固体变色或分解,如需要则在真空恒温干燥箱中干燥。 干燥器干燥对于易吸湿或较高温度下干燥时会发生分解或变色得周体化和物可用干 燥器干燥,干燥器有普通干燥器(图1-15(a)、真空干燥器(图1-15b)和真空恒温干燥器 (图1-15c)。 (a)普通千燥器 b)其空千燥器 (c其空恒温干燥器 1磁板2干燥剂3夹层4.放样品5.容剂6,抽气7.P20 图1-15千燥器 (4)液体有机化合物的干燥 1)干燥剂去水 a.干燥剂的选择 液体有机化合物的干燥,通常是用干燥剂直接与其接触,因此干燥剂与被干燥的液体有 机化合物不发生化学反应,包括溶解、配位、缔合和催化等作用,例如酸性物质不能使用碱 性干燥剂,而碱性物质则不能使用酸性干燥剂。常用的干燥剂见表12。 当选用与水结合生成水合物的干燥剂时,必须考虑干燥剂的吸水容量和干操效能。吸水 容量是指单位质量干燥剂所吸收的水量,干燥效能指达到平衡时液体被干燥的程度,例如, 无水疏酸钠可形成NSO10HO,即1 gNazSO:最多能吸1.27g水,其吸收水容量为127,但 其水化物的水蒸气压也较大(25℃时为255.98Pa),故干燥效能差.氯化钙能形成CaC16H0, 其吸水容量为0.97,此水化物在25℃水蒸气压为39.99P阳,故无水氯化钙的吸水容量虽然较小, 但干燥效能强,所以干燥操作时应根据除去水分的要求而选择合适的干燥剂。通常与水结合 生成水合物的干燥剂形成水合物需要一定的平衡时间,所以,加入干燥剂后必须放置一段时 间才能达到脱水的效果。常用的干燥剂性能见附录三。 己吸水的干燥剂受热后又会脱水,其蒸气压随着温度的升高而增加,所以,对已干燥的液体 在蒸瘤之前必须把干燥剂滤去
15 为了防止空气中的潮气进入反应系统中,在空气的可能入口处需要装上填了干燥剂的干燥 管。常用的干燥剂为无水氯化钙。它容易吸收水分,但吸水后会结成块状将干燥管堵塞。故 每次用过后的干燥管应保存在干燥器中防止吸潮。如管中氯化钙已潮解,则需重新装管。 (3)固体有机化合物的干燥 重结晶得到的固体常带水分或有机溶剂,应根据化合物性质选择适当的方法进行干燥。 晾干 这是最简便的干燥方法。把要干燥的固体先放在瓷孔漏斗中的滤纸上,或在滤纸 上面压干,然后在一张滤纸上面薄薄地摊开,用另一张滤纸覆盖起来,让它在空气中慢慢地 晾干。 加热干燥 对于热稳定的固体化合物可以放在烘箱内或红外灯下干燥,加热的温度切忌 超过该固体的熔点,以免固体变色或分解,如需要则在真空恒温干燥箱中干燥。 干燥器干燥 对于易吸湿或较高温度下干燥时会发生分解或变色得固体化和物可用干 燥器干燥,干燥器有普通干燥器(图1-15(a))、真空干燥器(图1-15(b))和真空恒温干燥器 (图1-15(c))。 (a) 普通干燥器 (b) 真空干燥器 (c) 真空恒温干燥器 1. 磁板 2.干燥剂 3.夹层 4.放样品 5.容剂 6.抽气 7. P2O5 图 1-15 干燥器 (4)液体有机化合物的干燥 1)干燥剂去水 a. 干燥剂的选择 液体有机化合物的干燥,通常是用干燥剂直接与其接触,因此干燥剂与被干燥的液体有 机化合物不发生化学反应,包括溶解、配位、缔合和催化等作用,例如酸性物质不能使用碱 性干燥剂,而碱性物质则不能使用酸性干燥剂。常用的干燥剂见表1-2。 当选用与水结合生成水合物的干燥剂时,必须考虑干燥剂的吸水容量和干燥效能。吸水 容量是指单位质量干燥剂所吸收的水量,干燥效能指达到平衡时液体被干燥的程度,例如, 无水硫酸钠可形成Na2SO4•10H2O,即1g Na2SO4 最多能吸1.27g水,其吸收水容量为1.27,但 其水化物的水蒸气压也较大(25℃时为255.98Pa),故干燥效能差。氯化钙能形成CaCl2•6H2O, 其吸水容量为0.97,此水化物在25℃水蒸气压为39.99Pa,故无水氯化钙的吸水容量虽然较小, 但干燥效能强,所以干燥操作时应根据除去水分的要求而选择合适的干燥剂。通常与水结合 生成水合物的干燥剂形成水合物需要一定的平衡时间,所以,加入干燥剂后必须放置一段时 间才能达到脱水的效果。常用的干燥剂性能见附录三。 已吸水的干燥剂受热后又会脱水,其蒸气压随着温度的升高而增加,所以,对已干燥的液体 在蒸馏之前必须把干燥剂滤去