
176有机化学学习指号 第十四章 杂环化合物 一、内容提要 杂环化合物是指分子中含有碳原子和杂原了的环状结构的化合物,最常见的杂原子 是氮氧和硫原子。本章主要讨论一此环系比较稳定,具有一定芳香性的五元,六元杂环 及其钙杂坏化合物。 (一】杂环化合物的分类 杂环化合物可根据环的大小(最常见的是五元环和六元环)环中杂原子(N,O,S等) 的种类和数目以及环的形式(单杂环和树杂环)米进行分类。 (二)杂环化合物的命名 1.特定杂环的命名 以特定的45个杂环化合物的俗名和半俗名作为命名基础,采用外文名音译加“口” 旁表示。单杂环母核编号从杂原子开始,并使其它杂原子位号尽可能小。 若有两个以上不同的杂原子时,一般按氧硫氮(0,SNH,N=)的顺序编号。稠杂 环按其固定的顺序缩号。取代基位次用12,3.或BY.表示。 2.无特定名称的稠杂环母核的命名 通常采用附加环并基本环选行命名,附加环在前,基本环在后。例如 称作塞晚2,3味童 形框环对环巢号基本环细号基本环 (三)杂环化合物的结构特点 杂环化合物为平面型分子,杂坏中碳原子以及杂原子均为平杂化,并以▣健相连 五元杂环中的杂原子p轨道中有两个p电子,六元杂环中的杂原子n轨道中有一个p电 子,这些电子与碳p轨道中的电子构成垂直干环面的封闭式大石键,T电子数满足 4+2规则,具有一定的芳香性。与苯环相比,杂环化合物的电子云密集程度以及键的 均没有完全平均化。 (四】六元杂环 吡院是典刑的六元杂环。吡啶环上氮原子上的一对未共用电子木参与共绑体系,故 晕碱性。与苯相比,吡啶易选行亲核取代反亚,取代基主要进人:位:亲电取代反应则 需要在比较烈的条件下进行,取代基主要进水B位,但不能发生侧克反应 PDF created with pdfFactory trial version ww.pdffactory.com
PDF created with pdfFactory trial version www.pdffactory.com

第十四童杂环化合物1亿 B2,300℃ (亲电取代 1.NaNH,/NH/△2.HO (亲核取代) NH, 氧化反应、亲电取代) 克反应X (五)五元杂环 最简单的五元杂环化合物是吡咯、呋哺和噻吩。其芳香性为噻盼>吡咯>呋喃。由 于组成封闭大π健的五个轨道中含有六个电子,环上有高的电子云密度,与苯相 比,五元杂环容易发生亲电取代反应,反应主要在。位进行。 CH COO NO: NaOH,Ac,0.5C SO,H H NH. (不发生亲核取代反应】 0a (傅克酰化, (亲电取代) (六)调环化合物一吲哚、喹琳、异喹啉、嘌哈 吲哚的化学性质与吡咯相似,碱性极弱,亲电取代反应主要在3-位进行。 SO,H Q 喹啉,异喹啉具有苯和吡啶的双重性质。亲电取代反应主要发生在苯环上,亲核取 代反应则主要发生在吡啶环上。 PDF created with pdfFactory trial version ww.pdffactory.com
PDF created with pdfFactory trial version www.pdffactory.com

1☑8有机化学学习指号 N0. (亲电取代) NO (亲核取代) 苯环比吡啶环易被氧化,吡啶环较苯环易被还原。 芳香杂环化合物和苯相比较,其亲电和亲核取代反应的活性顺序如下: 亲电取代: 900 亲核取代: Q0 二、例题解析 [例1]烷基取代的吡啶的pKa如下所示: 5.25.97 5.76 6.58 它们的pKa不受位阻的影响,为什么? 解: 在水中的离解 +H,0 H PDF created with pdfFactory trial version www.pdffactory.com
PDF created with pdfFactory trial version www.pdffactory.com
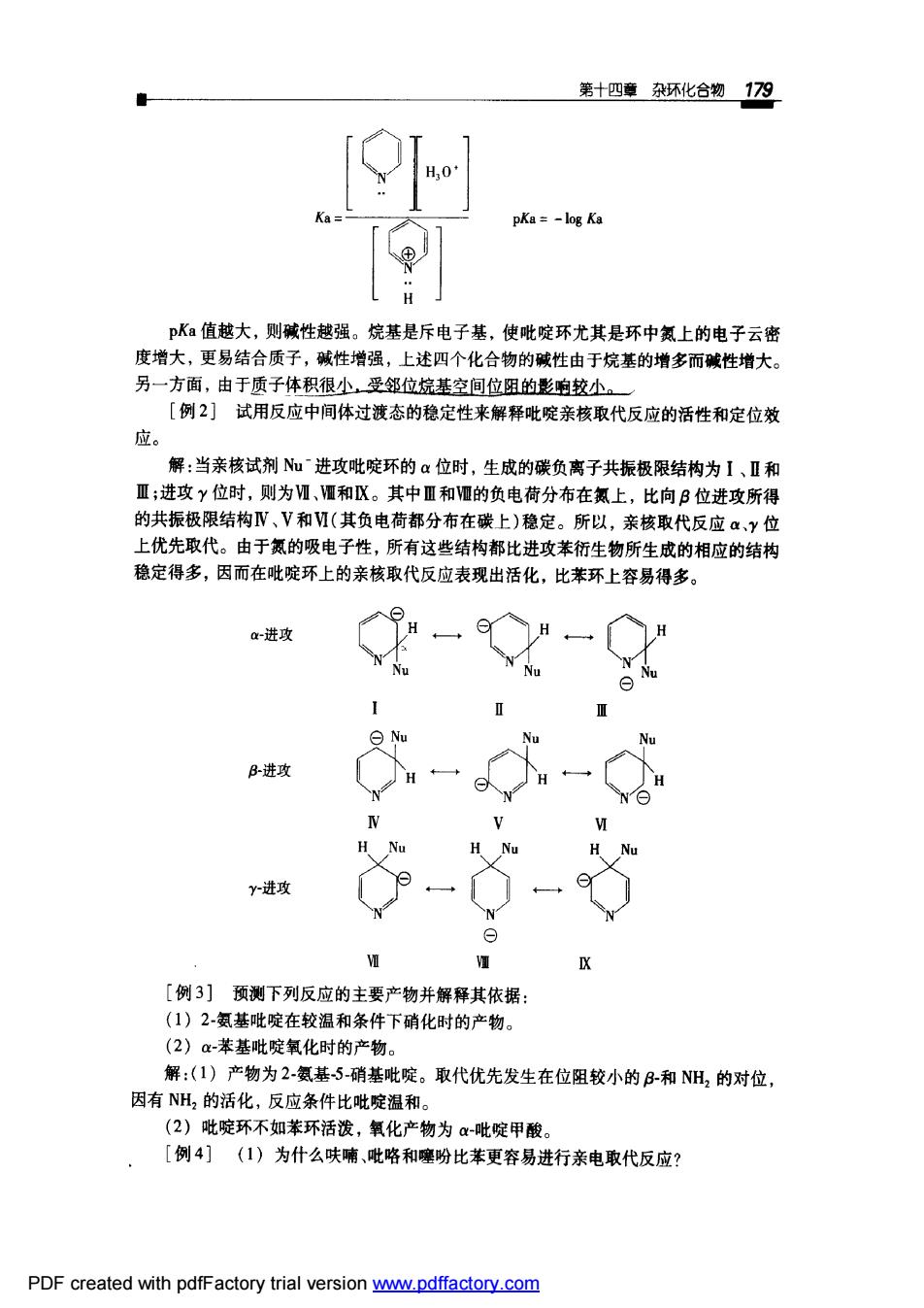
第十四章孙环化合物1☑9 pKa=-log Ka pKa值越大,则碱性越强。烷基是斥电子基,使吡啶环尤其是环中氮上的电子云密 度增大,更易结合质子,碱性增强,上述四个化合物的碱性由于烷基的增多而碱性增大。 另一方面,由于质子体积很小,受邻位烷基空间位阻的影响较小。 [例2]试用反应中间体过渡态的稳定性来解释吡啶亲核取代反应的活性和定位效 解:当亲核试剂恤进攻吡啶环的α位时,生成的碳负离子共振极限结构为I、Ⅱ和 Ⅲ:进攻y位时,则为M,Ⅷ和X。其中Ⅲ和Ⅷ的负电荷分布在氮上,比向B位进攻所得 的共振极限结构W、V和M(其负电荷都分布在碳上)稳定。所以,亲核取代反应α,Yy位 上优先取代。由于氯的吸电子性,所有这些结构都比进攻苯衍生物所生成的相应的结构 稳定得多,因而在吡啶环上的亲核取代反应表现出活化,比苯环上容易得多。 -进攻 - B进攻 H+→ H M H Nu H N y进政 [例3]预测下列反应的主要产物并解释其依据: (1)2氨基吡啶在较温和条件下硝化时的产物。 (2)α-苯基毗啶氧化时的产物。 解:(1)产物为2氨基5-硝基吡啶。取代优先发生在位阻较小的B和NH2的对位 因有NH,的活化,反应条件比吡啶温和。 (2)吡啶环不如苯环活泼,氧化产物为α吡啶甲酸。 [例4](1)为什么呋喃、吡咯和噻盼比苯更容易进行亲电取代反应? PDF created with pdfFactory trial version ww.pdffactory.com
PDF created with pdfFactory trial version www.pdffactory.com

180有机化学学习指导 (2)为什么芳香性的顺序是噻吩>吡咯>呋哺? 解:(1)由于在呋喃、吡咯和吩环上杂原子的轨道有一对电子参与共轭,组成 个五中心六电子的环状的闭合共轭体系。相对于苯的六电子六中心大π键而言,整个环 上的π电子云密度比苯大,因此比苯更容易进行亲电取代反应。 (2)因为这些环中的杂原子的电负性顺序是0>N>S,对芳环供电子的能力正好 相反,即呋喃中的0比吡略中的N更不易供电子给环构成芳香大π键,故芳香性最差 噻吩中的S较易供电子给环,故芳香性较强。 [例5]1.为什么吡咯没有碱性,而吡啶是有碱性的?请预测它的碱性比六氢吡啶 强还是弱?为什么? 2.请写出吡啶和下列化合物反应的产物: (1)B(CH) (2)H,s0 (3)CH, (4)t-C,HBr (5)C,H,C00oH(6)C0, 解:山.吡咯N原子p轨道中的二个电子已参与形成芳香大π键,不再具有给出电子 对的能力,故吡咯没有碱性。吡啶与吡咯不同,其N原子上的未共用电子对处于p杂 化轨道中,它并不参与环上的共轭体系,因此可以和质子结合或给出电子。 在六氢吡啶中,N上的未共用电子是p电子,其s成份少,它比吡啶中的p电子 更易提供未共用电子,亦即碱性要比吡啶强。 2.吡啶具有典型叔胺性质,故生成的产物是 (1)CHgN'B-(CH3) (2)(C,H,NH)'HSO (C,H,NH)SO; (3)[CH,N'GH,]I- (4)C,H,N'HBr+(CH,),C-CH,从卤代烷消除HX (5)P ©,氧化贱院 (6)C,H,NC0,可作酸敏感性化合物的氧化剂 [例6]从呋喃合成5-硝基呋嘴2-甲酸。 解:因呋喃对酸不稳定,故不能先用混酸进行硝化,可考虑先引人一个吸电子的定 位基使呋哺环纯化,然后再进行硝化,最后再转变成5硝基呋哺2甲酸。合成路线如 下: +0既 HNO, COCH, H 0,N人gcooa ON COOH [例7]吡喃环中也有六个电子,为什么没有芳香性? 解:吡晴环上虽也有六个电子,但4个电子来自π健,另2个电子来自氧原子,且 C,是邓杂化,没有轨道可提供交叠成闭环的大r键,因而没有芳香性。如果使C,成 PDF created with pdfFactory trial version ww.pdffactory.com
PDF created with pdfFactory trial version www.pdffactory.com