
40 第四章 糖类 一、教学目的与要求 1、 熟悉几种重要的单糖、双糖和多糖的结构特点 2、 了解糖类的的物理性质和化学性质 3、 掌握淀粉的糊化与老化对食品的影响及应用 二、教学重点与难点 1、 蔗糖的性质及其在烹饪中的应用 2、淀粉的糊化与老化对食品的影响 三、课时安排与教学方法 教学内容 (计划/实际) 课时数 课程类型/ 教学方法 第一节 糖类概述 1/ 理论/ 第二节 单糖 2/ 理论/ 第三节 低聚糖 2/ 理论/ 第四节 多糖 4/ 理论/ 实 验 淀粉的性质 2/ 实验/ 合计 11/ 四、教学过程 第四章 糖类 第一节 糖类概述 一、糖类在自然界中的存在 糖类是食品的重要成分。它广泛存在于植物体中,是绿色植物经过光合作用的产物,占植物体干重的 50%~80%。 动物体内不能制造糖类,而是以食用的植物的糖类为能源。因此糖类主要是由植物性食品供给。 二、糖类的生理功能 1、 糖类是人和动物体主要的供能物质。 2、 糖类可与脂类形成糖脂,是构成神经组织与细胞膜的成分; 3、 糖类还可与蛋白质结合成糖蛋白及粘蛋白,它们都是具有重要生理功能的物质。 三、糖类与食品加工的关系 1、 还原糖能使食品变褐; 2、 保持食品的粘弹性(淀粉与果胶等); 3、 赋予食品甜味(单糖、二糖)
40 第四章 糖类 一、教学目的与要求 1、 熟悉几种重要的单糖、双糖和多糖的结构特点 2、 了解糖类的的物理性质和化学性质 3、 掌握淀粉的糊化与老化对食品的影响及应用 二、教学重点与难点 1、 蔗糖的性质及其在烹饪中的应用 2、淀粉的糊化与老化对食品的影响 三、课时安排与教学方法 教学内容 (计划/实际) 课时数 课程类型/ 教学方法 第一节 糖类概述 1/ 理论/ 第二节 单糖 2/ 理论/ 第三节 低聚糖 2/ 理论/ 第四节 多糖 4/ 理论/ 实 验 淀粉的性质 2/ 实验/ 合计 11/ 四、教学过程 第四章 糖类 第一节 糖类概述 一、糖类在自然界中的存在 糖类是食品的重要成分。它广泛存在于植物体中,是绿色植物经过光合作用的产物,占植物体干重的 50%~80%。 动物体内不能制造糖类,而是以食用的植物的糖类为能源。因此糖类主要是由植物性食品供给。 二、糖类的生理功能 1、 糖类是人和动物体主要的供能物质。 2、 糖类可与脂类形成糖脂,是构成神经组织与细胞膜的成分; 3、 糖类还可与蛋白质结合成糖蛋白及粘蛋白,它们都是具有重要生理功能的物质。 三、糖类与食品加工的关系 1、 还原糖能使食品变褐; 2、 保持食品的粘弹性(淀粉与果胶等); 3、 赋予食品甜味(单糖、二糖)

41 四、糖类的结构 1、组成:糖类由碳、氢、氧三种元素组成。 2、通式:其中大多数成员的氢与氧之比为 2:1,与水组成相同,可用通式 Cn(H20)m 来表示,故称为碳 水化合物。但亦有例外,如在自然界中存在的脱氧核糖(C5H1004)及鼠李糖(C6H1205),根据它们的结构和性质应 该属于糖类,但其组成并不符合上面通式;而有些化合物,如甲醛(CH20)醋酸(C2H402),乳酸(C3H603)及苯三酚 (C6H603)等虽然分子组成符合上述通式,但从结构及性质上讲,则与糖类完全不同,因此,碳水化合物已失去 原有的涵义了。 3、结构特点:从化学结构特点来说,糖类是多羟基醛或多 羟基酮及它们的缩聚物和衍生物。 五、糖类的分类 糖类根据结构和性质,可以分为单糖、低聚糖和多糖 1、单糖 单糖是糖类的基本单位,即单独存在不能再被水解的多羟基醛或多羟基酮。 分类:根据每一成员的组成碳原子数又分为丙糖(三碳糖)、丁糖(四碳糖)、戊糖(五碳糖)、己 糖(六碳糖)等,其中以己糖在自然界分布最广。 单糖又按羰基的类型不同而分为醛糖和酮糖。 2、低聚糖 也叫寡糖,系由2~10个单糖分子脱水缩合而成的糖。完全水解后得到相应分子数的单糖。 分类:根据聚合度又分为二糖、三糖、四糖等等,其中以二糖的分布最广,也最为重要。 3、多聚糖 多聚糖是少则几十个,多则几千、几万个单糖分子的脱水缩聚产物,它们都是高分子化合物。 完全水解后产生相应数目的单糖分子。 分类:多聚糖习惯上简称多糖,根据其组成单体的种数又分为 均一多糖(同多糖)和混合多糖(杂多糖)。 均一多糖:由一种单糖所组成的,例如淀粉、纤维素、糖元等 混合多糖:由两种以上单糖组成,如半纤维素、果胶等。 第二节 单 糖 单糖是低聚糖和多聚糖的基本构成单位。所有食物中的低聚 糖和多聚糖摄入人体后,都必须水解成单糖后,才能被机体吸收和利用。 一、单糖的分子结构 前已述及单糖按碳原子数可分为丙糖、丁糖、戊糖、己糖等;按羰基又可分为醛糖和酮糖,这里 先讨论醛糖,然后再用综合比较的方法介绍酮糖。 (一)醛单糖 醛单糖按多羟基醛的构造来描述,其最简单的成员应是羟基 乙醛[CH2(OH)CHO]。这个化合物没有手性碳原子,所以只有一种构型式。当羟基乙醛分子中插入一个 -CHOH-基团形成其高一级成员甘油醛(应称为醛糖)时,就产生了一个手性碳原子,从而有一对对映异构 体。即: 对于这个甘油醛,我们在立体异构化学那一章中已经熟悉了。它被选作确定分子相对构型的基准 物质,上述左边的那个构型是右旋体,指定作为D型的基准,右边的那个构型是左旋体,指定作为L 型的基准,分别叫做D(+)-甘油醛和L(-)-甘油醛。如果继续在甘油醛分子中增加-CHOH-基团,则会产 生两个系列的高级成员。为了简便起见,我们在这里只列出D系列的成员(到己糖为止)。 对 于 L系 列,要求学生自行练习后 写出。 自然界存在的单糖,多为D型,L型极少见。例如存在于一些天然树胶中的L(+)-树胶糖[也有人称
41 四、糖类的结构 1、组成:糖类由碳、氢、氧三种元素组成。 2、通式:其中大多数成员的氢与氧之比为 2:1,与水组成相同,可用通式 Cn(H20)m 来表示,故称为碳 水化合物。但亦有例外,如在自然界中存在的脱氧核糖(C5H1004)及鼠李糖(C6H1205),根据它们的结构和性质应 该属于糖类,但其组成并不符合上面通式;而有些化合物,如甲醛(CH20)醋酸(C2H402),乳酸(C3H603)及苯三酚 (C6H603)等虽然分子组成符合上述通式,但从结构及性质上讲,则与糖类完全不同,因此,碳水化合物已失去 原有的涵义了。 3、结构特点:从化学结构特点来说,糖类是多羟基醛或多 羟基酮及它们的缩聚物和衍生物。 五、糖类的分类 糖类根据结构和性质,可以分为单糖、低聚糖和多糖 1、单糖 单糖是糖类的基本单位,即单独存在不能再被水解的多羟基醛或多羟基酮。 分类:根据每一成员的组成碳原子数又分为丙糖(三碳糖)、丁糖(四碳糖)、戊糖(五碳糖)、己 糖(六碳糖)等,其中以己糖在自然界分布最广。 单糖又按羰基的类型不同而分为醛糖和酮糖。 2、低聚糖 也叫寡糖,系由2~10个单糖分子脱水缩合而成的糖。完全水解后得到相应分子数的单糖。 分类:根据聚合度又分为二糖、三糖、四糖等等,其中以二糖的分布最广,也最为重要。 3、多聚糖 多聚糖是少则几十个,多则几千、几万个单糖分子的脱水缩聚产物,它们都是高分子化合物。 完全水解后产生相应数目的单糖分子。 分类:多聚糖习惯上简称多糖,根据其组成单体的种数又分为 均一多糖(同多糖)和混合多糖(杂多糖)。 均一多糖:由一种单糖所组成的,例如淀粉、纤维素、糖元等 混合多糖:由两种以上单糖组成,如半纤维素、果胶等。 第二节 单 糖 单糖是低聚糖和多聚糖的基本构成单位。所有食物中的低聚 糖和多聚糖摄入人体后,都必须水解成单糖后,才能被机体吸收和利用。 一、单糖的分子结构 前已述及单糖按碳原子数可分为丙糖、丁糖、戊糖、己糖等;按羰基又可分为醛糖和酮糖,这里 先讨论醛糖,然后再用综合比较的方法介绍酮糖。 (一)醛单糖 醛单糖按多羟基醛的构造来描述,其最简单的成员应是羟基 乙醛[CH2(OH)CHO]。这个化合物没有手性碳原子,所以只有一种构型式。当羟基乙醛分子中插入一个 -CHOH-基团形成其高一级成员甘油醛(应称为醛糖)时,就产生了一个手性碳原子,从而有一对对映异构 体。即: 对于这个甘油醛,我们在立体异构化学那一章中已经熟悉了。它被选作确定分子相对构型的基准 物质,上述左边的那个构型是右旋体,指定作为D型的基准,右边的那个构型是左旋体,指定作为L 型的基准,分别叫做D(+)-甘油醛和L(-)-甘油醛。如果继续在甘油醛分子中增加-CHOH-基团,则会产 生两个系列的高级成员。为了简便起见,我们在这里只列出D系列的成员(到己糖为止)。 对 于 L系 列,要求学生自行练习后 写出。 自然界存在的单糖,多为D型,L型极少见。例如存在于一些天然树胶中的L(+)-树胶糖[也有人称

42 为L(+)-阿拉伯糖]便是这种少见现象的一例。至于D型糖,则分布极广,为丁糖中的D(-)-赤藓糖(存 在于赤藓藻中);戊糖中的D(-)-核糖(存在于核酸中)、D(-)-树胶糖(存在于某些糖苷中)、D(+)-木糖 (存在于木胶和多种植物的茎、干中);至于最重要的己醛糖,除了众所周知的D(+)葡萄糖外,尚有D (+)-甘露糖(存在于某些植物和水果中)和D(+)-半乳糖(存在人及哺乳动物的乳汁中)。 从表4-1所列的醛单糖D-型系列化合物可知,它们何以会存在如此多的立体异构体,就是因为它 们的分子中含有手性碳原子的缘故,而且都符合2 n这个公式。如以己醛糖为例,它含有4个手性碳原 子,所以2 4=16,它应有16种对应异构体(除已写出的8种D型体外,尚有8种L型体)。 在立体化学中,为了研究上的方便。对于那些 含有多个 手性碳原子 的化合物, 把那些只有 第一个手性 碳 原子 不同的化 合物,叫做 差向异构 物(也 叫表里异 构物)。即表4-1中用大括号联系在一起的一对化合物,如 D(+)-葡萄糖和D(+)-甘露糖等,都互为差向异构体。 (二)酮单糖 酮单糖的最简单的成员甘油酮 CH2-C-CH2 OH O OH 它不含 手性碳 原子 ,所以 没有 任何构 型异 构体。如果 在其分 子中 插入一 个-C H2 OH- 基团 ,则 得到的 丁酮 糖, 因含有 一个 手性 碳原 子, 应有两 个对 映异 构体 ,且按 照立 体化 学的 规则 ,分 别为D型和L型,即 依此类 推,当碳 原子数 增加 到6时 ,即 为己 酮糖 ,它 应含有 3个手 性碳 原子 ,按 公式2 3 =8,它 即应有8种对 映异构 体,其 中有4种D型 体,4种L型 体。其实 在自 然界,迄今为 止,只 发现 一种 主要的己酮糖,这就是果糖, 而且 是D(-) -果糖 ,其 余的七 种都 是用人 工方 法合成 的。 D(-)-果糖的构型式为: 这个构型式的C3-C5与D(+)-葡萄糖和D(+)-甘露糖的C3 -C5构型相同。所以也可以看成是它们的 差向异构体,但实际不是,因为它们不属于同一个系列。 (三)单糖的环状结构 无论是醛单糖还是酮单糖,因其分子中既含有羰基,又含 有羟基,故而能够按半缩醛(酮)的作用方式生成环状结构。 现以葡萄糖和果糖为例:
42 为L(+)-阿拉伯糖]便是这种少见现象的一例。至于D型糖,则分布极广,为丁糖中的D(-)-赤藓糖(存 在于赤藓藻中);戊糖中的D(-)-核糖(存在于核酸中)、D(-)-树胶糖(存在于某些糖苷中)、D(+)-木糖 (存在于木胶和多种植物的茎、干中);至于最重要的己醛糖,除了众所周知的D(+)葡萄糖外,尚有D (+)-甘露糖(存在于某些植物和水果中)和D(+)-半乳糖(存在人及哺乳动物的乳汁中)。 从表4-1所列的醛单糖D-型系列化合物可知,它们何以会存在如此多的立体异构体,就是因为它 们的分子中含有手性碳原子的缘故,而且都符合2 n这个公式。如以己醛糖为例,它含有4个手性碳原 子,所以2 4=16,它应有16种对应异构体(除已写出的8种D型体外,尚有8种L型体)。 在立体化学中,为了研究上的方便。对于那些 含有多个 手性碳原子 的化合物, 把那些只有 第一个手性 碳 原子 不同的化 合物,叫做 差向异构 物(也 叫表里异 构物)。即表4-1中用大括号联系在一起的一对化合物,如 D(+)-葡萄糖和D(+)-甘露糖等,都互为差向异构体。 (二)酮单糖 酮单糖的最简单的成员甘油酮 CH2-C-CH2 OH O OH 它不含 手性碳 原子 ,所以 没有 任何构 型异 构体。如果 在其分 子中 插入一 个-C H2 OH- 基团 ,则 得到的 丁酮 糖, 因含有 一个 手性 碳原 子, 应有两 个对 映异 构体 ,且按 照立 体化 学的 规则 ,分 别为D型和L型,即 依此类 推,当碳 原子数 增加 到6时 ,即 为己 酮糖 ,它 应含有 3个手 性碳 原子 ,按 公式2 3 =8,它 即应有8种对 映异构 体,其 中有4种D型 体,4种L型 体。其实 在自 然界,迄今为 止,只 发现 一种 主要的己酮糖,这就是果糖, 而且 是D(-) -果糖 ,其 余的七 种都 是用人 工方 法合成 的。 D(-)-果糖的构型式为: 这个构型式的C3-C5与D(+)-葡萄糖和D(+)-甘露糖的C3 -C5构型相同。所以也可以看成是它们的 差向异构体,但实际不是,因为它们不属于同一个系列。 (三)单糖的环状结构 无论是醛单糖还是酮单糖,因其分子中既含有羰基,又含 有羟基,故而能够按半缩醛(酮)的作用方式生成环状结构。 现以葡萄糖和果糖为例:

43 开链式 环 式 很明显,原来开链式的醛基碳原子是非手性碳原子。现在成环以后,由于醛基氧原子变成了半 缩醛羟基,于是新产生一个手性碳原子,从而使得环式比开链式的对映异构体增加了一倍,即环式 中以波纹线标示的羟基,因其在碳链的右侧或左侧而形成一对对映体。 同样,对于己酮糖来说,如以D(-)-果糖为例,也有类似的情况。 即原来的酮基氧原子变成了半缩酮羟基,也新增加了一个手性碳原子,相应的对映异构体数目也增加 了一倍。 上述讨论,不是简单的符号游戏,而是通过糖溶液的变旋光现象,确证上述转变的存在,而且在 水溶液中确有下列平衡体系存在。 这里要说明的是:对于那个半缩醛羟基来说,它的空间位置也有两种选择,于是规定:凡是半缩醛 羟基与其定位的碳原子(即C5)上的羟基在链的同一侧的叫α型;在不同一侧的叫β型。 仿此,我们也可以写出D(-)-果糖相应的平衡体系,即: α -D (-)-果 糖 D (-)-果 糖 β -D (-)-果 糖
43 开链式 环 式 很明显,原来开链式的醛基碳原子是非手性碳原子。现在成环以后,由于醛基氧原子变成了半 缩醛羟基,于是新产生一个手性碳原子,从而使得环式比开链式的对映异构体增加了一倍,即环式 中以波纹线标示的羟基,因其在碳链的右侧或左侧而形成一对对映体。 同样,对于己酮糖来说,如以D(-)-果糖为例,也有类似的情况。 即原来的酮基氧原子变成了半缩酮羟基,也新增加了一个手性碳原子,相应的对映异构体数目也增加 了一倍。 上述讨论,不是简单的符号游戏,而是通过糖溶液的变旋光现象,确证上述转变的存在,而且在 水溶液中确有下列平衡体系存在。 这里要说明的是:对于那个半缩醛羟基来说,它的空间位置也有两种选择,于是规定:凡是半缩醛 羟基与其定位的碳原子(即C5)上的羟基在链的同一侧的叫α型;在不同一侧的叫β型。 仿此,我们也可以写出D(-)-果糖相应的平衡体系,即: α -D (-)-果 糖 D (-)-果 糖 β -D (-)-果 糖
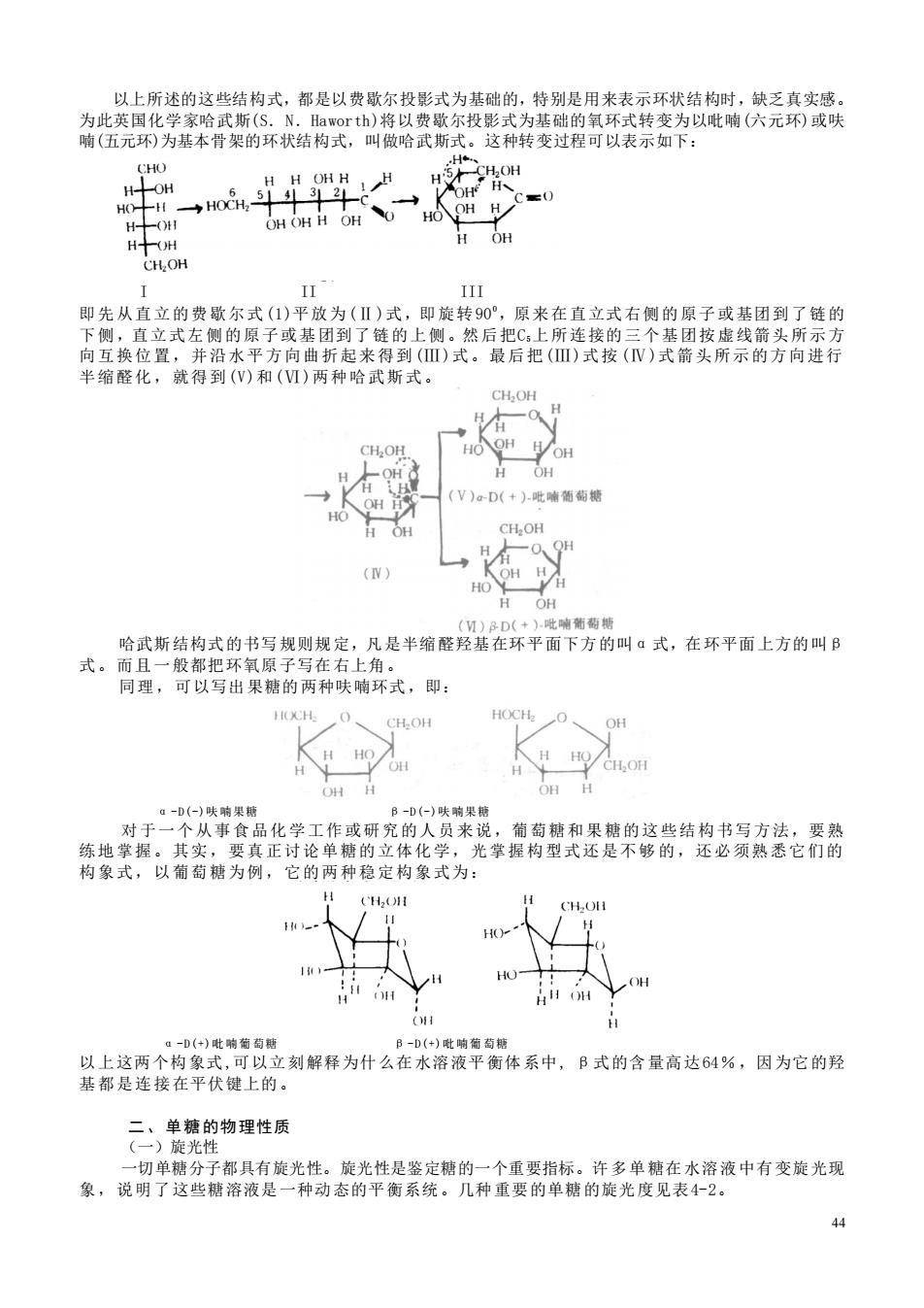
44 以上所述的这些结构式,都是以费歇尔投影式为基础的,特别是用来表示环状结构时,缺乏真实感。 为此英国化学家哈武斯(S.N.Haworth)将以费歇尔投影式为基础的氧环式转变为以吡喃(六元环)或呋 喃(五元环)为基本骨架的环状结构式,叫做哈武斯式。这种转变过程可以表示如下: I II III 即先从直立的费歇尔式(1)平放为(Ⅱ)式,即旋转900,原来在直立式右侧的原子或基团到了链的 下侧,直立式左侧的原子或基团到了链的上侧。然后把C5上所连接的三个基团按虚线箭头所示方 向互换位置,并沿水平方向曲折起来得到(Ⅲ)式。最后把(Ⅲ)式按 (Ⅳ)式箭头所示的方向进行 半缩醛化,就得到(V)和(Ⅵ)两种哈武斯式。 哈武斯结构式的书写规则规定,凡是半缩醛羟基在环平面下方的叫α式,在环平面上方的叫β 式。而且一般都把环氧原子写在右上角。 同理,可以写出果糖的两种呋喃环式,即: α -D (-)呋 喃果糖 β -D (-)呋 喃果糖 对于一个从事食品化学工作或研究的人员来说,葡萄糖和果糖的这些结构书写方法,要熟 练地掌握。其实,要真正讨论单糖的立体化学,光掌握构型式还是不够的,还必须熟悉它们的 构象式,以葡萄糖为例,它的两种稳定构象式为: α -D(+)吡 喃葡 萄糖 β -D(+)吡 喃葡 萄糖 以上这两个构象式,可以立刻解释为什么在水溶液平衡体系中, β式的含量高达64%,因为它的羟 基都是连接在平伏键上的。 二、单糖的物理性质 (一)旋光性 一切单糖分子都具有旋光性。旋光性是鉴定糖的一个重要指标。许多单糖在水溶液中有变旋光现 象,说明了这些糖溶液是一种动态的平衡系统。几种重要的单糖的旋光度见表4-2
44 以上所述的这些结构式,都是以费歇尔投影式为基础的,特别是用来表示环状结构时,缺乏真实感。 为此英国化学家哈武斯(S.N.Haworth)将以费歇尔投影式为基础的氧环式转变为以吡喃(六元环)或呋 喃(五元环)为基本骨架的环状结构式,叫做哈武斯式。这种转变过程可以表示如下: I II III 即先从直立的费歇尔式(1)平放为(Ⅱ)式,即旋转900,原来在直立式右侧的原子或基团到了链的 下侧,直立式左侧的原子或基团到了链的上侧。然后把C5上所连接的三个基团按虚线箭头所示方 向互换位置,并沿水平方向曲折起来得到(Ⅲ)式。最后把(Ⅲ)式按 (Ⅳ)式箭头所示的方向进行 半缩醛化,就得到(V)和(Ⅵ)两种哈武斯式。 哈武斯结构式的书写规则规定,凡是半缩醛羟基在环平面下方的叫α式,在环平面上方的叫β 式。而且一般都把环氧原子写在右上角。 同理,可以写出果糖的两种呋喃环式,即: α -D (-)呋 喃果糖 β -D (-)呋 喃果糖 对于一个从事食品化学工作或研究的人员来说,葡萄糖和果糖的这些结构书写方法,要熟 练地掌握。其实,要真正讨论单糖的立体化学,光掌握构型式还是不够的,还必须熟悉它们的 构象式,以葡萄糖为例,它的两种稳定构象式为: α -D(+)吡 喃葡 萄糖 β -D(+)吡 喃葡 萄糖 以上这两个构象式,可以立刻解释为什么在水溶液平衡体系中, β式的含量高达64%,因为它的羟 基都是连接在平伏键上的。 二、单糖的物理性质 (一)旋光性 一切单糖分子都具有旋光性。旋光性是鉴定糖的一个重要指标。许多单糖在水溶液中有变旋光现 象,说明了这些糖溶液是一种动态的平衡系统。几种重要的单糖的旋光度见表4-2