4.通过降低活化能加快化学反应速度。 Transition state ( 'K8.I9ue 4G¥ uncat cat P Reaction coordinate
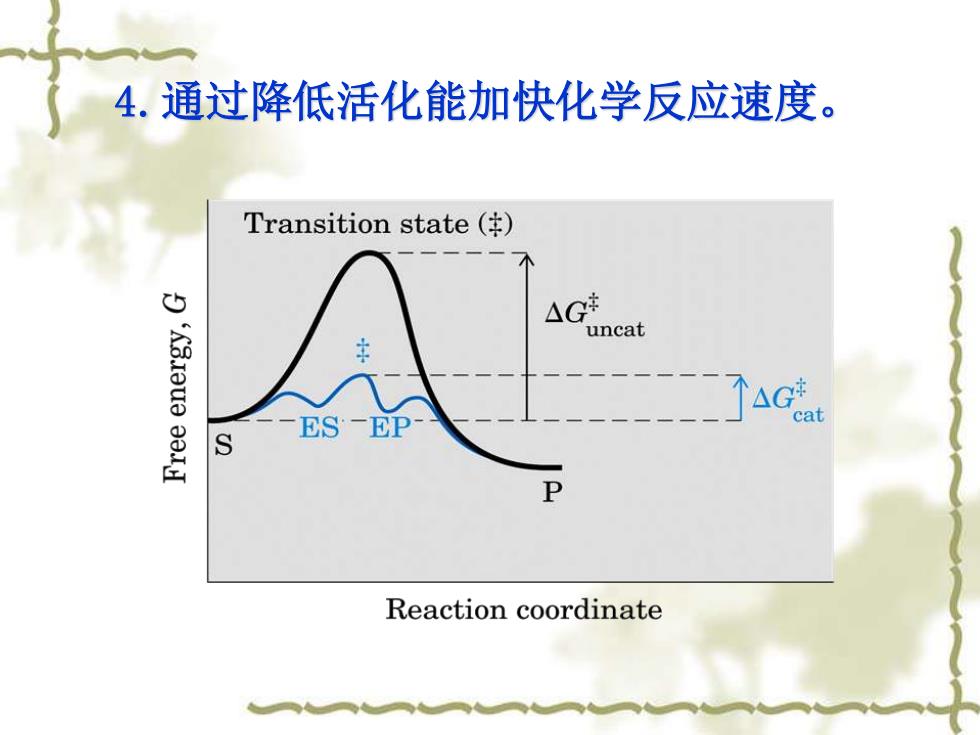
4.通过降低活化能加快化学反应速度

例2H202→2H20+02 反应 活化能 非催化反应 75.24kJ/mo1 钯催化反应 48.9kJ/mo1 H202酶催化 8.36kJ/mol
例 2H2 O2 → 2H2 O + O2 反 应 活化能 非催化反应 75.24kJ/mol 钯催化反应 48.9kJ/mol H2 O2酶催化 8.36kJ/mol

,酶是特殊的催化剂 (1)高的催化效率 以摩尔为单位进行比较,酶的催化效率比化学催化1 剂高107~1013倍,比非催化反应高108~1020倍。 例2H202→2H20+02 1mo1eH202酶 能催化5×10mo1eH20,2的分解 1mole Fe3+ 只能催化6×10-4mo1eH202的分解
(1)高的催化效率 以摩尔为单位进行比较,酶的催化效率比化学催化 剂高107~1013倍,比非催化反应高108~1020倍。 例 2H2 O2→2H2 O+O2 1mole H2 O2酶 能催化 5×106mole H2 O2的分解 1mole Fe3+ 只能催化6×10-4mole H2 O2的分解 ◆ 酶是特殊的催化剂

酶与一般催化剂催化效率的比较 底物 催化剂 反应温度 反应速度常数 尿素 H+ 62 7.4×10-7 脲酶 21 5.0×106 过氧化氢 Fe 2+ 22 56 过氧化氢酶 22 3.5×107 通常要高出一般催化剂催化活性的107-1013倍
酶与一般催化剂催化效率的比较 底物 催化剂 反应温度 反应速度常数 尿素 H + 62 7.4 10-7 脲酶 21 5.0 106 过氧化氢 Fe 2+ 22 56 过氧化氢酶 22 3.5 107 通常要高出一般催化剂催化活性的107 -1013倍

转换数(turnover number,keat):每秒钟或每分 钟,每个酶分子转换底物的分子数,或每秒钟或每 分钟每摩尔酶转换底物的摩尔数。 Table 8-7 Turnover numbers*(kcat)of some enzymes Enzyme Substrate kcat(s-1) Catalase H2O2 40,000,000 Carbonic anhydrase HCO3 400,000 Acetylcholinesterase Acetylcholine 140,000 B-Lactamase Benzylpenicillin 2,000 Fumarase Fumarate 800 RecA protein (ATPase) ATP 0.4 *Number of substrate molecules transformed per second per molecule of enzyme
转换数(turnover number,kcat): 每秒钟或每分 钟,每个酶分子转换底物的分子数,或每秒钟或每 分钟每摩尔酶转换底物的摩尔数