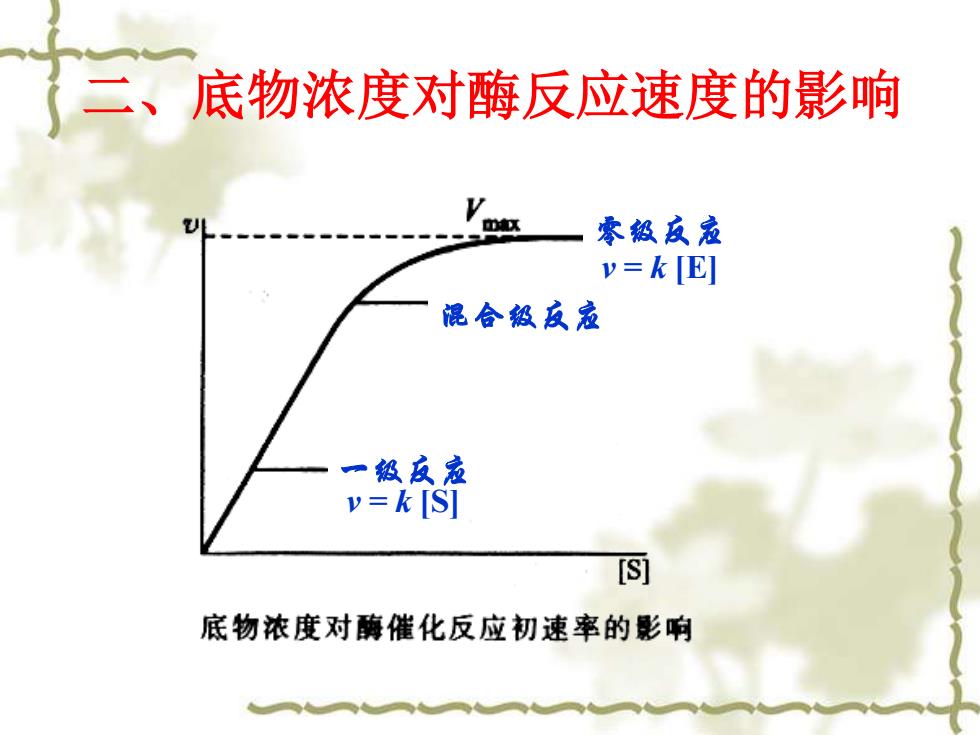
二、底物浓度对酶反应速度的影响 零级反应 y=k [E] 混合级反应 级反应 y=k [S] [S] 底物浓度对酶催化反应初速率的影响
二、底物浓度对酶反应速度的影响 一级反应 v = k [S] 零级反应 v = k [E] 混合级反应
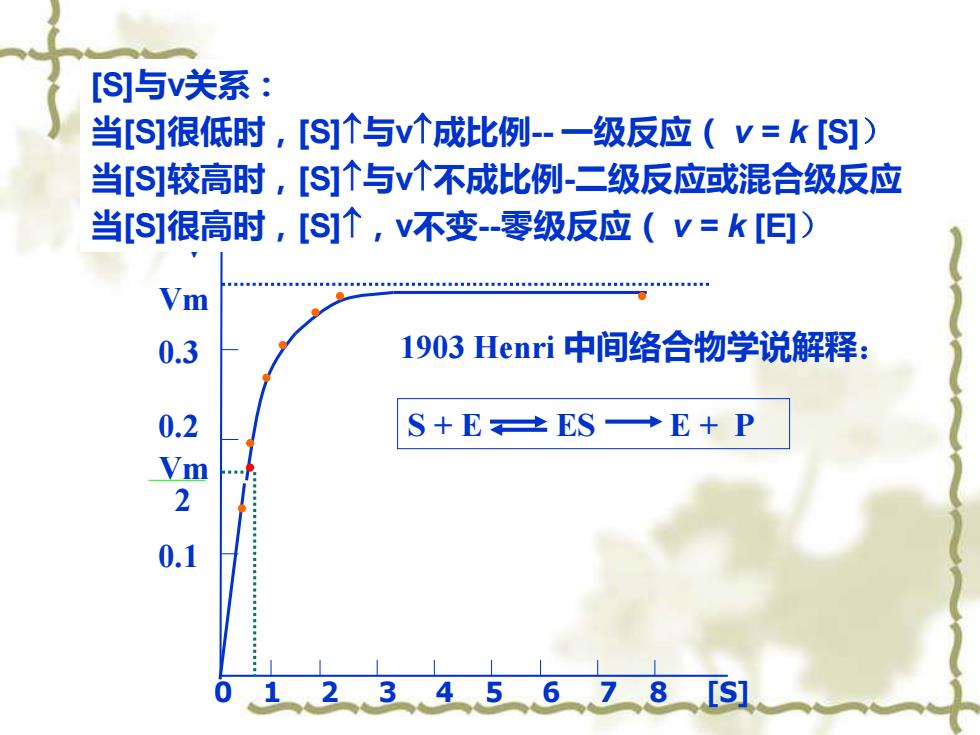
[S]与v关系: 当[S]很低时,[S]个与v个成比例-一级反应(V=k[S]) 当[S]较高时,[S]↑与v个不成比例-二级反应或混合级反应 当S]很高时,[S]个,v不变-零级反应(v=k[E]) Vm 0.3 1903 Henri中间络合物学说解释: S+E之ES→E+P 20 45678[S]
v Vm 0.3 0.2 Vm 2 0.1 [S]与v关系: 当[S]很低时,[S]与v成比例- 一级反应( v = k [S]) 当[S]较高时,[S]与v不成比例-二级反应或混合级反应 当[S]很高时,[S],v不变-零级反应( v = k [E]) 0 1 2 3 4 5 6 7 8 [S] S + E ES E + P 1903 Henri 中间络合物学说解释:

Michaelis-Menten方程(1913年) 1913年Michaelis和 Menten推导了米氏方程 VnxIS] V= K+[S] Leonor Michaelis 1875-1949 Maud Menten 1879-1960
1913年Michaelis和 Menten推导了米氏方程 K [S] V [S] v m max + = Michaelis-Menten方程(1913年)

假设E+SKES 的平衡迅速建立且只考虑 ES kE+P 逆反应或略不计,反 应速率由最高速度与底物浓度决定. v Vmax f(S) 推导 v Vmax /(1+Ks/[S]) 或 V= Vmax [S] Ks+[S]
假设 E+S ES 的平衡迅速建立且只考虑 ES E + P 逆反应或略不计,反 应速率由最高速度与底物浓度决定. v = Vmax f(S) v = Vmax / (1 +KS /[S]) 或 v = Vmax [S] KS + [S] 推导 KS k

1925年Briggs和Haldame对米氏方程作了一次 重要的修正,提出了恒态(稳态)的概念。 K1 K3 E+S ES -E+P K2 所谓恒态是指反应进行一定时间后,S的生 成速度和ES的分解速度相等,亦即ES的净生成速 度为零,此时ES的浓度不再改变,达到恒态,也 称稳态
1925年Briggs和Haldame对米氏方程作了一次 重要的修正,提出了恒态(稳态)的概念。 E + S ES E + P k1 k2 k3 所谓恒态是指反应进行一定时间后,ES的生 成速度和ES的分解速度相等,亦即ES的净生成速 度为零,此时ES的浓度不再改变,达到恒态,也 称稳态