盐析机理示意图
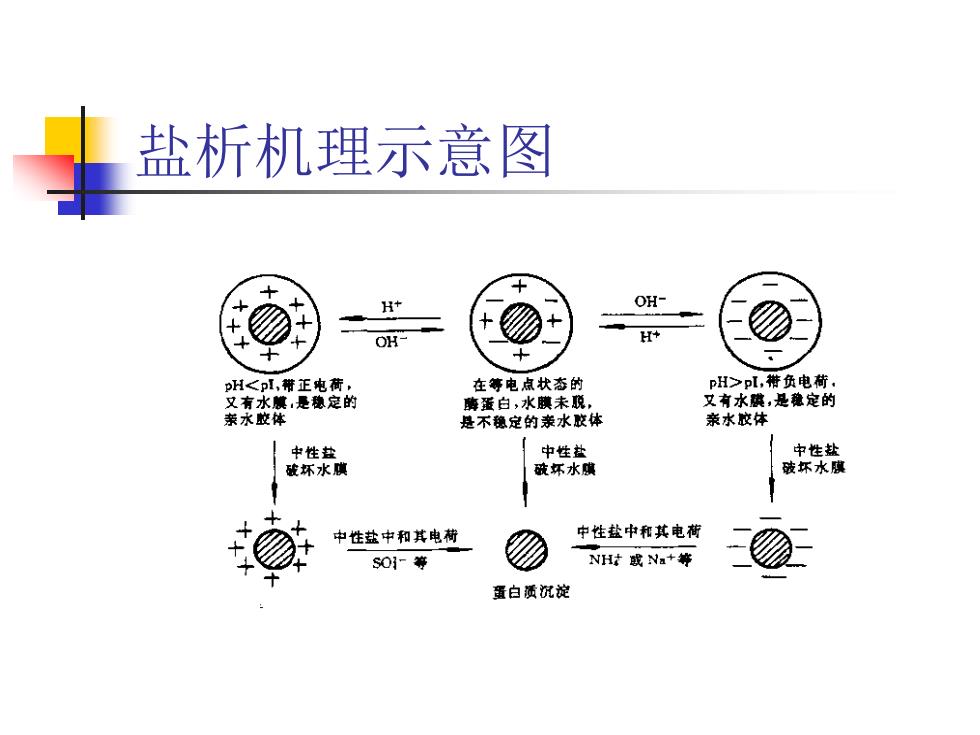
盐析机理示意图
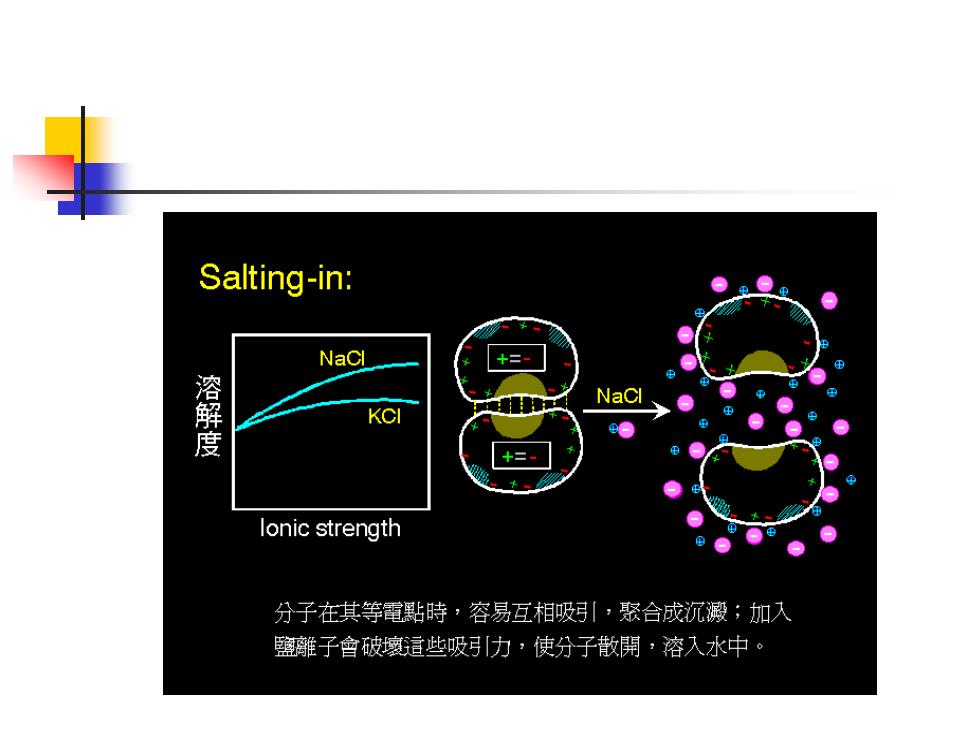
Salting-in: NaCl +三 溶解度 NaCl KC + lonic strength 分子在其等霜點時,容易互相吸好引·聚合成沉激;加入 鹽離子會破壤這些吸引力·使分子散開·溶入水中
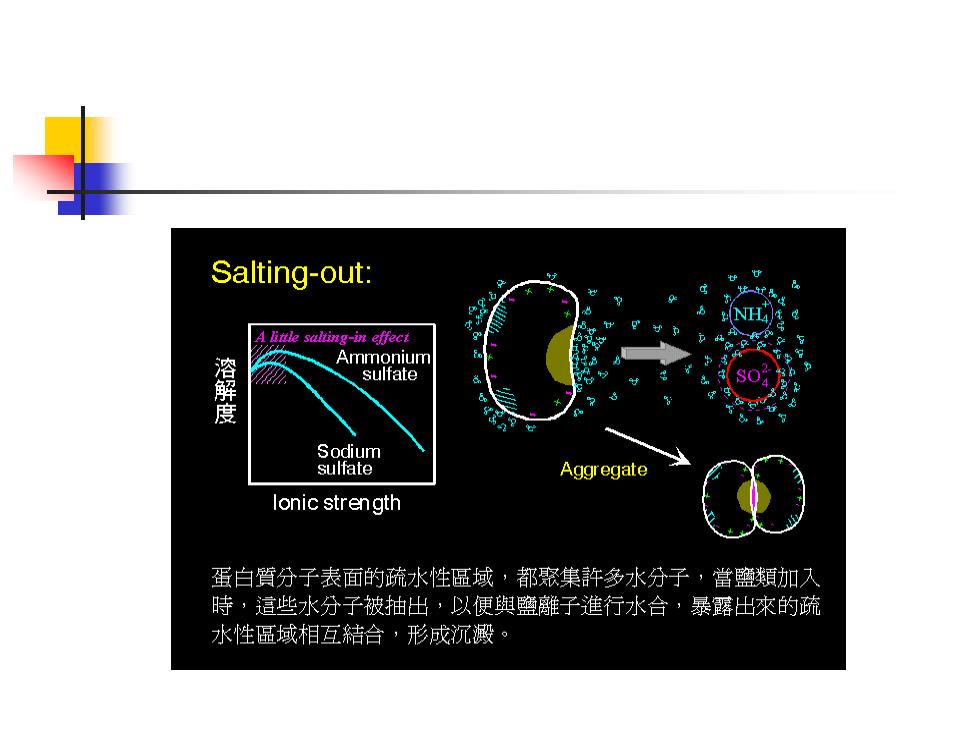
Salting-out: tle salting-in effect Ammonium 溶解度 sulfate Sodium sulfate Aggregate lonic stren gth 蛋白質分子表面的疏水性區域,都聚集許多水分子,當鹽類加入 時,這些水分子被抽出,以便與鹽離子進行水合,暴露出來的疏 水性區域相互結合,形成沉澱

◼ ①盐离子与蛋白质分子争夺水分子,降低了用于溶 解蛋白质的有效水量,减弱了蛋白质的水合程度, 破坏了蛋白表面的水化膜,导致蛋白质溶解度下降; ◼ ②盐离子电荷的中和作用,使蛋白质溶解度下降; ◼ ③盐离子引起原本在蛋白质分子周围有序排列的水 分子的极化,使水活度降低。 盐析的机理
◼ ①盐离子与蛋白质分子争夺水分子,降低了用于溶 解蛋白质的有效水量,减弱了蛋白质的水合程度, 破坏了蛋白表面的水化膜,导致蛋白质溶解度下降; ◼ ②盐离子电荷的中和作用,使蛋白质溶解度下降; ◼ ③盐离子引起原本在蛋白质分子周围有序排列的水 分子的极化,使水活度降低。 盐析的机理

◼ Cohn方程式logS=β-KsI ◼ Ks盐析 ◼ β盐析 ◼ 二次盐析 盐析沉淀基础
◼ Cohn方程式logS=β-KsI ◼ Ks盐析 ◼ β盐析 ◼ 二次盐析 盐析沉淀基础