
• 当温度升高时,0℃时冰的配位数从4.0增加至 1.50℃时的4.4、8.3℃时的4.9;与此同时,最邻 近水分子间的距离相应地从0.276nm增加至0.29nm 和0.305nm。 • 4 冰转变成水伴随着最邻近水分子间距离的增加 (降低密度)和最邻近水分子评价数目的增加 (增加密度),由于后一个因素占优势,导致密 度的净增加。在3.98℃达到最大密度,之后逐渐 下降。在0~3.98℃,配位数增加效应占优势, 3.98℃之后,最邻近分子间距增加效应占优势。 • 5 水的低粘度:水分子的氢键排列是高度动态的, 在纳秒至皮秒间个别的水分子改变它与邻近水分 子的氢键关系,增加了水的运动和流动
• 当温度升高时,0℃时冰的配位数从4.0增加至 1.50℃时的4.4、8.3℃时的4.9;与此同时,最邻 近水分子间的距离相应地从0.276nm增加至0.29nm 和0.305nm。 • 4 冰转变成水伴随着最邻近水分子间距离的增加 (降低密度)和最邻近水分子评价数目的增加 (增加密度),由于后一个因素占优势,导致密 度的净增加。在3.98℃达到最大密度,之后逐渐 下降。在0~3.98℃,配位数增加效应占优势, 3.98℃之后,最邻近分子间距增加效应占优势。 • 5 水的低粘度:水分子的氢键排列是高度动态的, 在纳秒至皮秒间个别的水分子改变它与邻近水分 子的氢键关系,增加了水的运动和流动

第七节 水-溶质相互作用 一 宏观水平 • 水结合(Water binding)、水合(Hydration)、 持水力(Water holding capacity)。 • 1 在食品中,水结合和水合常被用来表示水与包 括细胞物质在内的亲水物质缔合的一般倾向,这 两个术语与宏观水平相称。 • 水结合的程度和强度取决于许多因素,包括非水 成分的本质、盐的组成、pH和温度
第七节 水-溶质相互作用 一 宏观水平 • 水结合(Water binding)、水合(Hydration)、 持水力(Water holding capacity)。 • 1 在食品中,水结合和水合常被用来表示水与包 括细胞物质在内的亲水物质缔合的一般倾向,这 两个术语与宏观水平相称。 • 水结合的程度和强度取决于许多因素,包括非水 成分的本质、盐的组成、pH和温度

• 2 持水力这个术语通常被用来描述由分子(通常 是以低浓度存在的大分子)构成的基体通过物理 方式截留大量水而阻止水渗出的能力。如果胶、 淀粉凝胶、动物细胞截留水。 物理截留的水甚至当组织化食品被切割或剁 碎时仍不会流出。在食品加工时表现出来的性质 几乎与纯水相同:如在干燥时易于被除去,在冻 结时易于转变成冰,可以作为溶剂。 物理截留的水整体流动被严格限制,但个别分 子的运动基本上与稀盐溶液中水分子的运动相同
• 2 持水力这个术语通常被用来描述由分子(通常 是以低浓度存在的大分子)构成的基体通过物理 方式截留大量水而阻止水渗出的能力。如果胶、 淀粉凝胶、动物细胞截留水。 物理截留的水甚至当组织化食品被切割或剁 碎时仍不会流出。在食品加工时表现出来的性质 几乎与纯水相同:如在干燥时易于被除去,在冻 结时易于转变成冰,可以作为溶剂。 物理截留的水整体流动被严格限制,但个别分 子的运动基本上与稀盐溶液中水分子的运动相同

• 食品持水力(食品截流水的能力)的损害会严重 影响食品质量,如:凝胶食品脱水收缩,冷冻食 品解冻时渗水,动物宰后生理变化使肌肉pH下降 导致香肠质量变差等。 二 分子水平 (一) 概述 • 溶质与水混合会同时改变这两个成分的性质。亲 水溶质会改变邻近水的结构和流动性,水会改变 亲水溶质的反应性,有时甚至改变结构。溶质的 疏水基团仅与邻近水分子微弱地作用,它们优先 选择非水环境
• 食品持水力(食品截流水的能力)的损害会严重 影响食品质量,如:凝胶食品脱水收缩,冷冻食 品解冻时渗水,动物宰后生理变化使肌肉pH下降 导致香肠质量变差等。 二 分子水平 (一) 概述 • 溶质与水混合会同时改变这两个成分的性质。亲 水溶质会改变邻近水的结构和流动性,水会改变 亲水溶质的反应性,有时甚至改变结构。溶质的 疏水基团仅与邻近水分子微弱地作用,它们优先 选择非水环境
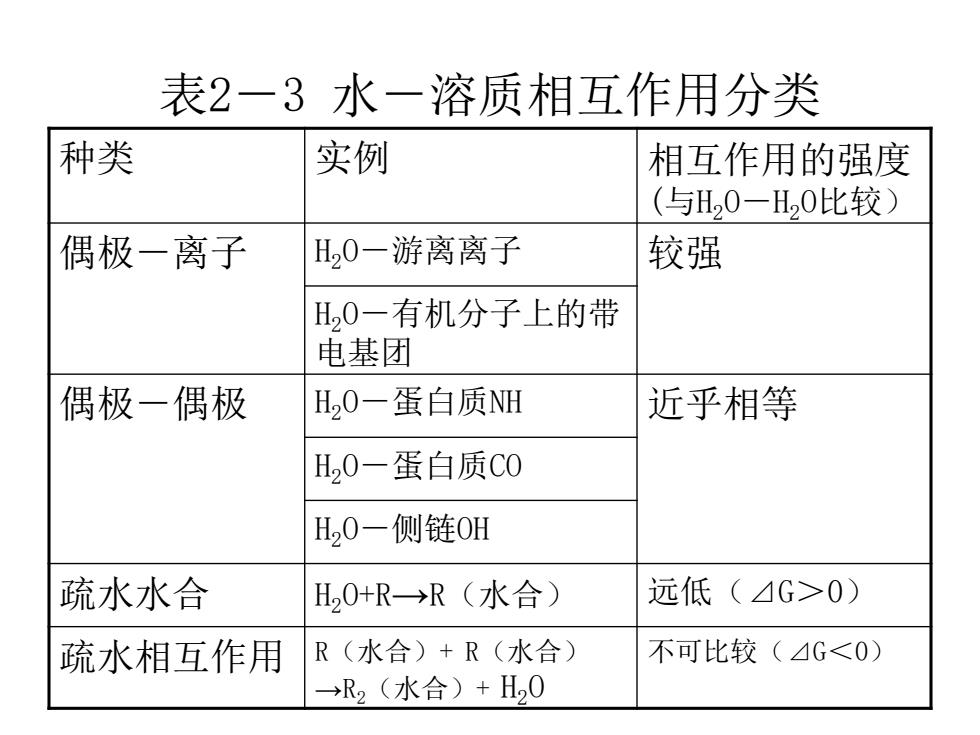
表2-3 水-溶质相互作用分类 种类 实例 相互作用的强度 (与H2O-H2O比较) 偶极-离子 H2O-游离离子 较强 H2O-有机分子上的带 电基团 偶极-偶极 H2O-蛋白质NH 近乎相等 H2O-蛋白质CO H2O-侧链OH 疏水水合 H2O+R→R(水合) 远低(⊿G>0) 疏水相互作用 R(水合)+ R(水合) →R2(水合)+ H2O 不可比较(⊿G<0)
表2-3 水-溶质相互作用分类 种类 实例 相互作用的强度 (与H2O-H2O比较) 偶极-离子 H2O-游离离子 较强 H2O-有机分子上的带 电基团 偶极-偶极 H2O-蛋白质NH 近乎相等 H2O-蛋白质CO H2O-侧链OH 疏水水合 H2O+R→R(水合) 远低(⊿G>0) 疏水相互作用 R(水合)+ R(水合) →R2(水合)+ H2O 不可比较(⊿G<0)