
的高低和化合物的性质选择合适的热源。一般80℃以下可用水浴,高于80℃用油浴。如果化合物较稳定,沸点较高又不易燃烧的,可在石棉网上加热(空气浴),亦可用电热套加热。(2)仪器的选择选择仪器应根据反应物的体积、反应的条件及反应物(或生成物)的理化性质来决定。①选择反应瓶时应使反应物体积不超过反应瓶容积的2/3,一般为1/2。②回流反应一般采用圆底烧瓶和球形冷凝管:需要回流、搅拌并控制反应温度时可采用三颈瓶。③蒸馏操作需用蒸馏瓶:减压蒸馏采用减压蒸馏瓶。④被蒸馏物的沸点低于130℃用直形冷凝管,高于130℃用空气冷凝管。③选择温度计,一般根据反应温度选用最大刻度高于反应温度1020℃的温度计。水银温度计适用于测量-30~300℃的物质。温度低于-38℃时,常用内装有机液体的低温温度计(因水银会凝固)。(3)仪器的装配从安全、整洁、方便和可能出发,大致确定仪器装配在台面上的位置,并方便使用水源和电源。仪器装配通常是从下到上,从左到右(或从右到左)遂个装配。拆卸时按照与装配相反的顺序进行。仪器用铁夹牢固地固定在铁架上,夹玻璃仪器的铁夹不宜夹得太紧或太松,以用手能轻轻转动又不致于掉落为宜。铁夹的双钳应包有橡皮或贴有绒布等衬垫,以免铁夹直接接触玻璃仪器,将仪器夹破。冷凝管应夹在其中间部位。仪器装好后所有纵向仪器的轴心应与铁架的支撑杆平行,横向仪器与操作台前沿平行。仪器装配完毕后,必须仔细检查,每件仪器是否符合要求,装配是否无误、整齐稳妥,安全是否达到要求。要注意装置应与大气相通(除减压装置外),不能形成封闭体系,各接头处应吻合。(二)有机化学实验常用技术及装置1、加热有机反应在常温下进行较慢。为了增加有机反应的速度,往往需要在加热下进行反应。此外,有机化学实验的许多基本操作(如重结晶、蒸馏等)也需要加热。因此,加热是有机化学实验最常用的操作之一。掌握和正确选用加热方法,对完成有机化学实验是十分重要的。加热用的热源有煤气灯、酒精灯、电炉等。经常选用的加热方法有下列几种:(1)空气浴用空气作传热介质。将受热容器放在石棉网上用电炉加热,这是最简单的空气浴,对于沸点在80℃以上的液体均可采用。其缺点是受热不均匀,不能用于回流低沸点易燃的液体或者减压蒸馏。(2)水浴:用水作传热介质。将受热容器浸入盛水的水浴锅或大烧杯中(注意勿使容器触及水浴底部),适用于需要加热的温度在100℃以下的有机反应或后处理的加热。(3)油浴:用油作传热介质。所用的油有甘油、植物油和石蜡油。加热温度在100~11
11 的高低和化合物的性质选择合适的热源。一般 80℃以下可用水浴,高于 80℃用油浴。 如果化合物较稳定,沸点较高又不易燃烧的,可在石棉网上加热(空气浴),亦可用电 热套加热。 (2)仪器的选择 选择仪器应根据反应物的体积、反应的条件及反应物(或生成 物)的理化性质来决定。 ①选择反应瓶时应使反应物体积不超过反应瓶容积的 2/3,一般为 1/2。 ②回流反应一般采用圆底烧瓶和球形冷凝管;需要回流、搅拌并控制反应温度时 可采用三颈瓶。 ③蒸馏操作需用蒸馏瓶;减压蒸馏采用减压蒸馏瓶。 ④被蒸馏物的沸点低于 130℃用直形冷凝管,高于 130℃用空气冷凝管。 ⑤选择温度计,一般根据反应温度选用最大刻度高于反应温度10~20℃的温度计。 水银温度计适用于测量﹣30~300℃的物质。温度低于﹣38℃时,常用内装有机液体的 低温温度计(因水银会凝固)。 (3)仪器的装配 从安全、整洁、方便和可能出发,大致确定仪器装配在台面上 的位置,并方便使用水源和电源。 仪器装配通常是从下到上,从左到右(或从右到左)逐个装配。拆卸时按照与装 配相反的顺序进行。 仪器用铁夹牢固地固定在铁架上,夹玻璃仪器的铁夹不宜夹得太紧或太松,以用 手能轻轻转动又不致于掉落为宜。铁夹的双钳应包有橡皮或贴有绒布等衬垫,以免铁 夹直接接触玻璃仪器,将仪器夹破。冷凝管应夹在其中间部位。仪器装好后所有纵向 仪器的轴心应与铁架的支撑杆平行,横向仪器与操作台前沿平行。 仪器装配完毕后,必须仔细检查,每件仪器是否符合要求,装配是否无误、整齐、 稳妥,安全是否达到要求。要注意装置应与大气相通(除减压装置外),不能形成封闭 体系,各接头处应吻合。 (二)有机化学实验常用技术及装置 1、加热 有机反应在常温下进行较慢。为了增加有机反应的速度,往往需要在加热下进行 反应。此外,有机化学实验的许多基本操作(如重结晶、蒸馏等)也需要加热。因此, 加热是有机化学实验最常用的操作之一。掌握和正确选用加热方法,对完成有机化学 实验是十分重要的。 加热用的热源有煤气灯、酒精灯、电炉等。经常选用的加热方法有下列几种: (1)空气浴 用空气作传热介质。将受热容器放在石棉网上用电炉加热,这是最 简单的空气浴,对于沸点在 80℃以上的液体均可采用。其缺点是受热不均匀,不能用 于回流低沸点易燃的液体或者减压蒸馏。 (2)水浴 用水作传热介质。将受热容器浸入盛水的水浴锅或大烧杯中(注意勿 使容器触及水浴底部),适用于需要加热的温度在 100℃以下的有机反应或后处理的加 热。 (3)油浴 用油作传热介质。所用的油有甘油、植物油和石蜡油。加热温度在 100~
250℃之间。必须指出,用油浴加热时不能让水溅入油中,否则加热时会产生泡沫或爆溅。(4)砂浴用细砂子作传热介质。将细砂平铺在铁板上或盛在大蒸发血内,受热容器半埋在砂子中。砂浴的温度可达到数百摄氏度以上,适用于沸点达200℃以上的液体及固体升华的加热。缺点是砂子传热慢散热快,温度上升慢且不易控制。(5)盐浴用硝酸钾和硝酸钠的混合物作传热介质。将等量比的硝酸钾、硝酸钠装在铁锅内,适用于温度在220~680℃之间的加热。注意:盐浴时切勿溅入水。用过后的盐冷却后保存于干燥器中。出水进水图1-4红外灯加热装置电加热套1、冷凝器:2、温度计:3、红外灯图1-5电加热套加热装置4、液体;5、搅拌棒红外灯加热装置见图1-4。(7)电加热套电加热套由玻璃纤维包裹电热丝编织而成,外接调压变压器以调节加热温度。它的优点是安全、方便。缺点是一种规格加热套只适用于一定容积的烧瓶,故需配备几种尺寸的加热套,电加热套加热装置见图1-5。2.冷却在有机化学实验中,有时必须采用一定的冷却剂进行冷却操作,在一定的低温条件下进行反应、分离提纯等。例如:①某些反应要在特定的低温条件下进行,如重氮化反应一般在0~5℃进行:②沸点很低的有机物,冷却时可减少损失:③要加速结晶的析出。选择冷却剂是根据冷却温度和带走的热量来决定的。有机化学实验中常用的冷却剂如下:(1)水是常用的冷却剂。但随着季节的变化,其冷却效率变化较大。(2)冰-水混合物也是常用的冷却剂,可冷至0~5℃:要将冰弄得很碎,效果才好。12
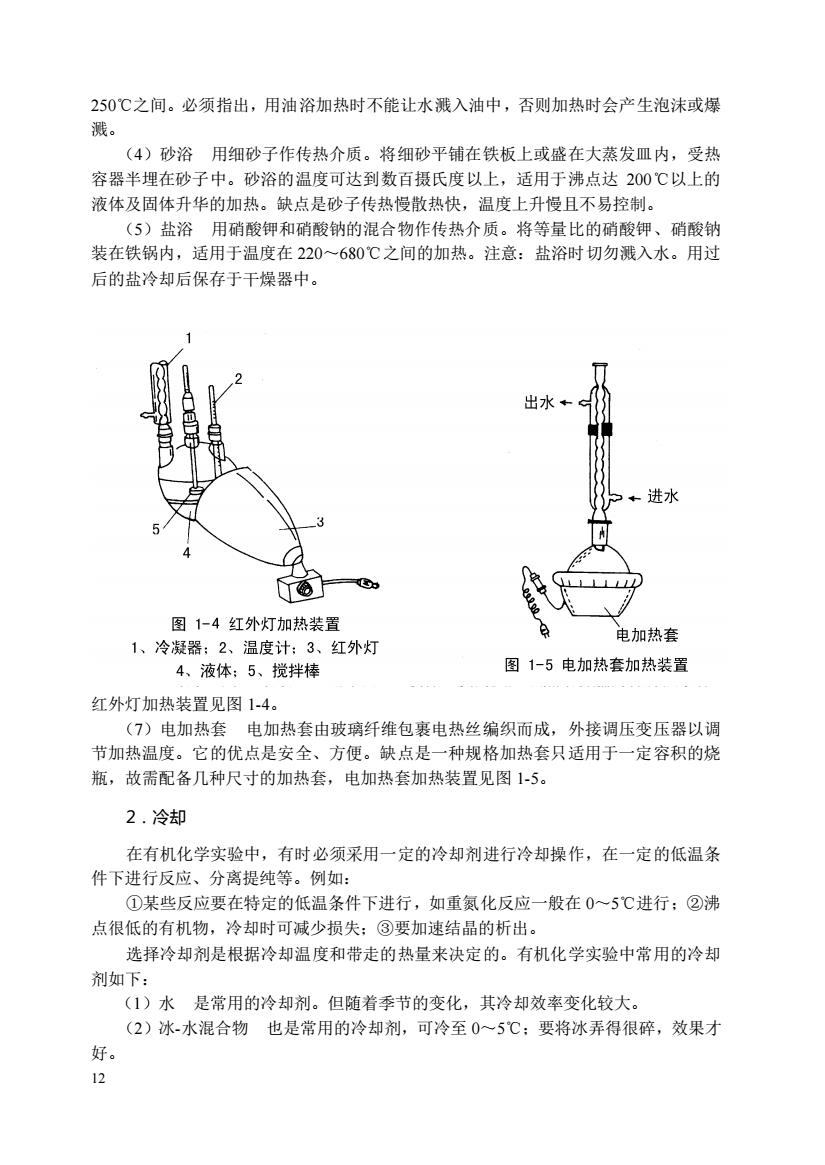
12 250℃之间。必须指出,用油浴加热时不能让水溅入油中,否则加热时会产生泡沫或爆 溅。 (4)砂浴 用细砂子作传热介质。将细砂平铺在铁板上或盛在大蒸发皿内,受热 容器半埋在砂子中。砂浴的温度可达到数百摄氏度以上,适用于沸点达 200℃以上的 液体及固体升华的加热。缺点是砂子传热慢散热快,温度上升慢且不易控制。 (5)盐浴 用硝酸钾和硝酸钠的混合物作传热介质。将等量比的硝酸钾、硝酸钠 装在铁锅内,适用于温度在 220~680℃之间的加热。注意:盐浴时切勿溅入水。用过 后的盐冷却后保存于干燥器中。 (6)红外灯 用红外灯加热适用于加热较低温度的反应或蒸馏易燃的低沸点液体, 红外灯加热装置见图 1-4。 (7)电加热套 电加热套由玻璃纤维包裹电热丝编织而成,外接调压变压器以调 节加热温度。它的优点是安全、方便。缺点是一种规格加热套只适用于一定容积的烧 瓶,故需配备几种尺寸的加热套,电加热套加热装置见图 1-5。 2.冷却 在有机化学实验中,有时必须采用一定的冷却剂进行冷却操作,在一定的低温条 件下进行反应、分离提纯等。例如: ①某些反应要在特定的低温条件下进行,如重氮化反应一般在 0~5℃进行;②沸 点很低的有机物,冷却时可减少损失;③要加速结晶的析出。 选择冷却剂是根据冷却温度和带走的热量来决定的。有机化学实验中常用的冷却 剂如下: (1)水 是常用的冷却剂。但随着季节的变化,其冷却效率变化较大。 (2)冰-水混合物 也是常用的冷却剂,可冷至 0~5℃;要将冰弄得很碎,效果才 好

(3)冰-盐混合物通常用冰-食盐混合物,即一份食盐与三份碎冰的混合物,可冷至-18~-5℃。食盐投入冰内时易结块,故最好边加边搅拌。其它盐类如CaC12?6H205份和碎冰4份,可冷至-50~-40℃。若无冰时,可用某些盐类溶于水吸热作为冷却剂使用。如:1份NH4CI和1份NaNO3溶于2份水中,可冷至-15~-10℃:3份NH4CI溶于10份水中,可冷至-15~-13℃11份Na2S2O3.5HO溶于10份水中,可冷至-8~11℃:3份NaNO3溶于5份水中,可冷至-13~13℃。(4)干冰(固体二氧化碳)可冷至-60℃以下。如将干冰加到甲醇或丙酮等有机溶剂中,可冷至-78℃,但加入时会猛烈起泡。(5)液氮可冷至-196℃。应当注意,温度若低于-38℃时,则不能使用水银温度计,因为低于-38.87℃时,水银就会凝固。对于较低的温度,常常使用内装有机液体(如甲苯,可达-90℃:正戊烷,可达-130℃)的低温温度计。为了便于读数,往往向液体内加入少许颜料。3、回流在有机化学实验中,有些反应和重结晶样品的溶解往往需要煮沸一段时间,为了不使反应物或溶剂的蒸气逸出,常在烧瓶口垂直装上冷凝管,冷却水自下而上流动,使蒸气在冷凝管中冷凝成液体又回到烧瓶中,这一过程称为加热回流,简称为回流。有机化学实验常用的回流装置如图1-6所示。图1-6(1)是可以防潮的回流装置。如不需要防潮,可以去掉冷凝管顶端的干燥管。图1-6(2)可吸收反应中生成的气体,适用于回流时有水溶性气体(如氯化氢、漠化氢、二氧化硫等)产生的实验。图1-6(3)可在回流的同时滴加液体。回流操作时应注意以下几点:(1)若使用磨口烧瓶和冷凝管,在接口处应涂上极薄一层的润滑脂(如凡士林),一引入水槽V(1)回流装置(2)回流装置(3)回流滴加装置13图1-6回流装置(普通玻璃仪器)
13 (3)冰-盐混合物 通常用冰-食盐混合物,即一份食盐与三份碎冰的混合物,可 冷至﹣18~﹣5℃。食盐投入冰内时易结块,故最好边加边搅拌。其它盐类如 CaC12 ﹒6H2O 5 份和碎冰 4 份,可冷至﹣50~﹣40℃。 若无冰时,可用某些盐类溶于水吸热作为冷却剂使用。如:1份 NH4Cl 和1 份NaNO3 溶于 2 份水中,可冷至﹣15~﹣10℃;3 份 NH4Cl 溶于 10 份水中,可冷至﹣15~﹣13℃; 11 份 Na2S2O3﹒5H2O 溶于 10 份水中,可冷至﹣8~11℃;3 份 NaNO3 溶于 5 份水中, 可冷至﹣13~13℃。 (4)干冰(固体二氧化碳) 可冷至﹣60℃以下。如将干冰加到甲醇或丙酮等有机 溶剂中,可冷至﹣78℃,但加入时会猛烈起泡。 (5)液氮 可冷至﹣196℃。 应当注意,温度若低于﹣38℃时,则不能使用水银温度计,因为低于﹣38.87℃时, 水银就会凝固。对于较低的温度,常常使用内装有机液体(如甲苯,可达﹣90℃;正 戊烷,可达﹣130℃)的低温温度计。为了便于读数,往往向液体内加入少许颜料。 3、回流 在有机化学实验中,有些反应和重结晶样品的溶解往往需要煮沸一段时间,为了 不使反应物或溶剂的蒸气逸出,常在烧瓶口垂直装上冷凝管,冷却水自下而上流动, 使蒸气在冷凝管中冷凝成液体又回到烧瓶中,这一过程称为加热回流,简称为回流。 有机化学实验常用的回流装置如图 1-6 所示。图 1-6(1)是可以防潮的回流装置。 如不需要防潮,可以去掉冷凝管顶端的干燥管。图 1-6(2)可吸收反应中生成的气体, 适用于回流时有水溶性气体(如氯化氢、溴化氢、二氧化硫等)产生的实验。图 1-6(3)可 在回流的同时滴加液体。 回流操作时应注意以下几点: (1)若使用磨口烧瓶和冷凝管,在接口处应涂上极薄一层的润滑脂(如凡士林)

以防止两个磨口玻璃接头因长时间加热而粘牢。当处理碱性溶液时,这是特别需要的但润滑脂不能涂得大多,否则,在加热时过多的润滑脂会进入烧瓶中,影响实验。(2)回流加热前,应在烧瓶中加入沸石。(3)回流的加热方式,应根据烧瓶内液体的特性和沸腾温度选用水浴、油浴、石棉网直接加热等方式。(4)回流的速度,应控制在液体蒸气浸润不超过回流冷凝管两个球为宜。(5)回流操作不管采用哪种装置,顶端都要与大气相通,否则会引起爆炸事故。14
14 以防止两个磨口玻璃接头因长时间加热而粘牢。当处理碱性溶液时,这是特别需要的。 但润滑脂不能涂得大多,否则,在加热时过多的润滑脂会进入烧瓶中,影响实验。 (2)回流加热前,应在烧瓶中加入沸石。 (3)回流的加热方式,应根据烧瓶内液体的特性和沸腾温度选用水浴、油浴、石 棉网直接加热等方式。 (4)回流的速度,应控制在液体蒸气浸润不超过回流冷凝管两个球为宜。 (5)回流操作不管采用哪种装置,顶端都要与大气相通,否则会引起爆炸事故

4、气体吸收在有机化学实验中,有些反应会生成有刺激性的气体。为了减少环境污染,必须采用气体吸收装置。对于具有水溶性的气体(如氯化氢、二氧化硫等)可用图1-7所示的气体吸收装置。水一其中图1-7(1)和图+气体气体1-7(2)可作少量气体的吸t收装置。图1-7(1)中的玻璃漏斗应微倾斜使漏斗口-气体0N引入水槽半在水中,一半在水面上。这样,既能防止气体逸出,又能防止水被倒吸至反应瓶中。若反应过程中有大量气体生成或气体逸出很快时,(1)(2)(3)可使用图1-7(3)的装置。图1-7气体吸收装置水自上端流入抽滤瓶中,在恒定的平面上溢出,粗的玻璃管恰好伸入水面,被水封住,以防止气体逸入大气中。对于酸性物质,有的需用稀碱液吸收。5、抽气过滤为了使结晶和母液迅速有效地分离和有利于干燥,通常用抽气过滤(或称减压过滤),简称抽滤。抽滤装置见图1-8所示。图1-8带安全瓶的抽滤装置图1-9金属水泵图1-10玻璃水泵抽气过滤的装置包括三部分:(1)漏斗常使用布氏漏斗,瓷质,底部有许多小孔,铺上圆形滤纸,其直径应略小于漏斗内径,以能紧贴于漏斗的底部,恰好盖住所有小孔为宜,布氏漏斗有大小不一的各种规格(以直径计)。选用时应和过滤物之量相称。即晶体必须把漏斗内滤纸15
15 4、气体吸收 在有机化学实验中,有些反应会生成有刺激性的气体。为了减少环境污染,必须 采用气体吸收装置。对于具有水溶性的气体(如氯化氢、二氧化硫等)可用图 1-7 所 示的气体吸收装置。 其中图 1-7(1)和图 1-7(2)可作少量气体的吸 收装置。图 1-7(1)中的玻 璃漏斗应微倾斜使漏斗口一 半在水中,一半在水面上。 这样,既能防止气体逸出, 又能防止水被倒吸至反应瓶 中。若反应过程中有大量气 体生成或气体逸出很快时, 可使用图 1-7(3)的装置。 水自上端流入抽滤瓶中,在 恒定的平面上溢出,粗的玻 璃管恰好伸入水面,被水封住,以防止气体逸入大气中。对于酸性物质,有的需用稀 碱液吸收。 5、抽气过滤 为了使结晶和母液迅速有效地分离和有利于干燥,通常用抽气过滤(或称减压过 滤),简称抽滤。抽滤装置见图 1-8 所示。 抽气过滤的装置包括三部分: (1)漏斗 常使用布氏漏斗,瓷质,底部有许多小孔,铺上圆形滤纸,其直径应 略小于漏斗内径,以能紧贴于漏斗的底部,恰好盖住所有小孔为宜,布氏漏斗有大小 不一的各种规格(以直径计)。选用时应和过滤物之量相称。即晶体必须把漏斗内滤纸