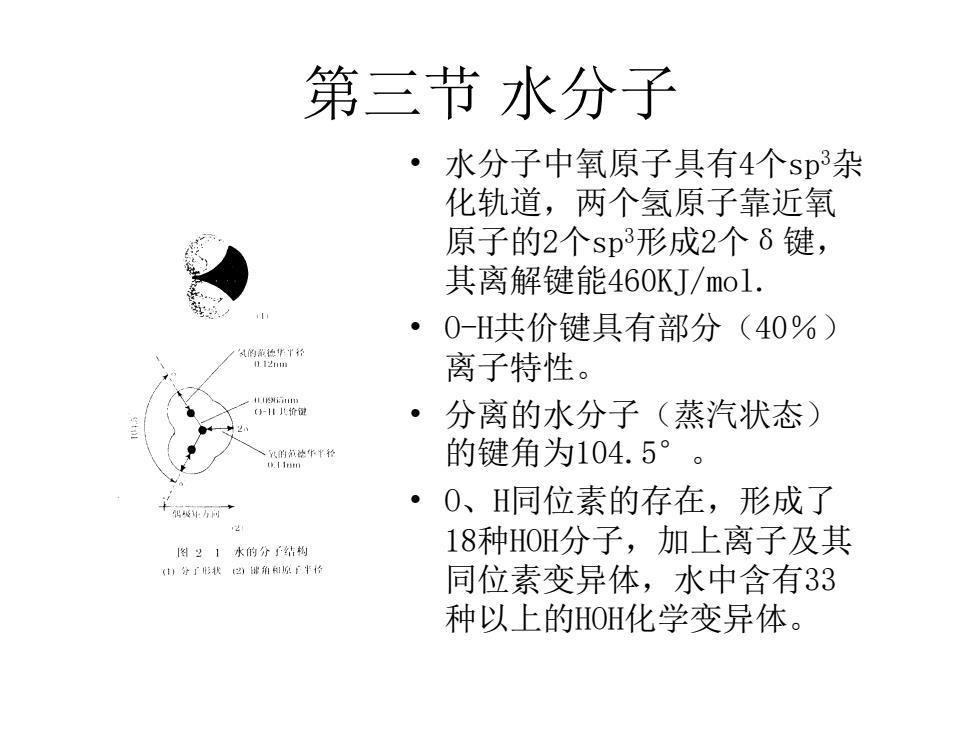
第三节 水分子 • 水分子中氧原子具有4个sp3杂 化轨道,两个氢原子靠近氧 原子的2个sp3形成2个δ键, 其离解键能460KJ/mol. • O-H共价键具有部分(40%) 离子特性。 • 分离的水分子(蒸汽状态) 的键角为104.5° 。 • O、H同位素的存在,形成了 18种HOH分子,加上离子及其 同位素变异体,水中含有33 种以上的HOH化学变异体
第三节 水分子 • 水分子中氧原子具有4个sp3杂 化轨道,两个氢原子靠近氧 原子的2个sp3形成2个δ键, 其离解键能460KJ/mol. • O-H共价键具有部分(40%) 离子特性。 • 分离的水分子(蒸汽状态) 的键角为104.5° 。 • O、H同位素的存在,形成了 18种HOH分子,加上离子及其 同位素变异体,水中含有33 种以上的HOH化学变异体

第四节 水分子的缔合 • 1 HOH分子呈V字形状,O-H具有极性, 造成不对称的电荷分布,纯水在蒸汽状态 时具有1.84D偶极矩。 • 2 水分子极性产生分子间吸引力,使水分子 具有强烈缔合的倾向。 • 3 水分子间吸引力不完全是由于它的大偶极 矩,偶极矩并不能指出水分子中电荷暴露 的程度和水分子的几何形状,而这二者对 水分子的缔合程度具有重要影响
第四节 水分子的缔合 • 1 HOH分子呈V字形状,O-H具有极性, 造成不对称的电荷分布,纯水在蒸汽状态 时具有1.84D偶极矩。 • 2 水分子极性产生分子间吸引力,使水分子 具有强烈缔合的倾向。 • 3 水分子间吸引力不完全是由于它的大偶极 矩,偶极矩并不能指出水分子中电荷暴露 的程度和水分子的几何形状,而这二者对 水分子的缔合程度具有重要影响

• 4 水分子参与形成三维空间多重氢键的能力 可以解释水分子间的大吸引力。 共价键平均键能约335KJ/mol,氢键离解 能约13~25KJ/mol。 每个水分子具有数目相等的氢键供体和受 体部位,可以形成三维氢键。 每个水分子最多能与其它4个水分子形成氢 键,形成四面体结构。 与同样能形成氢键的分子(如NH3、HF) 比较,水分子间的吸引力高很多
• 4 水分子参与形成三维空间多重氢键的能力 可以解释水分子间的大吸引力。 共价键平均键能约335KJ/mol,氢键离解 能约13~25KJ/mol。 每个水分子具有数目相等的氢键供体和受 体部位,可以形成三维氢键。 每个水分子最多能与其它4个水分子形成氢 键,形成四面体结构。 与同样能形成氢键的分子(如NH3、HF) 比较,水分子间的吸引力高很多

• 5 水形成三维氢键的能 力可解释水高相转变 热、高表面张力等性 质。 • 6 水的介电常数也受氢 键影响:通过氢键结 合的水分子簇产生多 分子偶极,有效地提 高了水的介电常数。 • 水合氢离子带正电, 比非离子化水更大氢 键给与能力,羟基, 更大接受能力
• 5 水形成三维氢键的能 力可解释水高相转变 热、高表面张力等性 质。 • 6 水的介电常数也受氢 键影响:通过氢键结 合的水分子簇产生多 分子偶极,有效地提 高了水的介电常数。 • 水合氢离子带正电, 比非离子化水更大氢 键给与能力,羟基, 更大接受能力
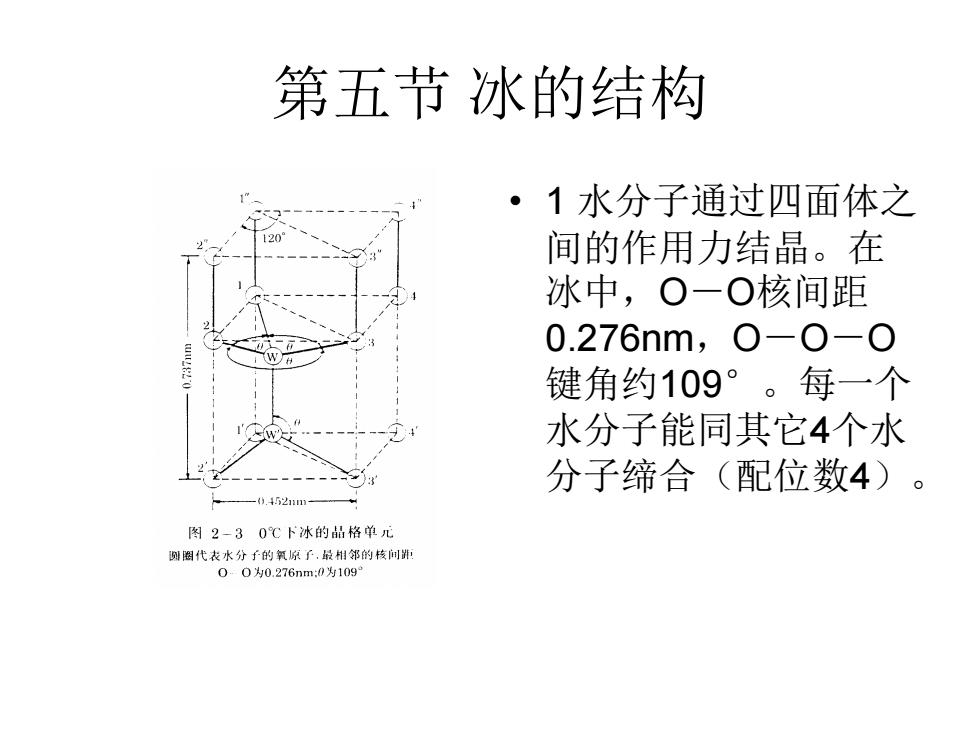
第五节 冰的结构 • 1 水分子通过四面体之 间的作用力结晶。在 冰中,O-O核间距 0.276nm,O-O-O 键角约109°。每一个 水分子能同其它4个水 分子缔合(配位数4)
第五节 冰的结构 • 1 水分子通过四面体之 间的作用力结晶。在 冰中,O-O核间距 0.276nm,O-O-O 键角约109°。每一个 水分子能同其它4个水 分子缔合(配位数4)