法(毕业要求3创新设计/开发解决方案的能力): 5.在实验中逐步培养正确、细致、整洁地进行科学实验的良好习惯(毕业要求3创新设计 /开发解决方案的能力)。 四、课程的实验要求与内容 序号 项目 对应课 内容提要 学时 性质 要求 程目标 二草酸根合铜 1.进一步掌握溶解、沉淀、吸滤、蒸发、 (Ⅱ)酸钾的制备 浓缩等基本操作: 1、2、3 1 与组成分析 2. 制备二草酸根合铜(Ⅱ)酸钾晶体; 4 综合 必做 3. 4、5 确定二草酸根合铜(Ⅱ)酸钾的组成。 过氧化钙的制备 1. 掌握制备过氧化钙的原理及方法: 及含量的分析 2. 掌握过氧化钙含量的分析方法: 1、2、3、 2 4 3. 巩固无机制备及化学分析的基本操作。 综合 必做 4、5 三草酸根合铜酸 1.掌握三草酸根合铁(II)酸钾的制备 钾的制备、性质、 方法: 组成 2.熟悉化学分析、热分析、电导率测定 3 等方法在化合物组成分析中的应用: 4 综合 必做 1、2、3、 4、5 3.了解三草酸根合铁(III)酸钾的光化 学性质。 三氯化六氨合钴 1.掌握三氯化六氨合钴(III)的合成及 的制备、性质、组其组成测定的操作方法: 成 2.练习三种滴定方法(酸碱滴定,氧化 还原滴定,沉淀滴定)的操作; 3.学习电导测定原理与方法以及DDS一 4 综合 必做 1、2、3、 4、5 11A电导率仪的使用: 4.加深理解配合物的形成对三价钴稳定 性的影响。 硫酸铜的制备,提1.了解硫酸铜的制备原理和用重结晶法 纯和质量鉴定 提纯物质的基本原理:。 2.掌握加热、溶解、蒸发浓缩、结晶、 1、2、3、 5 综合 必做 常压过滤、减压过滤等基本操作技术: 4、5 3.掌握天平、电炉和研钵的操作。 无水氯化亚锡的 1.了解制备无水金属卤化物的一般方法: 1、2、3 6 制备,提纯和质量2.掌握无机制备的几种基本操作。 综合 必做 鉴定 4、5 纳米二氧化硅胶 1.了解溶胶凝胶法制备纳米颗粒的方法。 体的制备 2.掌握无机制备的几种基本操作。 综合 1、2、3、 4 3.巩固胶体化学的基本知识。 必做 4、5 14
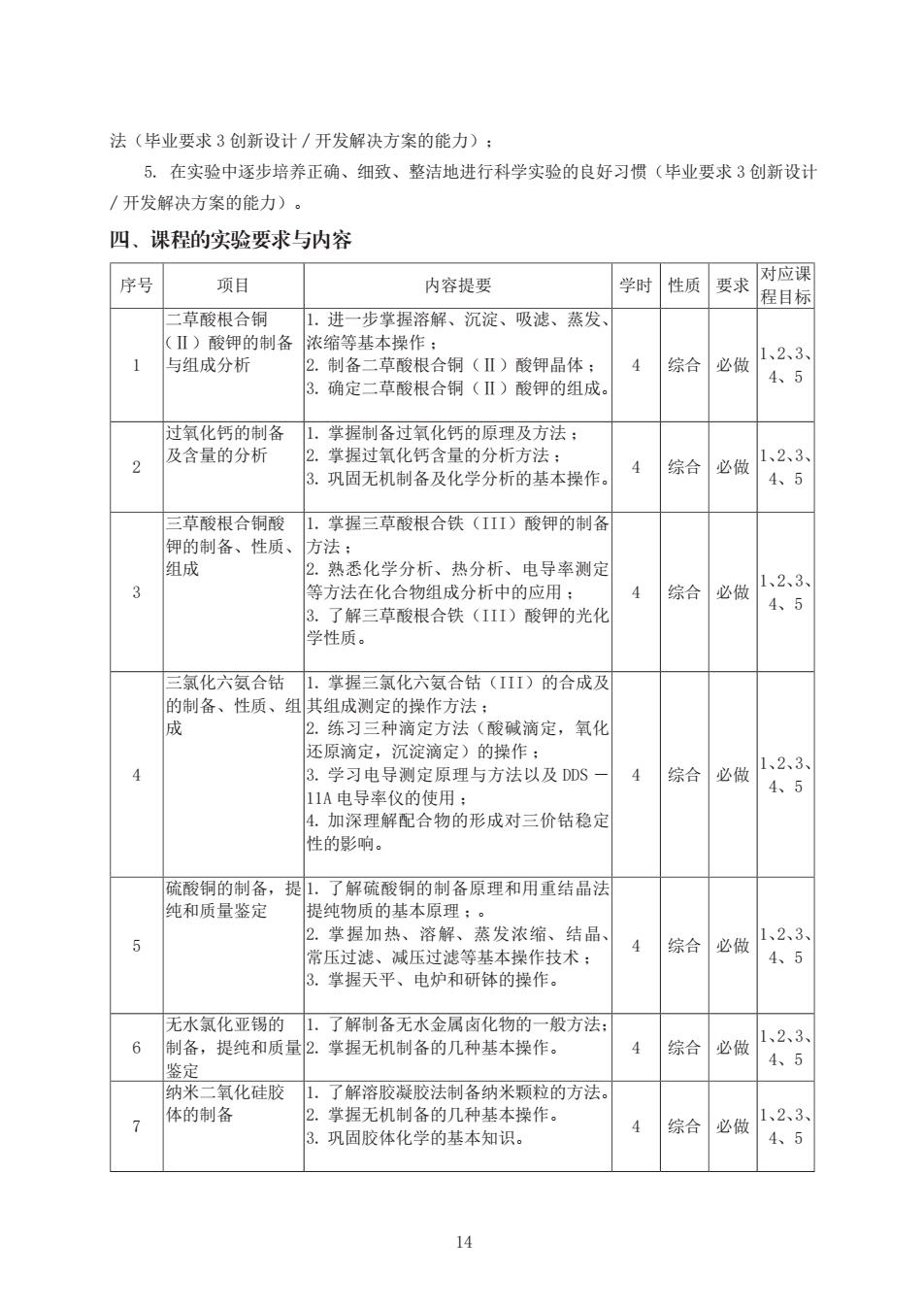
14 法(毕业要求 3 创新设计 / 开发解决方案的能力); 5. 在实验中逐步培养正确、细致、整洁地进行科学实验的良好习惯(毕业要求 3 创新设计 / 开发解决方案的能力)。 四、课程的实验要求与内容 序号 项目 内容提要 学时 性质 要求 对应课 程目标 1 二草酸根合铜 (Ⅱ)酸钾的制备 与组成分析 1. 进一步掌握溶解、沉淀、吸滤、蒸发、 浓缩等基本操作 ; 2. 制备二草酸根合铜(Ⅱ)酸钾晶体 ; 3. 确定二草酸根合铜(Ⅱ)酸钾的组成。 4 综合 必做 1、2、3、 4、5 2 过氧化钙的制备 及含量的分析 1. 掌握制备过氧化钙的原理及方法 ; 2. 掌握过氧化钙含量的分析方法 ; 3. 巩固无机制备及化学分析的基本操作。 4 综合 必做 1、2、3、 4、5 3 三草酸根合铜酸 钾的制备、性质、 组成 1. 掌握三草酸根合铁(III)酸钾的制备 方法 ; 2. 熟悉化学分析、热分析、电导率测定 等方法在化合物组成分析中的应用 ; 3. 了解三草酸根合铁(III)酸钾的光化 学性质。 4 综合 必做 1、2、3、 4、5 4 三氯化六氨合钴 的制备、性质、组 成 1. 掌握三氯化六氨合钴(III)的合成及 其组成测定的操作方法 ; 2. 练习三种滴定方法(酸碱滴定,氧化 还原滴定,沉淀滴定)的操作 ; 3. 学习电导测定原理与方法以及 DDS - 11A 电导率仪的使用 ; 4. 加深理解配合物的形成对三价钴稳定 性的影响。 4 综合 必做 1、2、3、 4、5 5 硫酸铜的制备,提 纯和质量鉴定 1. 了解硫酸铜的制备原理和用重结晶法 提纯物质的基本原理 ;。 2. 掌握加热、溶解、蒸发浓缩、结晶、 常压过滤、减压过滤等基本操作技术 ; 3. 掌握天平、电炉和研钵的操作。 4 综合 必做 1、2、3、 4、5 6 无水氯化亚锡的 制备,提纯和质量 鉴定 1. 了解制备无水金属卤化物的一般方法; 2. 掌握无机制备的几种基本操作。 4 综合 必做 1、2、3、 4、5 7 纳米二氧化硅胶 体的制备 1. 了解溶胶凝胶法制备纳米颗粒的方法。 2. 掌握无机制备的几种基本操作。 3. 巩固胶体化学的基本知识。 4 综合 必做 1、2、3、 4、5

羟基磷灰石的制 1.了解羟基磷灰石的制备方法。 备及其对水溶液 2. 掌握无机制备的几种基本操作。 1、2、3 8 中铅离子的吸附 3.了解羟基磷灰石对水溶液中铅离子的 综合 必做 4、5 吸附作用。 五、参考资料 [1]华东化工学院无机化学教研室编,无机化学实验(第三版),北京:高等教育出版社, 2002 [2]大连理工大学,无机化学实验,北京:高等教育出版社,2016 [3]包新华等,无机化学实验,北京:科学出版社,2016 [4]吉林大学,无机化学实验,北京:高等教育出版社,2006 六、考核与成绩评定 1、实验32学时,以学生操作、综合和验证为主,教师讲解、提问、引导、答疑为辅,实 验做到配合课堂教学,重视基本技能的训练,加深学生对无机化学基本概念、基本理论和基本 知识的理解,强化理论与实际的联系。 2、通过实验使学生学会准确细致地观察、记录实验现象和做出正确的结论,并不断地提高 学生的实验技能技巧和分析问题解决问题的能力。 3、通过多个环节的训练和考核,促进学习目标的达成: (1)预习成绩 (2)平时成绩 (3)实验报告 4、成绩评定 预习成绩 平时成绩 实验报告 20% 30% 50% 七、课程日标达成评价 课程目标的实际达成效果计算方式如下,达成值越高,教学效果越好。 课程目标达成度= 学生相应环节得分平均值 该环节的满分 毕业要求指标达成度=Σ课程目标达成度×课程目标在毕业要求指标点的权重 制定人:邹翔宇 审核人:杨铭 15
15 8 羟基磷灰石的制 备及其对水溶液 中铅离子的吸附 1. 了解羟基磷灰石的制备方法。 2. 掌握无机制备的几种基本操作。 3. 了解羟基磷灰石对水溶液中铅离子的 吸附作用。 4 综合 必做 1、2、3、 4、5 五、参考资料 [1] 华东化工学院无机化学教研室编,无机化学实验(第三版),北京:高等教育出版社, 2002 [2] 大连理工大学,无机化学实验,北京:高等教育出版社,2016 [3] 包新华等,无机化学实验,北京:科学出版社,2016 [4] 吉林大学,无机化学实验,北京:高等教育出版社,2006 六、考核与成绩评定 1、实验 32 学时,以学生操作、综合和验证为主,教师讲解、提问、引导、答疑为辅,实 验做到配合课堂教学,重视基本技能的训练,加深学生对无机化学基本概念、基本理论和基本 知识的理解,强化理论与实际的联系。 2、通过实验使学生学会准确细致地观察、记录实验现象和做出正确的结论,并不断地提高 学生的实验技能技巧和分析问题解决问题的能力。 3、通过多个环节的训练和考核,促进学习目标的达成: (1)预习成绩 (2)平时成绩 (3)实验报告 4、成绩评定 预习成绩 平时成绩 实验报告 20% 30% 50% 七、课程目标达成评价 课程目标的实际达成效果计算方式如下,达成值越高,教学效果越好。 课程目标达成度= 学生相应环节得分平均值 毕业要求指标达成度 = ∑课程目标达成度 × 课程目标在毕业要求指标点的权重 制定人:邹翔宇 审核人:杨 铭 该环节的满分

分析化学课程教学大纲 一、 课程基本信息 课程编码 070721105 开课单位 化学与环境工程学院 分析化学 课程名称 Analytical Chemistry 课程学时 32 课程学分 2 课程类别 学科基础课 课程性质 必修 开课学期 3 课内实验学时 0 适用专业 应用化学 选用教材 《分析化学》 先修课程 无机化学 考核方式 闭卷考试 制定人 耿爱芳 制定时间 2018.07 二、课程性质及目标 分析化学是研究物质的化学组成和结构的分析方法及有关理论的一门学科,它是化学学科 的一个重要分支。分析化学是获取物质化学组成、含量、结构及相关信息的科学。分析化学是 应用化学专业学生的主要基础课之一,它的理论和方法不仅是分析科学的基础,也是从事化学 教育、生命、地质、环境等学科的工作基础。 本课程拟达到的课程目标:分析化学课程的特点是基本理论与实践紧密结合,通过严格的 实验训练,培养认真的科学态度及独立进行精密科学实验的技巧,提高分析问题和处理问题的 能力。分析化学课程在教授学生基本分析化学原理和方法的同时,使学生建立起严格的量的概 念,培养学生从事理论研究和实际分析工作的严谨科学作风和能力。 三、课程目标对毕业要求的支撑 1.掌握常量组分定量分析的基本知识、基本理论和基本分析方法(毕业要求1获取和应用 化学知识的能力): 2.掌握分析测定中误差的来源、误差的表征以及初步学会实验数据的统计处理方法(毕业 要求2问题分析的能力): 3.了解定量分析中常用的分离方法的原理及其应用(毕业要求2问题分析的能力): 4.熟悉分光光度法的原理及其应用(毕业要求3创新设计/开发解决方案的能力): 5.本课程教学过程中不仅要讲清定量分析化学的基本概念和基本理论,而且要让学生懂得 建立这些概念和理论的化学方法和思维方法,加强素质教育,注重能力培养,提倡创新精神(毕 业要求5使用现代工具的能力、6分析与评价应用化学与社会关系的能力、7理解与评价环境和 可持续发展的能力)。 16
16 分析化学课程教学大纲 一、课程基本信息 课程编码 070721105 开课单位 化学与环境工程学院 课程名称 分析化学 Analytical Chemistry 课程学时 32 课程学分 2 课程类别 学科基础课 课程性质 必修 开课学期 3 课内实验学时 0 适用专业 应用化学 选用教材 《分析化学》 先修课程 无机化学 考核方式 闭卷考试 制定人 耿爱芳 制定时间 2018.07 二、课程性质及目标 分析化学是研究物质的化学组成和结构的分析方法及有关理论的一门学科,它是化学学科 的一个重要分支。分析化学是获取物质化学组成、含量、结构及相关信息的科学。分析化学是 应用化学专业学生的主要基础课之一,它的理论和方法不仅是分析科学的基础,也是从事化学 教育、生命、地质、环境等学科的工作基础。 本课程拟达到的课程目标:分析化学课程的特点是基本理论与实践紧密结合,通过严格的 实验训练,培养认真的科学态度及独立进行精密科学实验的技巧,提高分析问题和处理问题的 能力。分析化学课程在教授学生基本分析化学原理和方法的同时,使学生建立起严格的量的概 念,培养学生从事理论研究和实际分析工作的严谨科学作风和能力。 三、课程目标对毕业要求的支撑 1. 掌握常量组分定量分析的基本知识、基本理论和基本分析方法(毕业要求 1 获取和应用 化学知识的能力); 2. 掌握分析测定中误差的来源、误差的表征以及初步学会实验数据的统计处理方法(毕业 要求 2 问题分析的能力); 3. 了解定量分析中常用的分离方法的原理及其应用(毕业要求 2 问题分析的能力); 4. 熟悉分光光度法的原理及其应用(毕业要求 3 创新设计 / 开发解决方案的能力); 5. 本课程教学过程中不仅要讲清定量分析化学的基本概念和基本理论,而且要让学生懂得 建立这些概念和理论的化学方法和思维方法,加强素质教育,注重能力培养,提倡创新精神(毕 业要求 5 使用现代工具的能力、6 分析与评价应用化学与社会关系的能力、7 理解与评价环境和 可持续发展的能力)
四、课程的教学内容、基本要求与学时分配 序号 教学内容 学时 教学对应课 基本要求 方式 程目标 、 绪论 1. 了解分析化学的发展现状和展望: 1.1分析化学的任务和作用 2. 掌握分析化学的定义、分类、 1.2分析化学的分类 任务和作用。 授课 1、5 1.3分析化学的进展简况 误差及分析数据的统计处 1. 了解误差的传递及有效数字的 理 意义: 2.1定量分析中的误差 2. 理解准确度和精密度的意义与 2.2分析结果的数据处理 关系: 2.3误差的传递 3.掌握误差、偏差及其表示方法 4 2.4有效数字及其运算规则 授课 2 随机误差的正态分布、有限测定 2.5标准曲线的回归分析 数据的统计处理、分析数据的处 理原则: 4.掌握有效数字运算规则。 三、滴定分析 1.了解滴定分析法的特点和类别: 3.1滴定分析概述 2 理解滴定分析对化学反应的要 3.2滴定分析法的分类与滴定 求: 反应的条件 3.掌握标准溶液浓度的表示方法 授课 1 3.3标准溶液 及标准溶液配制和浓度的标定、 3.4标准溶液浓度表示法 基准物质必备的条件: 3.5滴定分析结果的计算 4.掌握滴定分析结果的计算。 四、酸碱滴定法 掌握各种溶液H值的计算方 4.1酸碱平衡的理论基础 法; 4.2分布曲线 2. 掌握酸碱指示剂的作用原理、 4.3酸碱溶液pH的计算 变色范围及其应用: 4.4酸碱滴定终点的指示方法 3. 了解各种类型的酸碱滴定过程 4 4.5一元酸碱的滴定 中pH值的变化规律 授课 1 4.6混合碱的滴定 4.掌握酸碱标准溶液的配制与标 4.7酸碱滴定法应用示例 定 4.8酸碱标准溶液配制与标定 5.掌握酸碱滴定法结果计算 4.9酸碱滴定法结果计算示例 五、配位滴定法 掌握酸效应和配位效应对配位 5.1EDTA与金属离子的配合物 平衡的影响K'g的计算方法: 及其稳定性 2.掌握金属离子能被准确滴定的 5.2外界条件对EDTA与金属 依据: 5 离子配合物稳定性的影响 3.了解选择金属指示剂的依据: 授课 1 5.3金属指示剂确定滴定终点 4. 掌握控制溶液酸度进行选择性 的方法 滴定的方法。 5.4混合离子的分别滴定 5.5配位滴定的方式和应用 17
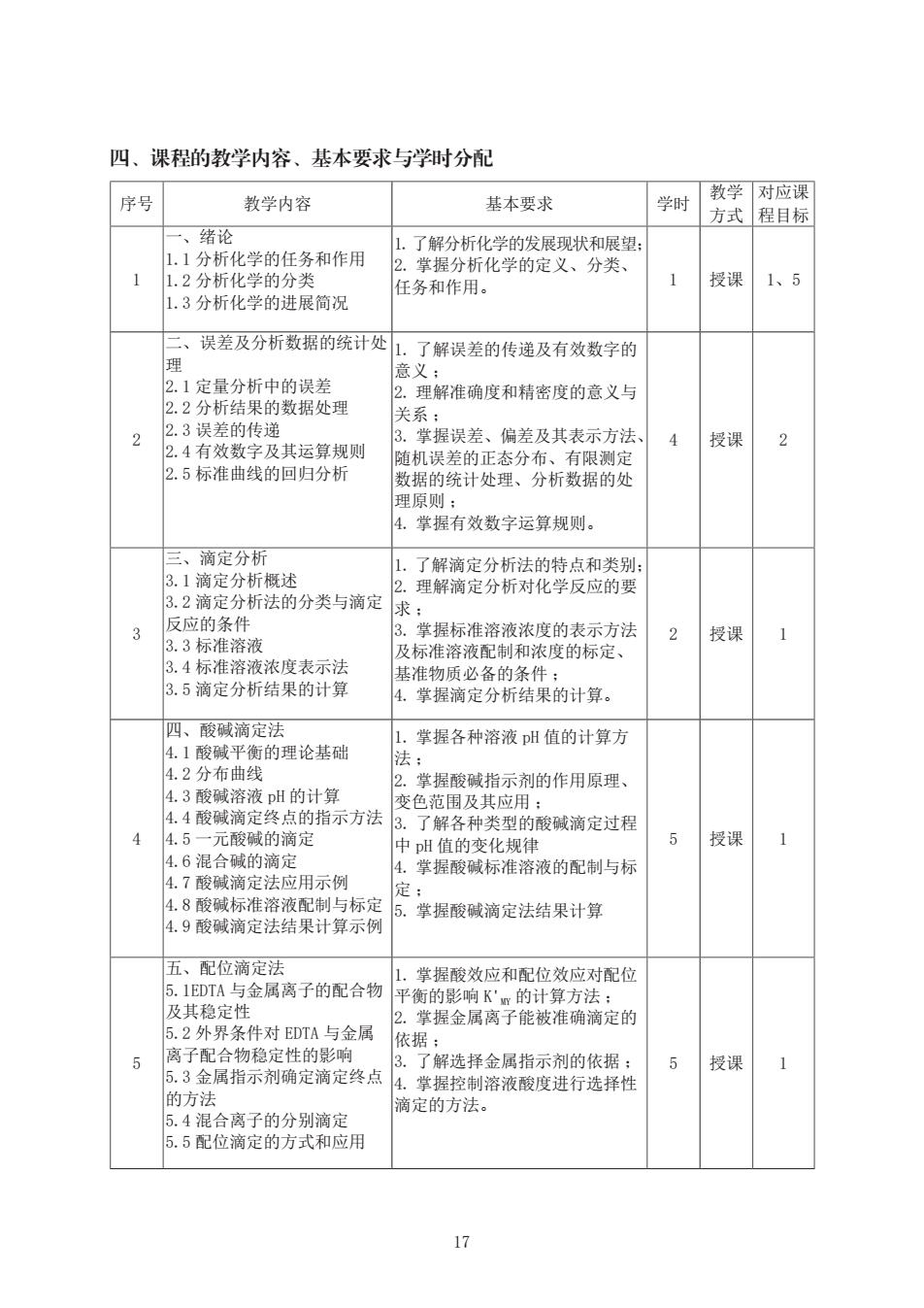
17 四、课程的教学内容、基本要求与学时分配 序号 教学内容 基本要求 学时 教学 方式 对应课 程目标 1 一、绪论 1.1 分析化学的任务和作用 1.2 分析化学的分类 1.3 分析化学的进展简况 1.了解分析化学的发展现状和展望; 2. 掌握分析化学的定义、分类、 任务和作用。 1 授课 1、5 2 二、误差及分析数据的统计处 理 2.1 定量分析中的误差 2.2 分析结果的数据处理 2.3 误差的传递 2.4 有效数字及其运算规则 2.5 标准曲线的回归分析 1. 了解误差的传递及有效数字的 意义 ; 2. 理解准确度和精密度的意义与 关系 ; 3. 掌握误差、偏差及其表示方法、 随机误差的正态分布、有限测定 数据的统计处理、分析数据的处 理原则 ; 4. 掌握有效数字运算规则。 4 授课 2 3 三、滴定分析 3.1 滴定分析概述 3.2 滴定分析法的分类与滴定 反应的条件 3.3 标准溶液 3.4 标准溶液浓度表示法 3.5 滴定分析结果的计算 1. 了解滴定分析法的特点和类别; 2. 理解滴定分析对化学反应的要 求 ; 3. 掌握标准溶液浓度的表示方法 及标准溶液配制和浓度的标定、 基准物质必备的条件 ; 4. 掌握滴定分析结果的计算。 2 授课 1 4 四、酸碱滴定法 4.1 酸碱平衡的理论基础 4.2 分布曲线 4.3 酸碱溶液 pH 的计算 4.4 酸碱滴定终点的指示方法 4.5 一元酸碱的滴定 4.6 混合碱的滴定 4.7 酸碱滴定法应用示例 4.8 酸碱标准溶液配制与标定 4.9 酸碱滴定法结果计算示例 1. 掌握各种溶液 pH 值的计算方 法 ; 2. 掌握酸碱指示剂的作用原理、 变色范围及其应用 ; 3. 了解各种类型的酸碱滴定过程 中 pH 值的变化规律 4. 掌握酸碱标准溶液的配制与标 定 ; 5. 掌握酸碱滴定法结果计算 5 授课 1 5 五、配位滴定法 5.1EDTA 与金属离子的配合物 及其稳定性 5.2 外界条件对 EDTA 与金属 离子配合物稳定性的影响 5.3 金属指示剂确定滴定终点 的方法 5.4 混合离子的分别滴定 5.5 配位滴定的方式和应用 1. 掌握酸效应和配位效应对配位 平衡的影响 K'MY 的计算方法 ; 2. 掌握金属离子能被准确滴定的 依据 ; 3. 了解选择金属指示剂的依据 ; 4. 掌握控制溶液酸度进行选择性 滴定的方法。 5 授课 1
六、氧化还原滴定法 1. 理解能斯特公式与电极电位: 6.1氧化还原反应平衡 2. 掌握计量点时电极电位变化的 6.2氧化还原反应进行的程度 计算方法: 6.3氧化还原反应的速率与影 3.掌握常用的氧化还原滴定方法 响因素 KMnO,、 KCr0,、碘量法: 6 6.4氧化还原指示剂 4.掌握氧化还原滴定结果的计算 授课 1 6.5高锰酸钾法 6.6重铬酸钾法 6.7碘量法 6.8氧化还原滴定结果计算 七、重量分析和沉淀滴定法 1. 了解重量分析对沉淀的要求、 7.1重量分析概述 沉淀形成过程: 7.2重量分析对沉淀的要求 2. 理解影响沉淀溶解度的因素: 7.3沉淀完全的程度与影响沉 3 了解影响沉淀纯度的因素及提 淀溶解度的因素 高沉淀纯度的措施: 7 7.4影响沉淀纯度的因素 4. 掌握晶形沉淀与非晶形沉淀的 4 授课 1 7.5沉淀的形成与沉淀的条件 形成条件: 7.6重量分析的计算 5. 了解沉淀滴定法的原理。 7.7沉淀滴定法概述 7.8银量法滴定终点的确定 八、吸光光度法 了解摩尔吸光系数的意义和计 8.1吸光光度法基本原理 算: 8.2光度计及其基本部件 2.了解选择显色剂的原理及影响 8.3显色反应及显色条件的选 显色反应的因素: 8 择 3.理解朗伯一比尔定律的数学表 8.4吸光度测量条件的选择 达式及意义: 3 授课 4 8.5吸光光度法的应用 4.初步掌握分光光度法的基本原 理应用: 5. 熟悉如何正确选择测量条件 九、分析化学中的分离与富集 了解沉淀分离法、萃取分离法、 方法 离子交换分离法 9 9.1沉淀分离法 9.2溶剂萃取分离法 3 授课 3 9.3离子交换分离法 十、定量分析的一般步骤 1.了解试样全分析的基本原理和 10.1试样的采取和制备 般步骤 10.2试样的分解 2.了解分析结果准确度的保证与 10 10.3测定方法的选择 评价方法 授课 1、5 10.4分析结果准确度的保证 与评价 合计 32 18
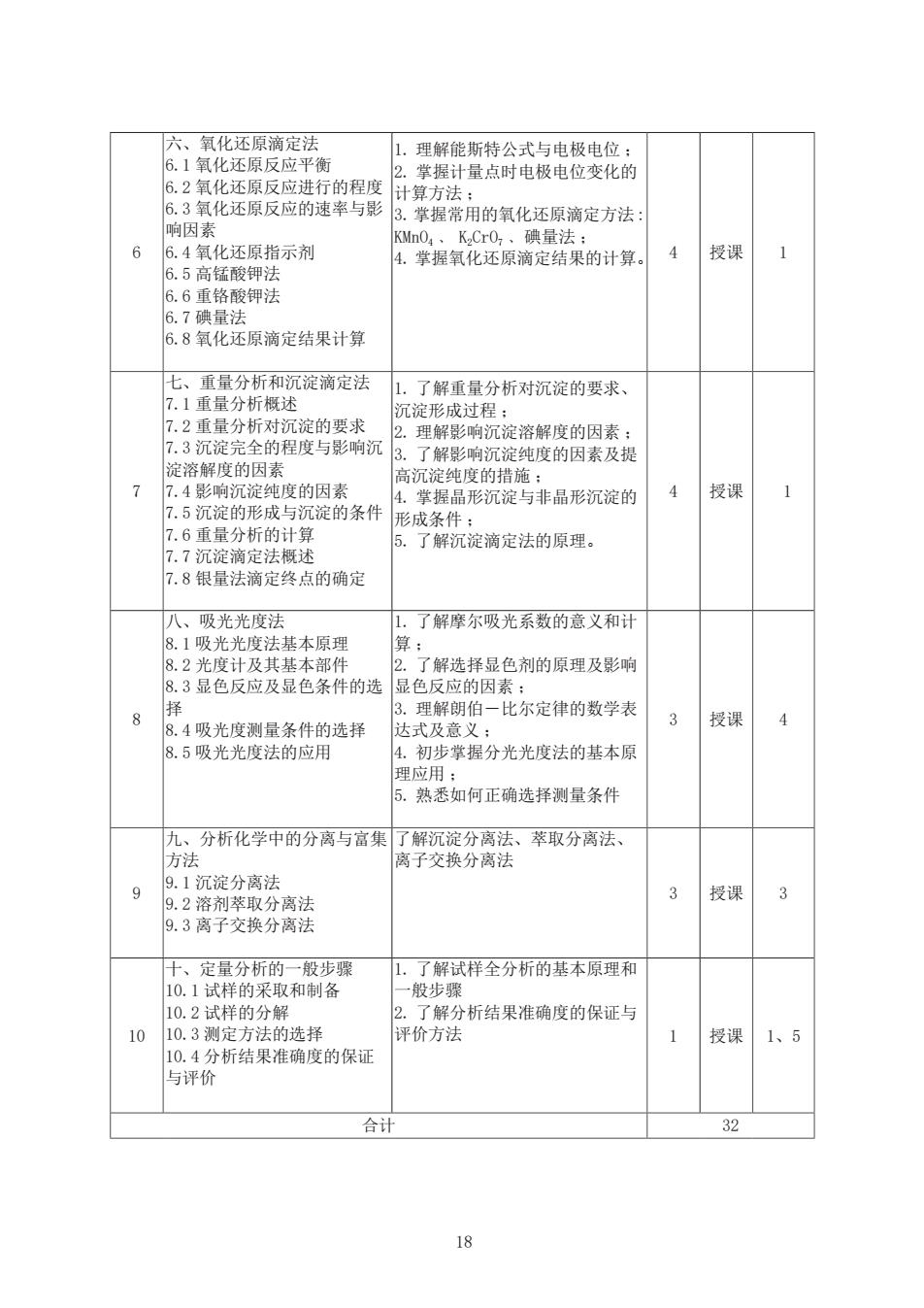
18 6 六、氧化还原滴定法 6.1 氧化还原反应平衡 6.2 氧化还原反应进行的程度 6.3 氧化还原反应的速率与影 响因素 6.4 氧化还原指示剂 6.5 高锰酸钾法 6.6 重铬酸钾法 6.7 碘量法 6.8 氧化还原滴定结果计算 1. 理解能斯特公式与电极电位 ; 2. 掌握计量点时电极电位变化的 计算方法 ; 3.掌握常用的氧化还原滴定方法 : KMnO4 ﹑ K2CrO7 ﹑碘量法 ; 4. 掌握氧化还原滴定结果的计算。 4 授课 1 7 七、重量分析和沉淀滴定法 7.1 重量分析概述 7.2 重量分析对沉淀的要求 7.3 沉淀完全的程度与影响沉 淀溶解度的因素 7.4 影响沉淀纯度的因素 7.5 沉淀的形成与沉淀的条件 7.6 重量分析的计算 7.7 沉淀滴定法概述 7.8 银量法滴定终点的确定 1. 了解重量分析对沉淀的要求、 沉淀形成过程 ; 2. 理解影响沉淀溶解度的因素 ; 3. 了解影响沉淀纯度的因素及提 高沉淀纯度的措施 ; 4. 掌握晶形沉淀与非晶形沉淀的 形成条件 ; 5. 了解沉淀滴定法的原理。 4 授课 1 8 八、吸光光度法 8.1 吸光光度法基本原理 8.2 光度计及其基本部件 8.3 显色反应及显色条件的选 择 8.4 吸光度测量条件的选择 8.5 吸光光度法的应用 1. 了解摩尔吸光系数的意义和计 算 ; 2. 了解选择显色剂的原理及影响 显色反应的因素 ; 3. 理解朗伯-比尔定律的数学表 达式及意义 ; 4. 初步掌握分光光度法的基本原 理应用 ; 5. 熟悉如何正确选择测量条件 3 授课 4 9 九、分析化学中的分离与富集 方法 9.1 沉淀分离法 9.2 溶剂萃取分离法 9.3 离子交换分离法 了解沉淀分离法、萃取分离法、 离子交换分离法 3 授课 3 10 十、定量分析的一般步骤 10.1 试样的采取和制备 10.2 试样的分解 10.3 测定方法的选择 10.4 分析结果准确度的保证 与评价 1. 了解试样全分析的基本原理和 一般步骤 2. 了解分析结果准确度的保证与 评价方法 1 授课 1、5 合计 32