分子轨道法与HMO 2.水分子的分子轨道法定性处理 2al gal S-Pz 2al 3al gal S-D 3al 4a1 gal S-p- 4al >11
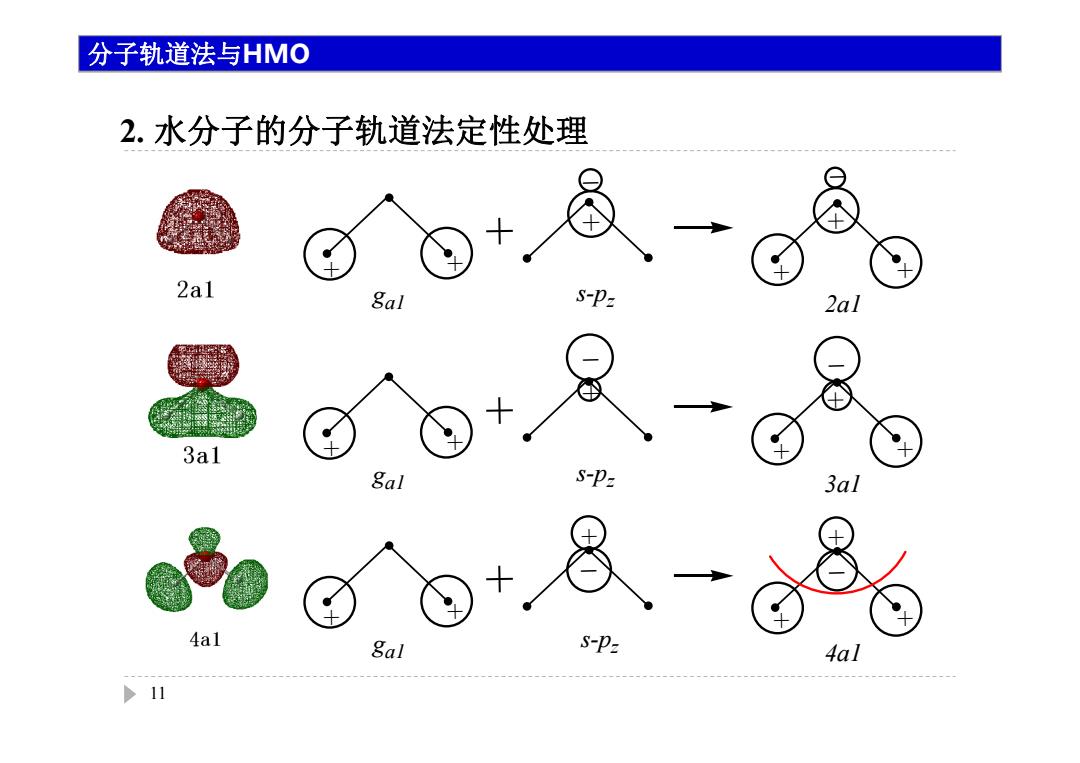
2. 水分子的分子轨道法定性处理 11 + ga1 _ _ + 2a1 + + + + + s-pz + ga1 + _ + _ + s-pz 4a1 + + + + ga1 _ _ + 3a1 + + + + + s-pz 分子轨道法与HMO

分子轨道法与HMO 2.水分子的分子轨道法定性处理 结果讨论 (1)MO的构成特点 (A) 能量最低的M0(1a1)全部贡献来自氧原子的1s (B) 成键M0为:2a1、1b2、3a1 (C) 最高占据轨道1b,是非键性质,来自氧原子的2px (D) 4a1、2b2是反键M0(空轨道)。 (2)电子谱项 若分子开壳层电子组态为(y)1(y1,其中y1和y2分别属于点群的不 可约表示G1和G,则电子谱项由直积表示G,×G2约化给出。 闭壳层组态的电子谱项属全对称表示。 基组态:(1a2(2a1)2(1b2)2(3a1)2(1b1)2 电子谱项:XA1 第一激发组态:(1a)2(2a)2(1b2)2(3a1)2(1b1)1(4a)1 电子谱项:B,、B >12
2.水分子的分子轨道法定性处理 12 (A) 能量最低的MO(1a1)全部贡献来自氧原子的 1s (1)MO的构成特点 (B) 成键MO为:2a1 、1b2 、3a1 (C) 最高占据轨道 1b1 是非键性质,来自氧原子的 2px (D) 4a1 、2b2 是反键MO(空轨道)。 分子轨道法与HMO 结果讨论 (2)电子谱项 若分子开壳层电子组态为 (y1)1 (y2)1,其中y1 和 y2 分别属于点群的不 可约表示G1 和 G2,则电子谱项由直积表示 G1 × G2 约化给出。 闭壳层组态的电子谱项属全对称表示。 第一激发组态:(1a1)2(2a1)2(1b2)2(3a1)2(1b1)1(4a1)1 电子谱项: 1B1 、3B1 基组态:(1a1)2(2a1)2(1b2)2(3a1)2(1b1)2 电子谱项:X1A1

分子轨道法与HMO 2.水分子的分子轨道法定性处理 小结 多原子分子定域键的分子轨道法定性处理步骤 (1)分析原子轨道集合在分子对称操作下的变换性质: (2)结构等价原子的相应AO按对称性组合成群轨道(SALC)即: 分子轨道碎片: (3)按对称性匹配和能量相近的原则,将不等价原子的轨道碎片 组合成分子轨道: 同位相组合 ---- 成键(无节面), 反位相组合 -反键(有节面); (4)能级图、电子组态、电子光谱项。 >13
小结 13 (4)能级图、电子组态、电子光谱项。 多原子分子定域键的分子轨道法定性处理步骤 (3)按对称性匹配和能量相近的原则,将不等价原子的轨道碎片 组合成分子轨道: 同位相组合 ---- 成键(无节面), 反位相组合 ---- 反键(有节面); (2)结构等价原子的相应AO按对称性组合成群轨道(SALC) 即: 分子轨道碎片; (1)分析原子轨道集合在分子对称操作下的变换性质; 分子轨道法与HMO 2.水分子的分子轨道法定性处理

分子轨道法与HMO 3.Huickel分子轨道法(HMO) HISTORY HMO法为量子化学的经验方法之一。它在1930年代提出, 1950-1960年代得到较为广泛的应用。HMO法在了解有机共轭分子的性 质方面,曾起到过很好的作用。 适用对象: (1) 大p键(共轭分子):CH,N02 (2) 多中心非p键(缺电子体系):B,H,H (3) 原子团簇:Cu3 有机分子的共轭效应: C1C2键长=1.35A> 典型CC双键键长(1.33A) C2C3键长=1.46A 典型CC单键键长(1.54A) CC键长趋向平均化,单双键之分不明显 结论:存在遍及整个分子的化学键一-一离域键(非定域 >14 键)
3. Hückel分子轨道法(HMO) 14 HISTORY HMO法为量子化学的经验方法之一。它在1930年代提出, 1950-1960年代得到较为广泛的应用。HMO法在了解有机共轭分子的性 质方面,曾起到过很好的作用。 (1) 大 p 键(共轭分子):C6H6,NO 适用对象: 2 (2) 多中心非 p 键(缺电子体系):B2H6,H3+ (3) 原子团簇:Cu3 分子轨道法与HMO 有机分子的共轭效应: H C1 H C2 C3 C4 H H H H CC键长趋向平均化,单双键之分不明显 C1C2键长=1.35Å > 典型CC双键键长(1.33Å) C2C3键长=1.46Å < 典型CC单键键长(1.54Å) 结论:存在遍及整个分子的化学键----离域键(非定域 键)