
《物理化学2》教学大纲 课程名称:物理化学2 课程类别(必修/选修):必修 课程英文名称:Physical Chemistry 总学时/周学时/学分:32/22 其中实验/实战学时:0 先倦课程:高等数学、无机化学、分析化学、大学物理 后续课程支撑:有机化学、化工原理、化学反应工程、化工热力学 授课时间:1-16周,周一上午34节 授课地点:7B312 授课对象:2020级应用化学卓越计划1、2班 开课学院:化学工程与能源技术学院 任课教师姓名职称:苗荣荣讲师 答疑时间、地点与方式: 1课堂:每次上课的课前、课间和课后进行答疑: 2.课外:可直接到机电楼12L302公室进行答疑: 3.线上:建立QQ/微信课程群,实施线上答疑。 课程考核方式:开卷()闭卷()课程论文()其它() 使用教材:《物理化学》下册,天津大学物理化学教研室主编,高等教育出版社,2017年(第6版) 敏学参考资料:(1)《物理化学》上、下册(第五版)南京大学物理化学教研室傅献彩 (2)《物理化学练习500例》(第二版)李大珍 课程简介:本课程是应用化学(化学工程与工艺卓越计划班)的专业基础课程。它从物质的物理现象和化学现象的联系入手,探求化学变化规律的一门 科学,在实验方法上主要采用物理学中的方法,公式推导过程中运用高等数学的知识。本学期将重点学习物理化学中热力学的应用部分及化学动力学: 热力学的应用包括化学平衡、相平衡、电化学、界面平衡及胶体化学,化学动力学主要涉及化学反应的速率。物理化学这门课程的特点有:(1)逻辑 性很强,内容前后联系密切:(2)公式的应用条件严格,而具体变化过程较多,解题比较灵活:(3)理论性很强,但极具实践性,一方面需配合做大
《物理化学 2》教学大纲 课程名称:物理化学 2 课程类别(必修/选修):必修 课程英文名称:Physical Chemistry 总学时/周学时/学分:32/2/2 其中实验/实践学时:0 先修课程:高等数学、无机化学、分析化学、大学物理 后续课程支撑:有机化学、化工原理、化学反应工程、化工热力学 授课时间:1-16 周,周一 上午 3-4 节 授课地点:7B312 授课对象:2020 级应用化学卓越计划 1、2 班 开课学院:化学工程与能源技术学院 任课教师姓名/职称:苗荣荣/讲师 答疑时间、地点与方式: 1.课堂:每次上课的课前、课间和课后进行答疑; 2.课外:可直接到机电楼 12L302 公室进行答疑; 3.线上:建立 QQ/微信课程群,实施线上答疑。 课程考核方式:开卷( )闭卷(√)课程论文( )其它( ) 使用教材:《物理化学》下册,天津大学物理化学教研室主编,高等教育出版社,2017 年(第 6 版) 教学参考资料:(1) 《物理化学》上、下册 (第五版)南京大学 物理化学教研室 傅献彩 (2) 《物理化学练习 500 例》 (第二版)李大珍 课程简介:本课程是应用化学(化学工程与工艺卓越计划班)的专业基础课程。它从物质的物理现象和化学现象的联系入手,探求化学变化规律的一门 科学,在实验方法上主要采用物理学中的方法,公式推导过程中运用高等数学的知识。本学期将重点学习物理化学中热力学的应用部分及化学动力学: 热力学的应用包括化学平衡、相平衡、电化学、界面平衡及胶体化学,化学动力学主要涉及化学反应的速率。物理化学这门课程的特点有:(1)逻辑 性很强,内容前后联系密切;(2)公式的应用条件严格,而具体变化过程较多,解题比较灵活;(3)理论性很强,但极具实践性,一方面需配合做大

量的习题,加强对理论的应用及提高独立思考问题和解决问题的能力,另一方面通过实验验证理论和发展理论,且提高实验操作技能,为进行科学研究 打下良好的基础。 程教学目标及对单业要求拍标点的支撑(与人才培养方案中“单业要求指标点分解、相关教学活动及权重赋值”相一致,每个程目标可以对应多 个毕业要求指标点) 课程教学目标 支撑毕业要求指标点 毕业要求 目标1: 1.理解物理化学的基本概念、基本原理及不同理 论间逻辑关系。掌握热力学三大定律在相平衡, 1具备从事化学化工领域工作所需的自然科学、工程基础 11掌握数学、自然科学、工程基础知识 化学平衡,电化学平衡,界面现象等领域的应用 和专业知识,能够用于解决复杂工程问题 及平衡计算。学握化学动力学基本原理、反应速 率计算方法,及反应速率的调控和判断。 目标2 运用热力学三大定律分析热力学平衡态变化过程 22能够理解到解决复杂问题的多种方 2能够运用数学、自然科学和化学学科等领域的基本原 中各种热力学参数的变化及化学反应方向的判 案,并通过分析文献选择和判断可替代的 理,识别和表达化学领域相关的工程与设计问题,并通 断。掌握从实验结果出发进行归纳和演绎的一般 解决方案 过文献研究分析以获得有效结论 方法,熟悉由假设和模型上升为理论的方法。 目标3 32能够设计开发满足需求的化学系统, 3能够设计针对化学相关的工程问题的解决方案,设计满 根据物理化学基本原理和规律合理设计和分析实 能够在设计环节体现创新意识,遵循化学 足特定需求的系统、功能单元,并体现人文知识,考虑 际化工问题,揭示日常生活中所蕴含的物理化学 体系和工程化系统开发的基本要求 社会、健康、安全、法律法规、工程伦理等因素。 知识
量的习题,加强对理论的应用及提高独立思考问题和解决问题的能力,另一方面通过实验验证理论和发展理论,且提高实验操作技能,为进行科学研究 打下良好的基础。 课程教学目标及对毕业要求指标点的支撑(与人才培养方案中“毕业要求指标点分解、相关教学活动及权重赋值”相一致,每个课程目标可以对应多 个毕业要求指标点) 课程教学目标 支撑毕业要求指标点 毕业要求 目标 1: 1. 理解物理化学的基本概念、基本原理及不同理 论间逻辑关系。掌握热力学三大定律在相平衡, 化学平衡,电化学平衡,界面现象等领域的应用 及平衡计算。掌握化学动力学基本原理、反应速 率计算方法,及反应速率的调控和判断。 1-1 掌握数学、自然科学、工程基础知识 1 具备从事化学化工领域工作所需的自然科学、工程基础 和专业知识,能够用于解决复杂工程问题 目标 2 运用热力学三大定律分析热力学平衡态变化过程 中各种热力学参数的变化及化学反应方向的判 断。掌握从实验结果出发进行归纳和演绎的一般 方法,熟悉由假设和模型上升为理论的方法。 2-2 能够理解到解决复杂问题的多种方 案,并通过分析文献选择和判断可替代的 解决方案 2 能够运用数学、自然科学和化学学科等领域的基本原 理,识别和表达化学领域相关的工程与设计问题,并通 过文献研究分析以获得有效结论 目标 3 根据物理化学基本原理和规律合理设计和分析实 际化工问题,揭示日常生活中所蕴含的物理化学 知识。 3-2 能够设计开发满足需求的化学系统, 能够在设计环节体现创新意识,遵循化学 体系和工程化系统开发的基本要求 3 能够设计针对化学相关的工程问题的解决方案,设计满 足特定需求的系统、功能单元,并体现人文知识,考虑 社会、健康、安全、法律法规、工程伦理等因素
目标4 6能够基于化学相关背景知识进行合理分析,评价应用 6-2在化学实验设计中具备综合考虑多种 了解物理化学基本原理对经济、社会发展和环境 化学实践和相关工程问题解决方案对社会、健康、安全、 制约因素的意识,能够合理分析和评价工 的理论指导和应用承接作用,理解学生应具备的 法律法规以及工程伦理的影响,并理解应承担的社会责 程实践与相关因素间的关系 职业及伦理规范。 任 理论散学进程表 救学模式 周次 散学主题 授课教师 学时数 教学内容(盒点、难点、课程思政融入点) 支撑课程 教学方法 作业安排 (线上/线下) 目标 重点:温习热力学三大定律及多组分系统热 力学、介绍化学反应的方向及平衡条件,重 阅读两篇与 点掌握理想气体的等温方程 化学反应的方 化学创新发 难点:掌握理想气体的等温方程 目标1 向及平衡条 苗荣荣 2 展有关的文 思政内容:回顾物理化学课程的演变过程及 线下教学 课堂讲授 件,等温方程 章或书籍 热力学领域历代伟人的巨大贡献。通过热力 学三大定律的发现历史以及中国著名化学家 的故事,培养学习学习化学兴趣,增强学生 爱国热情和投身化学科学创新事业的理想。 理解标准平衡常数的定义: 课后作业: 标准平衡常数 重点:掌握平衡常数的计算和测量方法 平衡常数的 目标1 2 苗荣荣 2 线下教学 课堂讲授 及计算 课程思政融入点:区分并探讨宏观化学平衡 求算及平衡 和撤观化学平衡,培有学生的独立思考能力、 移动判断
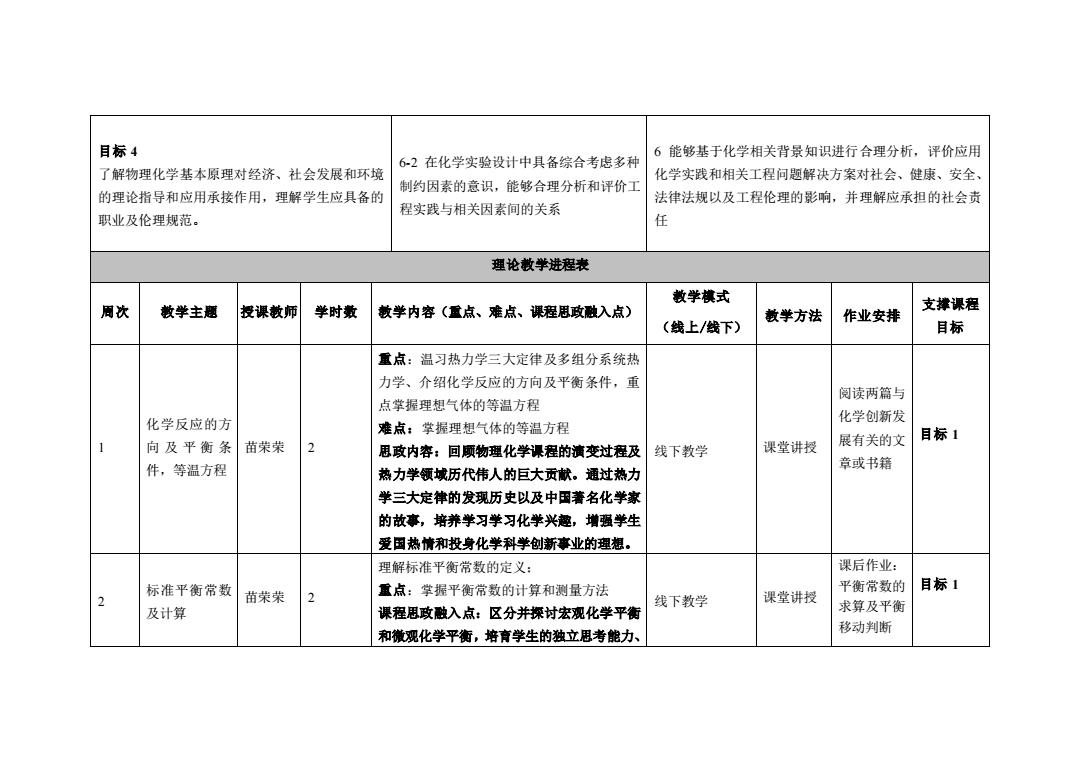
目标 4 了解物理化学基本原理对经济、社会发展和环境 的理论指导和应用承接作用,理解学生应具备的 职业及伦理规范。 6-2 在化学实验设计中具备综合考虑多种 制约因素的意识,能够合理分析和评价工 程实践与相关因素间的关系 6 能够基于化学相关背景知识进行合理分析,评价应用 化学实践和相关工程问题解决方案对社会、健康、安全、 法律法规以及工程伦理的影响,并理解应承担的社会责 任 理论教学进程表 周次 教学主题 授课教师 学时数 教学内容(重点、难点、课程思政融入点) 教学模式 (线上/线下) 教学方法 作业安排 支撑课程 目标 1 化学反应的方 向 及 平 衡 条 件,等温方程 苗荣荣 2 重点:温习热力学三大定律及多组分系统热 力学、介绍化学反应的方向及平衡条件,重 点掌握理想气体的等温方程 难点:掌握理想气体的等温方程 思政内容:回顾物理化学课程的演变过程及 热力学领域历代伟人的巨大贡献。通过热力 学三大定律的发现历史以及中国著名化学家 的故事,培养学习学习化学兴趣,增强学生 爱国热情和投身化学科学创新事业的理想。 线下教学 课堂讲授 阅读两篇与 化学创新发 展有关的文 章或书籍 目标 1 2 标准平衡常数 及计算 苗荣荣 2 理解标准平衡常数的定义; 重点:掌握平衡常数的计算和测量方法 课程思政融入点:区分并探讨宏观化学平衡 和微观化学平衡,培育学生的独立思考能力、 线下教学 课堂讲授 课后作业: 平衡常数的 求算及平衡 移动判断 目标 1
协作精神、沟通和交流的能力,引导学生学 思政作业: 好专业知识、掌握专业本领,拓展多方面的 要求学生分 能力,全面成长成才。 组探讨宏观 化学平衡和 微观化学平 衡的辩证关 芳 重点:掌握范特霍夫方程,标准平衡常随温 影响标准平衡 度变化规律,标准平衡常数的计算,会判断 标准平衡常 常数的因素, 压力、惰性组分及反应物量对平衡移动的影 数的影响规 真实气体、混 目标1 3 苗荣荣 合物及溶液中 响: 线下教学 分组讨论 律及该章知 难点:真实气体、液态混合物及液态溶液中 识点总结: 的反应化学平 的化学平衡问题 衡 相律、单组分 重点:相平衡的基本概念,相律介绍及其应 课后作业: 相图、二组分 用:单组分相图中各部分表示含义,压力组 根据相图绘 理想液态混合 苗荣荣 成图,杠杆规则,温度组成图: 线下教学 课堂讲授 制步冷曲线 目标2 物气-液平衡 难点:二组分理想液态混合物系统气-液平衡 相图 相图各个部分含义及步冷曲线绘制 二组分真实液 重点:二组分完全互溶的真实液态混合物体 课后作业: 态完全互溶、 苗荣荣 、2 系压力组成图及温度组成图,介绍部分互溶 线下教学 课堂讲授 根据不同体 目标2 液态部分及完 液体的相互溶解度,共轭溶液的饱和蒸气压, 系的温度
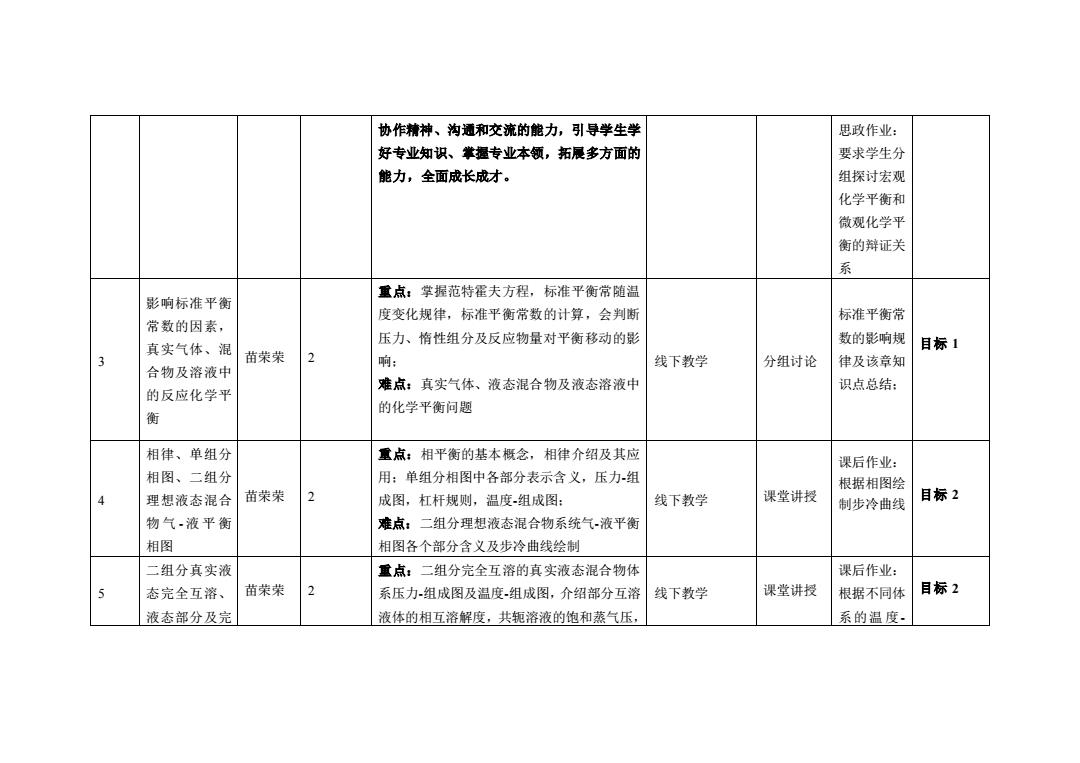
协作精神、沟通和交流的能力,引导学生学 好专业知识、掌握专业本领,拓展多方面的 能力,全面成长成才。 思政作业: 要求学生分 组探讨宏观 化学平衡和 微观化学平 衡的辩证关 系 3 影响标准平衡 常数的因素, 真实气体、混 合物及溶液中 的反应化学平 衡 苗荣荣 2 重点:掌握范特霍夫方程,标准平衡常随温 度变化规律,标准平衡常数的计算,会判断 压力、惰性组分及反应物量对平衡移动的影 响; 难点:真实气体、液态混合物及液态溶液中 的化学平衡问题 线下教学 分组讨论 标准平衡常 数的影响规 律及该章知 识点总结; 目标 1 4 相律、单组分 相图、二组分 理想液态混合 物 气 -液平衡 相图 苗荣荣 2 重点:相平衡的基本概念,相律介绍及其应 用;单组分相图中各部分表示含义,压力 - 组 成图,杠杆规则,温度 -组成图; 难点:二组分理想液态混合物系统气 -液平衡 相图各个部分含义及步冷曲线绘制 线下教学 课堂讲授 课后作业: 根据相图绘 制步冷曲线 目标 2 5 二组分真实液 态完全互溶、 液态部分及完 苗荣荣 2 重点:二组分完全互溶的真实液态混合物体 系压力 -组成图及温度 -组成图,介绍部分互溶 液体的相互溶解度,共轭溶液的饱和蒸气压, 线下教学 课堂讲授 课后作业 : 根据不同体 系的温 度 - 目标 2

全不互溶系统 部分互溶系统的温度组成图和完全不互溶系 组成图指出 的气-液平衡 统的温度组成图 每部分表示 相图、二组分 难点:共轭溶液的饱和蒸气压,部分互溶系 的状态及相 固态不互溶系 统的温度组成图和完全不互溶系统的温度 律的计算 统液,固平衡 组成图 相图 生成化合物的 重点:介绍生产稳定化合物及不稳定化合物 二组分凝聚系 讨论总结各 系统的二组分相图,固态完全互溶及部分互 统相图、二组 类相图的特 溶系统的液固平衡相图,了解三组分系统的 分固态固溶系 征,由已知 6 苗荣荣 2 图解表示法及三组分系统对液体部分互溶的 线下教学 分组讨论 目标2 统液.固平衡 相图判断该 液.液平衡相图 相图、三组分 体系是何种 难点:生成不稳定化合物系统的液-固平衡相 系统液,液平 体系 图相态判断及相律运用: 衡相图 重点:介绍电极过程、电解质溶液及法拉第 定律、离子迁移数的定义,物理意义及测量 方法、介绍溶液体系中电导、电导率、摩尔 课后作业: 电化学基本概 电导概念: 苗荣荣 、2 利用电导率 难点:介绍电解质溶液的活度、活度因子, 线下教学 课堂讲授 目标2 念 进行水解常 了解德拜休克尔极限公式 数计算 思政内容:普通蒸馏水的电导率约为1*103 S·m',如果水质被污染,水体里面含有的导 电离子数目会显著增多,并引起水的电导率
全不互溶系统 的 气 -液平衡 相图、二组分 固态不互溶系 统 液 -固平衡 相图 部分互溶系统的温度 -组成图和完全不互溶系 统的温度 -组成图 难点:共轭溶液的饱和蒸气压,部分互溶系 统的温度 -组成图和完全不互溶系统的温度 - 组成图 组成图指出 每部分表示 的状态及相 律的计算 6 生成化合物的 二组分凝聚系 统相图、二组 分固态固溶系 统 液 -固平衡 相图、三组分 系统液 - 液 平 衡相图 苗荣荣 2 重点:介绍生产稳定化合物及不稳定化合物 系统的二组分相图,固态完全互溶及部分互 溶系统的液 -固平衡相图,了解三组分系统的 图解表示法及三组分系统对液体部分互溶的 液-液平衡相图 难点:生成不稳定化合物系统的液 -固平衡相 图相态判断及相律运用; 线下教学 分组讨论 讨论总结各 类相图的特 征,由已知 相图判断该 体系是何种 体系 目标 2 7 电化学基本概 念 苗荣荣 2 重点:介绍电极过程、电解质溶液及法拉第 定律、离子迁移数的定义,物理意义及测量 方法、介绍溶液体系中电导、电导率、摩尔 电导概念; 难点:介绍电解质溶液的活度、活度因子, 了解德拜 -休克尔极限公式 思政内容:普通蒸馏水的电导率约为 1*10 - 3 S·m- 1,如果水质被污染,水体里面含有的导 电离子数目会显著增多,并引起水的电导率 线下教学 课堂讲授 课后作业: 利用电导率 进行水解常 数计算 目标 2