
2)电解池: 电解池:充电过程,电能一→化学能 例:Zn++Cu 一→ Zn+Cu+不能发生 若在可逆电池:电解,能发生 (-)Zn++2e一→Zm 还原,阴极 (+)Cu-→Cu++2e 氧化,阳极 总反应:Zn++Cu一→Zn+Cu+
1 2)电解池: 电解池:充电过程,电能—→化学能 例:Zn++ + Cu —→ Zn + Cu++ 不能发生 若在可逆电池:电解,能发生 (-)Zn++ + 2e —→ Zn 还原,阴极 (+)Cu —→ Cu++ + 2e 氧化,阳极 总反应:Zn++ + Cu —→ Zn + Cu++
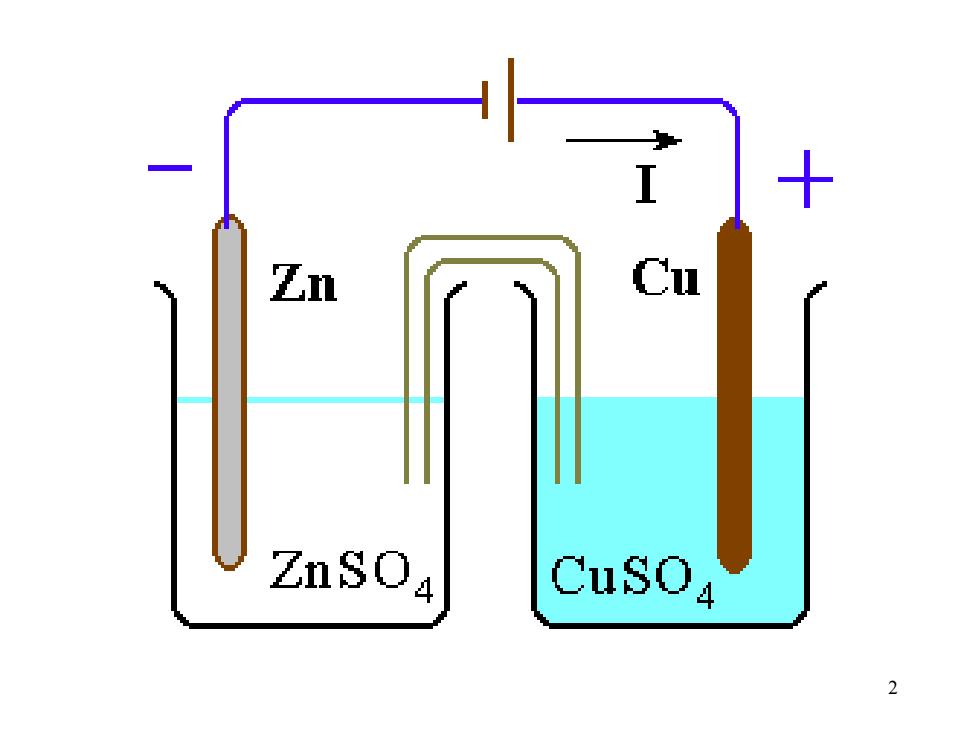
Zn ZnSO4 CuSOa 2
2

说明:a)电解池: 负极(-):还原反应 阳极(+):氧化反应 3.电池的表示 1)“|”或“,”表示不同相的接界, “‖”表示盐桥 例:Zn(s)|H2SO4(I)|Cu(s) Zn (s)ZnCl (1)AgCI (s),Ag (s) Zn (s)ZnSO (1)II CuSO (1)Cu (s) 3
3 负极(-):还原反应 阳极(+):氧化反应 说明:a)电解池: 3. 电池的表示 1)“∣”或“,”表示不同相的接界, “‖”表示盐桥 例: Zn(s)∣H2 SO4(l)∣Cu(s) Zn(s)∣ZnCl2(l)∣AgCl(s), Ag(s) Zn(s)∣ZnSO4(l)‖CuSO4(l)∣Cu(s)

2)写原电池时,一般左边(一)极, 右边(十)极 3)标出体系T,P,m及物态, 298K,P,m=m°,可略 4)气体电极,因气体不能直接作为电极, 必须惰性金属如Pt,惰性电极不参加 反应,可略 (Pt),H2(g,P)HSO(m)O2(g,P2),(Pt)
4 2)写原电池时,一般左边(-)极, 右边(+)极 3)标出体系 T,P,m 及物态, 298K,P θ,m=mθ,可略 4)气体电极,因气体不能直接作为电极, 必须惰性金属如 Pt,惰性电极不参加 反应,可略 (Pt), H2 (g,P1 ) ∣HSO4 (m) ∣O2 (g,P2 ), (Pt)

二.电化学反应的△G1,p和可逆电池电动势 1.电化学反应△Gm,P 等T,P,可逆条件下:-△GT,=W可' W可'=nFE n; 电极反应中得失电子数 E:电池的电动势 -A GT,P=nFE 表示可逆电池的化学势来源于化学能 在T,P,可逆:-△,G,=nFE E:标准电池的电动势 5
5 二.电化学反应的Δ rGT,P和可逆电池电动势 1. 电化学反应Δ rGT,P 等 T,P,可逆条件下:-Δ rGT,P =W 可 ' W 可 '=nFE n:电极反应中得失电子数 E:电池的电动势 -Δ rGT,P = nFE 表示可逆电池的化学势来源于化学能 在 T,P θ,可逆:-Δ rG θ T,P = nFEθ E θ:标准电池的电动势