
第十章血清无机离子及微量元素测定第一节钾、钠离子测定钠离子(Sodium ion,Nat)是细胞外液中的主要阳离子,含量最多,平均浓度为140mmol/L其次为钾离子(potassium ion,K+)平均浓度为4.5mmol/L。由于钠、钾离子对机体有重要的生理作用,血清(浆)中钠、钾浓度的改变与某些疾病有密切的关系,故临床上非常重视血清钾、钠浓度的测定,且多数情况下是同时被测定。体液中钠、钾测定的常用方法有化学法、火焰发射光谱法、离子选择电极法及原子吸收分光光度法。化学法因操作步骤繁琐,测定结果的准确性及精密性差而被淘汰。我国卫生部临床检验中心推荐火焰发射光谱法(flameemissionspectrophotometry,FES)和离子选择电极电位分析测定法(ionselectiveelectrodes,IES)为钠、钾测定方法,其中FES法为参考方法。近来发展的酶法测定钠、钾具有特异性强、与火焰发射光谱法高度相关等优点,日益受到临床化学家的重视。血清钾、钠的原子吸收光谱法测定灵敏、准确,但设备昂贵,需要特殊的元素灯,因此不能广泛使用。本节主要介绍火焰发射光谱法和离子选择性电极法。实验55火焰发射光谱法测定血清钾、钠离子【原理】火焰发射光谱法(FES)是一种原子发射光谱分析技术,利用火焰的热能使原子被激发而发射出特异的光谱进行分析。丙烷-空气火焰的温度使血清或尿液中的K+、Na+气化这些气化的离子从还原焰中获得电子生成基态原子Na、K。基态原子在火焰中被加热,结果生成激发态原子Na和K。激发态的原子不稳定,能迅速回到基态,放出能量,发射出元素特有波长的辐射谱线,钠的特征谱线为589nm(黄色);钾的特征谱线为767nm(深红色),用相应波长的滤光片将谱线分离,然后通过光电管或光电池转换成电信号,经放大器放大后进行测量。样品溶液中钠、钾浓度越大,所发射的光谱越强,发射光谱强度直接与钠钾浓度成正比。用已知含量的标准液与待测标本对比,即可计算出血清、尿等标本中钠钾的浓度。内
第十章 血清无机离子及微量元素测定 第一节 钾、钠离子测定 钠离子(Sodium ion, Na+ )是细胞外液中的主要阳离子,含量最多,平均浓度为 140mmol/L, 其次为钾离子(potassium ion,K+)平均浓度为 4.5mmol/L。由于钠、钾离子对机体有重要的 生理作用,血清(浆)中钠、钾浓度的改变与某些疾病有密切的关系,故临床上非常重视血清 钾、钠浓度的测定,且多数情况下是同时被测定。体液中钠、钾测定的常用方法有化学法、 火焰发射光谱法、离子选择电极法及原子吸收分光光度法。化学法因操作步骤繁琐,测定结 果的准确性及精密性差而被淘汰。我国卫生部临床检验中心推荐火焰发射光谱法(flame emission spectrophotometry,FES)和离子选择电极电位分析测定法(ionselective electrodes,IES) 为钠、钾测定方法,其中 FES 法为参考方法。近来发展的酶法测定钠、钾具有特异性强、与 火焰发射光谱法高度相关等优点,日益受到临床化学家的重视。血清钾、钠的原子吸收光谱 法测定灵敏、准确,但设备昂贵,需要特殊的元素灯,因此不能广泛使用。本节主要介绍火 焰发射光谱法和离子选择性电极法。 实验 55 火焰发射光谱法测定血清钾、钠离子 【原理】 火焰发射光谱法(FES)是一种原子发射光谱分析技术,利用火焰的热能使原子 被激发而发射出特异的光谱进行分析。丙烷-空气火焰的温度使血清或尿液中的 K+、Na +气化。 这些气化的离子从还原焰中获得电子生成基态原子 Na0、K0。基态原子在火焰中被加热,结 果生成激发态原子 Na*和 K*。激发态的原子不稳定,能迅速回到基态,放出能量,发射出元 素特有波长的辐射谱线,钠的特征谱线为 589nm(黄色);钾的特征谱线为 767nm(深红色),用 相应波长的滤光片将谱线分离,然后通过光电管或光电池转换成电信号,经放大器放大后进 行测量。样品溶液中钠、钾浓度越大,所发射的光谱越强,发射光谱强度直接与钠钾浓度成 正比。用已知含量的标准液与待测标本对比,即可计算出血清、尿等标本中钠钾的浓度。内

标法用含锂的溶液作稀释液,同时测定锂的电信号(锂火焰呈红色,波长为671nm),根据钠或钾电信号与锂电信号的比值作为定量参数进行钠、钾含量的计算,以减少由于雾化速度科火焰温度的波动所引起的测定误差,可提高测定的准确度和精密度,当前国产火焰光度计多属直接测定型,本实验介绍直接法。【试剂与器材】1.钾标准贮存液(10mmol/L)精确称取经110~120℃烘烤4h以上并置于干燥器至恒重的氯化钾(AR或GR)0.7455g,用去离子水溶解,并定容至1000ml。2.钠标准贮存液(200mmol/L)精确称取经110~120℃烘烤4h以上并置干燥器至恒重的氯化钠(AR或GR)11.691g,用去离子水溶解后定容至1000ml。3.钠钾标准应用液1(钾0.04mmol/L,钠1.2mmol/L)取钾标准贮存液4ml、钠标准赔存液6ml溶于去离子水中,并定容至1000ml。贮存于塑料瓶中备用。4.钠钾标准应用液II(钾0.04mmol/L,钠1.4mmol/L)取钾标准贮存液4ml、钠标准购存液7ml溶于去离子水中,并定容至1000ml,贮存于塑料瓶中备用。5.钾钠标准应用液II(钾0.04mmol/L,钠1.6mmol/L)取钾标准贮存液4ml、钠标准购存液8ml溶于去离子水中,并定容至1000ml,贮存于塑料瓶中备用。6.HG-3型火焰光度仪(国产)。【操作步骤】1.待测标本准备取不溶血的血清0.1ml,加去离子水9.9ml稀释。24h尿液标本充分混合后,吸出尿液,用去离子水作适当稀释。稀释的血清或尿液标本置火焰光度计的样品吸入管吸入,进行测定。2.仪器准备不同型号的仪器操作步骤不完全一样,可按仪器说明书进行操作。不同厂家生产的仪器虽然型号不同,但主机(包括空气压缩机)基本上包括雾化燃烧部分、光学部分和光度测量部分。国产火焰光度仪主要有6400 型和HG-3型,本节以国产HG-3型为例描述其工作流程:(1)接通电源,开启空气压缩机开关,2~3min后调节压缩空气压力为0.4kg/cm2。(2)检查各管道有无漏气,调节气阀并核对气压
标法用含锂的溶液作稀释液,同时测定锂的电信号(锂火焰呈红色,波长为 671nm),根据钠 或钾电信号与锂电信号的比值作为定量参数进行钠、钾含量的计算,以减少由于雾化速度和 火焰温度的波动所引起的测定误差,可提高测定的准确度和精密度,当前国产火焰光度计多 属直接测定型,本实验介绍直接法。 【试剂与器材】 1.钾标准贮存液(10mmol/L) 精确称取经 110~120℃烘烤 4h 以上并置于干燥器至恒重 的氯化钾(AR 或 GR)0.7455g,用去离子水溶解,并定容至 1 000ml。 2.钠标准贮存液(200mmol/L) 精确称取经 110~120℃烘烤 4h 以上并置干燥器至恒重 的氯化钠(AR 或 GR)11.691g,用去离子水溶解后定容至 1 000ml。 3.钠钾标准应用液Ⅰ(钾 0.04mmol/L,钠 1.2mmol/L) 取钾标准贮存液 4ml、钠标准贮 存液 6ml 溶于去离子水中,并定容至 1 000ml。贮存于塑料瓶中备用。 4.钠钾标准应用液Ⅱ(钾 0.04mmol/L,钠 1.4mmol/L) 取钾标准贮存液 4ml、钠标准贮 存液 7ml 溶于去离子水中,并定容至 1 000ml,贮存于塑料瓶中备用。 5.钾钠标准应用液Ⅲ(钾 0.04mmol/L,钠 1.6mmol/L) 取钾标准贮存液 4ml、钠标准贮 存液 8ml 溶于去离子水中,并定容至 1 000ml,贮存于塑料瓶中备用。 6.HG-3 型火焰光度仪(国产)。 【操作步骤】 1.待测标本准备 取不溶血的血清 0.1ml,加去离子水 9.9ml 稀释。24h 尿液标本充分混 合后,吸出尿液,用去离子水作适当稀释。稀释的血清或尿液标本置火焰光度计的样品吸入 管吸入,进行测定。 2.仪器准备 不同型号的仪器操作步骤不完全一样,可按仪器说明书进行操作。不同厂 家生产的仪器虽然型号不同,但主机(包括空气压缩机)基本上包括雾化燃烧部分、光学部分 和光度测量部分。国产火焰光度仪主要有 6400 型和 HG-3 型,本节以国产 HG-3 型为例描述 其工作流程: (1) 接通电源,开启空气压缩机开关,2~3min 后调节压缩空气压力为 0.4kg/cm2。 (2) 检查各管道有无漏气,调节气阀并核对气压

(3)选择钠或钾测定档(4)点火,要求火焰高度稳定,焰色纯净,以不显黄色为宜。(5)吸入去离子水冲洗管道1min,调节零点,至少稳定1min,即可进行测定。3.测定吸入钠钾标准应用液(I、II、IⅢI),分别记录各标准液读数;吸入去离子水,待指针回到零点,再吸入待测标本,记录测定液读数。4.关机、使用完毕后,应以去离子水喷雾冲洗管道1~2min,然后依次关闭检流计、燃气及空气压缩机开关。【计算】1.绘制校正曲线以不同浓度的钠钾标准应用液(I、II、I)测定的发光强度读数为坐标,以浓度为横坐标,绘制校正曲线,然后根据待测标本的读数从校正曲线上查得标本中钠、钾的浓度。血清钾在10mmol/L内呈直线关系,血清钠在高浓度区似抛物线状,失去直线关系。故不宜用单一标准液来计算测定结果。2.如果认为每次测定钠、钾都要做系列标准曲线过于麻烦,可以用120、140、160mmol/L三个钠标准液(均含钾4mmol/L)作比较法测定,每次同时作高、中、低三个浓度标准测定,使待测标本读数在高、低二个标准计数之间,然后下列公式计算:-(Ru=R+(C.-C)+C, DCu=(Rμ-R,式中:Cu为测定标本浓度;Ru为测定标本读数;Ch为高标准液浓度;RH为高标准液读数;CL为低标准液浓度:RL为低标准液读数D为稀释倍数【参考范围】血清钠135~145mmol/L;血清钾3.6~5.1mmol/L。尿钠40~220mmol/L;尿钾25~125mmol/24h。【注意事项】1.溶血或延迟分离血清可使血清钾浓度升高,应及时分离血清,置于有塞试管内冰箱保存。若遇到标本溶血,应在报告单上注明,以避免医生误解
(3) 选择钠或钾测定档 (4) 点火,要求火焰高度稳定,焰色纯净,以不显黄色为宜。 (5) 吸入去离子水冲洗管道 1min,调节零点,至少稳定 1min,即可进行测定。 3.测定 吸入钠钾标准应用液(Ⅰ、Ⅱ、Ⅲ),分别记录各标准液读数;吸入去离子水, 待指针回到零点,再吸入待测标本,记录测定液读数。 4.关机 使用完毕后,应以去离子水喷雾冲洗管道 1~2 min,然后依次关闭检流计、燃 气及空气压缩机开关。 【计算】 1.绘制校正曲线 以不同浓度的钠钾标准应用液(Ⅰ、Ⅱ、Ⅲ)测定的发光强度读数为纵 坐标,以浓度为横坐标,绘制校正曲线,然后根据待测标本的读数从校正曲线上查得标本中 钠、钾的浓度。血清钾在 10mmol/L 内呈直线关系,血清钠在高浓度区似抛物线状,失去直 线关系。故不宜用单一标准液来计算测定结果。 2.如果认为每次测定钠、钾都要做系列标准曲线过于麻烦,可以用 120、140、160mmol/L 三个钠标准液(均含钾 4mmol/L)作比较法测定,每次同时作高、中、低三个浓度标准测定, 使待测标本读数在高、低二个标准计数之间,然后下列公式计算: (C C ) C D R R R R C H L L H L U L U + − − − = 式中:CU 为测定标本浓度;RU 为测定标本读数; CH 为高标准液浓度;RH 为高标准液读数; CL 为低标准液浓度;RL 为低标准液读数; D 为稀释倍数 【参考范围】 血清钠 135~145mmol/L;血清钾 3.6~5.1mmol/L。 尿钠 40~220mmol/L;尿钾 25~125mmol/24h。 【注意事项】 1.溶血或延迟分离血清可使血清钾浓度升高,应及时分离血清,置于有塞试管内冰箱保 存。若遇到标本溶血,应在报告单上注明,以避免医生误解
2.测定用玻璃器皿必须用去离子水冲洗干净,不得有离子污染。3.血清稀释必须准确,若遇血清标本结果异常偏低时,必须反复测定和核对。4.火焰光度计的各管道应保持通畅,不得有堵塞,燃料气压及助燃气压应保持恒定,并有一定比例,应防止室内空气流动造成的火焰摆动。5.所用燃料为易燃物,有一定的危险性,应注意安全。6.尿液标本钠、钾浓度波动范围大,故稀释倍数要作适当调整,使尿钾的测定浓度在10mmol/L以内,尿钠的测定读数位于高、中、低三个标准管中两个标准读数之间,以便作比较法计算尿钠浓度。现将尿钠稀释方法列于表10-1。表 10-1尿液稀释方法尿液(ml)稀释倍数稀释比例去离子水(ml) 0.5 9.520 1: 201000.1 9.91: 1005001:100稀释尿2.08.01: 5009.01 0001:100稀释尿1.01: 1 000【评价】1.火焰光度法测定钠、血钾快速准确,操作简便。标本不需去蛋白。线性范围:血钠100~160mmol/L,尿钠0~200mmol/L;血钾2~8mmol/L,尿钾0~200mmol/L。变异系数Na+批内0.7%~1.4%、批间1.5%~1.8%,K+批内1.5%~2.0%、批间2.3%~3.5%。回收率:K+97.1%~105%, Nat89.4%~93.30%2.严重的高脂血症和高蛋白血症的血清样品,由于单位体积血清中水量明显减少(脂质和蛋白占据体积),会导致假性低钠、钾血症。有人提出用校正因数F计算高脂血症血清离子的真正浓度。F=1+(0.021X TG)-0.006TG为血清甘油三酯的浓度,以g/dl [(mg/dl)×0.0113=(mmol/L)计。正常浓度的血清甘
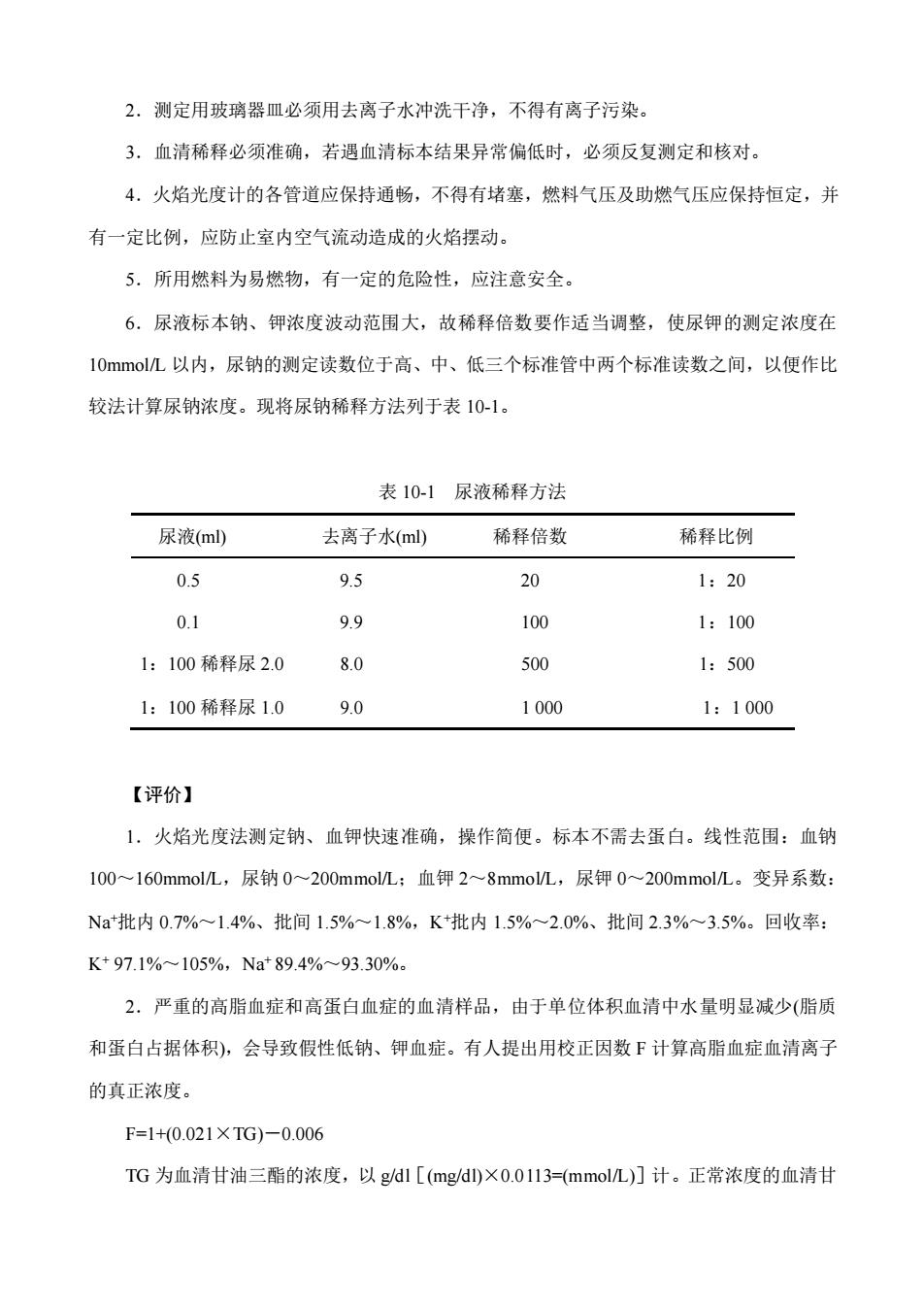
2.测定用玻璃器皿必须用去离子水冲洗干净,不得有离子污染。 3.血清稀释必须准确,若遇血清标本结果异常偏低时,必须反复测定和核对。 4.火焰光度计的各管道应保持通畅,不得有堵塞,燃料气压及助燃气压应保持恒定,并 有一定比例,应防止室内空气流动造成的火焰摆动。 5.所用燃料为易燃物,有一定的危险性,应注意安全。 6.尿液标本钠、钾浓度波动范围大,故稀释倍数要作适当调整,使尿钾的测定浓度在 10mmol/L 以内,尿钠的测定读数位于高、中、低三个标准管中两个标准读数之间,以便作比 较法计算尿钠浓度。现将尿钠稀释方法列于表 10-1。 表 10-1 尿液稀释方法 尿液(ml) 去离子水(ml) 稀释倍数 稀释比例 0.5 9.5 20 1:20 0.1 9.9 100 1:100 1:100 稀释尿 2.0 8.0 500 1:500 1:100 稀释尿 1.0 9.0 1 000 1:1 000 【评价】 1.火焰光度法测定钠、血钾快速准确,操作简便。标本不需去蛋白。线性范围:血钠 100~160mmol/L,尿钠 0~200mmol/L;血钾 2~8mmol/L,尿钾 0~200mmol/L。变异系数: Na+批内 0.7%~1.4%、批间 1.5%~1.8%,K+批内 1.5%~2.0%、批间 2.3%~3.5%。回收率: K+ 97.1%~105%,Na+ 89.4%~93.30%。 2.严重的高脂血症和高蛋白血症的血清样品,由于单位体积血清中水量明显减少(脂质 和蛋白占据体积),会导致假性低钠、钾血症。有人提出用校正因数 F 计算高脂血症血清离子 的真正浓度。 F=1+(0.021×TG)-0.006 TG 为血清甘油三酯的浓度,以 g/dl[(mg/dl)×0.0113=(mmol/L)]计。正常浓度的血清甘

油三酯对测定结果无影响;若浓度增高至2.5g/d1时,F=1+(0.021×2.5)-0.006=1.047,测定浓度比实际浓度低5%。3.本方法需要特殊仪器,使用易燃气体,有潜在危险。目前国产火焰光度计多属直接型,国外产品多属内标型,用锂或作内标,能直接显示测定结果,内标测定法能减少由于雾化速度和火焰温度的波动而引起的误差,可提高测定的精密度和准确性。4.对较高的钠浓度通过影响钾原子在火焰中的离子化程度而对钾的结果产生小的影响,干扰的程度取决于标准液和病人标本中钠/钾比值不一致的程度,就血浆或血清中常见的数值范围而言,对钾干扰的最大误差为0.2mmol/L,但在尿中离子的干扰可能更大些。实验56离子选择性电极电位法测定血清钾、钠离子【原理】离子选择性电极(ISE)电位法是以测定电池的电位为基础的定量分析方法。将离子选择性电极和一个由银/氯化银构成的参比电极连接起来,置于待测的电解质溶液中,形成一个测量电池。此电池的电位随样品的离子浓度的改变而改变,电位的变化与离子活度的对数符合能斯特(Nernst)方程E= E + 2303RT Log,-f.式中:E:离子选择性电极在测量溶液中的电位;E:离子选择性电极的标准电极电位;R:气体常数(8.314J/K-mol);n:待测离子的电荷数;T:绝对温度(237+t℃);F:法拉第常数(96487C/mol)ax:待测离子的活度;fx:待测离子的活度系数。离子选择电极由钠、钾离子不同活度的作用而产生不同的电位。这种极电位的变化由钠、钾离子活度所决定,后者与钠、钾离子浓度成比例。检测时首先加入样品,测其电位,然后
油三酯对测定结果无影响;若浓度增高至 2.5g/dl 时,F=1+(0.021×2.5)-0.006=1.047,测定 浓度比实际浓度低 5%。 3.本方法需要特殊仪器,使用易燃气体,有潜在危险。目前国产火焰光度计多属直接型, 国外产品多属内标型,用锂或铯作内标,能直接显示测定结果,内标测定法能减少由于雾化 速度和火焰温度的波动而引起的误差,可提高测定的精密度和准确性。 4.对较高的钠浓度通过影响钾原子在火焰中的离子化程度而对钾的结果产生小的影响, 干扰的程度取决于标准液和病人标本中钠/钾比值不一致的程度,就血浆或血清中常见的数值 范围而言,对钾干扰的最大误差为 0.2mmol/L,但在尿中离子的干扰可能更大些。 实验 56 离子选择性电极电位法测定血清钾、钠离子 【原理】 离子选择性电极(ISE)电位法是以测定电池的电位为基础的定量分析方法。将 离子选择性电极和一个由银/氯化银构成的参比电极连接起来,置于待测的电解质溶液中,形 成一个测量电池。此电池的电位随样品的离子浓度的改变而改变,电位的变化与离子活度的 对数符合能斯特(Nernst)方程. x x 0 Loga f nF 2.303RT E = E + 式中: E:离子选择性电极在测量溶液中的电位; E 0:离子选择性电极的标准电极电位; R:气体常数(8.314J/K·mol) ; n:待测离子的电荷数; T:绝对温度(237+t℃); F:法拉第常数(96 487C/mol) ; ax:待测离子的活度; fx:待测离子的活度系数。 离子选择电极由钠、钾离子不同活度的作用而产生不同的电位。这种极电位的变化由钠、 钾离子活度所决定,后者与钠、钾离子浓度成比例。检测时首先加入样品,测其电位,然后