
第一章 光谱技术光是一种电磁波,具有波动性和粒子性。波动性的特征是波长和频率。从理论上说,光称为光子,是由光微粒子(光量子)所组成的,而光微粒子是一种具有能量的物质,不同波长的光具有不同的能量,光子的能量与光的波长成反比,与频率成正比。光的波长可用纳米(nm)为单位来表示。人的眼睛所能感觉到的波长为 400nm 的紫色到760mm的红色,该段波长以外的光就不能看见,故400-760nm之间的光波称为可见光。短于400nm的为紫外线,短于200nm为远紫外线。长于760nm的为红外线。利用物质的发射光谱、吸收光谱或散射光谱特征对物质进行定性、定量分析的技术称光谱分析技术。光谱分析的种类很多,可按光谱产生的方式加以分类。基于发射光谱特征的主要有火焰光度法、原子发射光谱法和荧光光谱法等;基于吸收光谱特征的主要有紫外及可见分光光度法、原子吸收分光光度法和红外光谱法等;基于散射光谱特征的有比浊法等。发射光谱法是根据物质受到热能或电能等的激发后所发射出的特征光谱线来进行定性及定量分析的一种方法;吸收光谱分析法是根据溶液能吸收由光源发出的某些波长的光所形成的光谱,利用这种光谱可鉴定物质的性质和含量的一种方法;散射光谱分析法是测定光线通过溶液混悬颗粒后的光吸收或光散射程度的一种定性或定量分析法。本章介绍应用吸收光谱原理进行分析的可见及紫外光分光光度法、原子吸收分光光度法,以及应用发射光谱原理进行分析的荧光光度法。实验1紫外分光光度法测定血清蛋白质蛋白质分子中存在着含有共轭双键的酪氨酸、色氨酸和苯丙氨酸,使蛋白质在【原理】270~290nm波长范围内具有吸收紫外光的性质,其中酪氨酸的入max为275nm,色氨酸的入max为280nm,苯丙氨酸的入max为257nm,在此波长范围内,蛋白质溶液的吸收值与其浓度成正比可作定量测定。由于生物样品中常混有核酸,核酸对紫外光也有吸收,但其峰值在260nm附近,因此可用下列经验公式计算蛋白质浓度Lowry-Kalckar公式:蛋白质浓度(g/L)=1.45A280-0.74A20Warburg-Christian 公:蛋白质浓度(g/L)=1.55A280—0.76A260将280nm的吸光度与260nm的吸光度各乘以系数相减后即为接近的蛋白质浓度。A280与
第一章 光谱技术 光是一种电磁波,具有波动性和粒子性。波动性的特征是波长和频率。从理论上说,光称 为光子,是由光微粒子(光量子)所组成的,而光微粒子是一种具有能量的物质,不同波长的 光具有不同的能量,光子的能量与光的波长成反比,与频率成正比。 光的波长可用纳米(nm)为单位来表示。人的眼睛所能感觉到的波长为 400nm 的紫色到 760nm 的红色,该段波长以外的光就不能看见,故 400~760nm 之间的光波称为可见光。短于 400nm 的为紫外线,短于 200nm 为远紫外线。长于 760nm 的为红外线。 利用物质的发射光谱、吸收光谱或散射光谱特征对物质进行定性、定量分析的技术称光谱 分析技术。光谱分析的种类很多,可按光谱产生的方式加以分类。基于发射光谱特征的主要有 火焰光度法、原子发射光谱法和荧光光谱法等;基于吸收光谱特征的主要有紫外及可见分光光 度法、原子吸收分光光度法和红外光谱法等;基于散射光谱特征的有比浊法等。发射光谱法是 根据物质受到热能或电能等的激发后所发射出的特征光谱线来进行定性及定量分析的一种方 法;吸收光谱分析法是根据溶液能吸收由光源发出的某些波长的光所形成的光谱,利用这种光 谱可鉴定物质的性质和含量的一种方法;散射光谱分析法是测定光线通过溶液混悬颗粒后的光 吸收或光散射程度的一种定性或定量分析法。 本章介绍应用吸收光谱原理进行分析的可见及紫外光分光光度法、原子吸收分光光度法, 以及应用发射光谱原理进行分析的荧光光度法。 实验1 紫外分光光度法测定血清蛋白质 【原理】 蛋白质分子中存在着含有共轭双键的酪氨酸、色氨酸和苯丙氨酸,使蛋白质在 270~290nm 波长范围内具有吸收紫外光的性质,其中酪氨酸的 λmax 为 275nm,色氨酸的 λmax 为 280nm,苯丙氨酸的 λmax 为 257nm,在此波长范围内,蛋白质溶液的吸收值与其浓度成正比, 可作定量测定。由于生物样品中常混有核酸,核酸对紫外光也有吸收,但其峰值在 260nm 附近, 因此可用下列经验公式计算蛋白质浓度。 Lowry-Kalckar 公式: 蛋白质浓度(g/L) = 1.45A280 -0.74A260 Warburg-Christian 公式: 蛋白质浓度(g/L) = 1.55A280 - 0.76A260 将 280nm 的吸光度与 260nm 的吸光度各乘以系数相减后即为接近的蛋白质浓度。A280 与

A260分别代表光径为1cm时对280nm和260nm的吸光度。由于蛋白质中肽键的存在,使其在200~225nm远紫外区波长也有光吸收,因此,蛋白质浓度在一定范围内,可用A215、A225值按下述公式测定。Waddell经验公式:蛋白质浓度(g/L)=144×(A215-A225)由于血清中不同类型蛋白质中酪氨酸和色氨酸含量不同,所以测定270~290nm波段紫外吸收也会因每个样品中蛋白质氨基酸组成的差异而有较大的变异,因而这个方法不能直接用于血清总蛋白的准确定量。而在远紫外区(200~225nm)的光吸收主要由肽键所致,各种蛋白质具有相同的吸收系数,蛋白质浓度在120g/L仍符合Beer定律,因而Ressley等人建立起210nm波长下测定血清总蛋白的实用方法,其准确性与双缩脲法和Kjeldahl法间有较好的可比性。【试剂】1.0.15mol/LNaCl溶液精确称取NaC18.766g溶于1000ml容量瓶中,用蒸馏水定容。2.蛋白质标准溶液(1mg/ml)准确称取经校正后的牛血清白蛋白用0.15mol/LNaCI溶液配制成1mg/ml。【操作步骤】1.标准曲线法取8支试管,分别按表1-1加入试剂。表1-1蛋白质标准曲线的制作管号试剂蛋白质标准溶液(mg/ml)0.51.01.52.02.53.04.00.15mol/LNaCI 溶液4.03.51.03.02.52.01.5蛋白质浓度(mg/ml)0.1250.2500.3750.5000.6250.7501.00混匀后,选用1cm的石英比色杯,在280nm处以第一管调节零点,分别测定各管吸光度值。以光密度值为纵坐标,蛋白质浓度为横坐标,绘制出280nm处血清蛋白质标准曲线。取1ml血清蛋白生理盐水稀释液(应使其浓度在蛋白质标准曲线范围内),加0.15mol/LNaCI溶液3ml,混匀后,按上述方法测定吸光度值,根据标准曲线查出蛋白质浓度。2.Lowry-Kalckar公式法及Warburg-Christian公式法用0.15mol/LNaCI溶液将在血清作100倍稀释,选用光径为1cm的石英比色杯,分别在280nm和260nm波长两处测定溶液的吸光度(A),根据Lowry-Kalckar公式或Warburg-Chrisian公式计算此溶液的蛋白质浓度,再乘以稀释
A260分别代表光径为 1cm 时对 280nm 和 260nm 的吸光度。 由于蛋白质中肽键的存在,使其在 200~225nm 远紫外区波长也有光吸收,因此,蛋白质浓 度在一定范围内,可用 A215、A225值按下述公式测定。 Waddell 经验公式: 蛋白质浓度(g/L) = 144 × (A215-A225) 由于血清中不同类型蛋白质中酪氨酸和色氨酸含量不同,所以测定 270~290nm 波段紫外吸 收也会因每个样品中蛋白质氨基酸组成的差异而有较大的变异,因而这个方法不能直接用于血 清总蛋白的准确定量。而在远紫外区(200~225nm)的光吸收主要由肽键所致,各种蛋白质具有相 同的吸收系数,蛋白质浓度在 120g/L 仍符合 Beer 定律,因而 Ressley 等人建立起 210nm 波长下 测定血清总蛋白的实用方法,其准确性与双缩脲法和 Kjeldahl 法间有较好的可比性。 【试剂】 1.0.15mol/L NaCl 溶液 精确称取 NaCl 8.766g 溶于 1000ml 容量瓶中,用蒸馏水定容。 2.蛋白质标准溶液(1mg/ml)准确称取经校正后的牛血清白蛋白用 0.15mol/L NaCl 溶液配 制成 1mg/ml。 【操作步骤】 1. 标准曲线法 取 8 支试管,分别按表 1-1 加入试剂。 表 1-1 蛋白质标准曲线的制作 管号 试剂 1 2 3 4 5 6 7 8 蛋白质标准溶液(mg/ml) - 0.5 1.0 1.5 2.0 2.5 3.0 4.0 0.15mol/LNaCl 溶液 4.0 3.5 3.0 2.5 2.0 1.5 1.0 - 蛋白质浓度(mg/ml) - 0.125 0.250 0.375 0.500 0.625 0.750 1.00 混匀后,选用 1cm 的石英比色杯,在 280nm 处以第一管调节零点,分别测定各管吸光度值。 以光密度值为纵坐标,蛋白质浓度为横坐标,绘制出 280nm 处血清蛋白质标准曲线。取 1ml 血清蛋白生理盐水稀释液(应使其浓度在蛋白质标准曲线范围内),加 0.15mol/L NaCl 溶液 3ml, 混匀后,按上述方法测定吸光度值,根据标准曲线查出蛋白质浓度。 2.Lowry-Kalckar 公式法及 Warburg-Christian 公式法 用 0.15mol/L NaCl 溶液将在血清作 100 倍稀释,选用光径为 1cm 的石英比色杯,分别在 280nm 和 260nm 波长两处测定溶液的吸光 度(A),根据 Lowry-Kalckar 公式或 Warburg-Christian 公式计算此溶液的蛋白质浓度,再乘以稀释

倍数100得到血清蛋白质的真实浓度。3.Waddell公式法用0.15mol/LNaCI溶液将血清作1000倍稀释,选用光径为1cm石英比色杯,分别在215nm和225nm波长两处测定溶液的吸光度(A),根据Waddell/公式计算此溶液的蛋白质浓度,再乘以稀释倍数1000得到血清蛋白质的真实浓度。【注意事项】1.270~-290m紫外法对测定蛋白质中酪氨酸和色氨酸含量差异较大的蛋白质溶液,有一定的误差。2.本法需用高质量石英比色杯。3.紫外分光光度计使用前需对其波长进行校正。4.待测样品的蛋白质浓度应控制在15~25g/L范围内。5.注意溶液pH值,这是由于蛋白质的紫外吸收峰会随pH的改变而变化。6.受非蛋白质因素的干扰较重,除核酸外,游离的色氨酸、酪氨酸、尿酸、核苷酸、嘌呤、嘧啶和胆红素等均有干扰。附:紫外分光光度法测定核酸的浓度嘌呤碱或嘧啶碱具有共轭双键,使核苷酸和核酸在紫外光区具有特征性的吸收光谱,最大吸收峰在260nm。比色杯光径1lcm,波长260nm,1个吸光度值(IA)相当于50ug/ml双螺旋DNA;401ug/ml单螺旋DNA或RNA;20μg/ml寡核苷酸。(一)DNA 的浓度测定1.取DNA溶液10ul,加双蒸馏水600ul(即稀释61倍)。2.用双蒸馏水调零,测定260m和280nm的吸光度值(A260,A28)。 426 ×50×613. DNA 浓度(μg/ul)=10004.DNA的纯度:A26d/A280的比值应大于1.7以上。若样品中含有蛋白质(吸收峰在280nm)等杂质时,比值下降,应重新纯化。有时需要测定A230,A2a/Aa30的比值应大于2.0,如比值太小,说明样品中残存酚等有机杂质。5.DNA溶液需经一定比例稀释,不可太浓。否则,因溶液粘稠,加样器不易吸准。(二)RNA的浓度测定1.取RNA(溶于5g/LSDS溶液中)溶液10ul,加入三蒸馏水500ul中(稀释51倍)。2.将5g/LSDS用三蒸馏水作51倍稀释,用此液调零,测定RNA稀释液在260mm和280mm的吸光度(A260,A2m)。3. RNA浓度(μg/l)-4×50×611000
倍数 100 得到血清蛋白质的真实浓度。 3. Waddell 公式法 用 0.15mol/L NaCl 溶液将血清作 1000 倍稀释,选用光径为 1cm 石英比 色杯,分别在 215nm 和 225nm波长两处测定溶液的吸光度(A),根据 Waddell 公式计算此溶液的 蛋白质浓度,再乘以稀释倍数 1000 得到血清蛋白质的真实浓度。 【注意事项】 1.270~290nm 紫外法对测定蛋白质中酪氨酸和色氨酸含量差异较大的蛋白质溶液,有一 定的误差。 2.本法需用高质量石英比色杯。 3.紫外分光光度计使用前需对其波长进行校正。 4.待测样品的蛋白质浓度应控制在 15~25g/L 范围内。 5.注意溶液 pH 值,这是由于蛋白质的紫外吸收峰会随 pH 的改变而变化。 6.受非蛋白质因素的干扰较重,除核酸外,游离的色氨酸、酪氨酸、尿酸、核苷酸、嘌呤、 嘧啶和胆红素等均有干扰。 附:紫外分光光度法测定核酸的浓度 嘌呤碱或嘧啶碱具有共轭双键,使核苷酸和核酸在紫外光区具有特征性的吸收光谱,最大吸收峰在 26Onm。比色杯光径 1cm,波长 260nm, 1 个吸光度值(lA)相当于 50μg/ml 双螺旋 DNA;401μg/ml 单螺旋 DNA 或 RNA;20μg/ml 寡核苷酸。 (一)DNA 的浓度测定 1.取 DNA 溶液 l0μl,加双蒸馏水 600μl (即稀释 61 倍)。 2.用双蒸馏水调零,测定 260nm 和 280nm 的吸光度值(A260,A280)。 3.DNA 浓度(μg/μl) = 1000 A260 5061 4.DNA 的纯度:A260/A280 的比值应大于 1.7 以上。若样品中含有蛋白质(吸收峰在 280nm)等杂质时,比 值下降,应重新纯化。有时需要测定 A230,A260/A230的比值应大于 2.0,如比值太小,说明样品中残存酚等有 机杂质。 5.DNA 溶液需经一定比例稀释,不可太浓。否则,因溶液粘稠,加样器不易吸准。 (二)RNA 的浓度测定 1.取 RNA(溶于 5g/L SDS 溶液中)溶液 l0μl,加入三蒸馏水 500μl 中(稀释 51 倍)。 2.将 5g/L SDS 用三蒸馏水作 51 倍稀释,用此液调零,测定 RNA 稀释液在 260nm 和 280nm 的吸光度 (A260,A280)。 3.RNA 浓度(μg/μl) = 1000 A260 5061
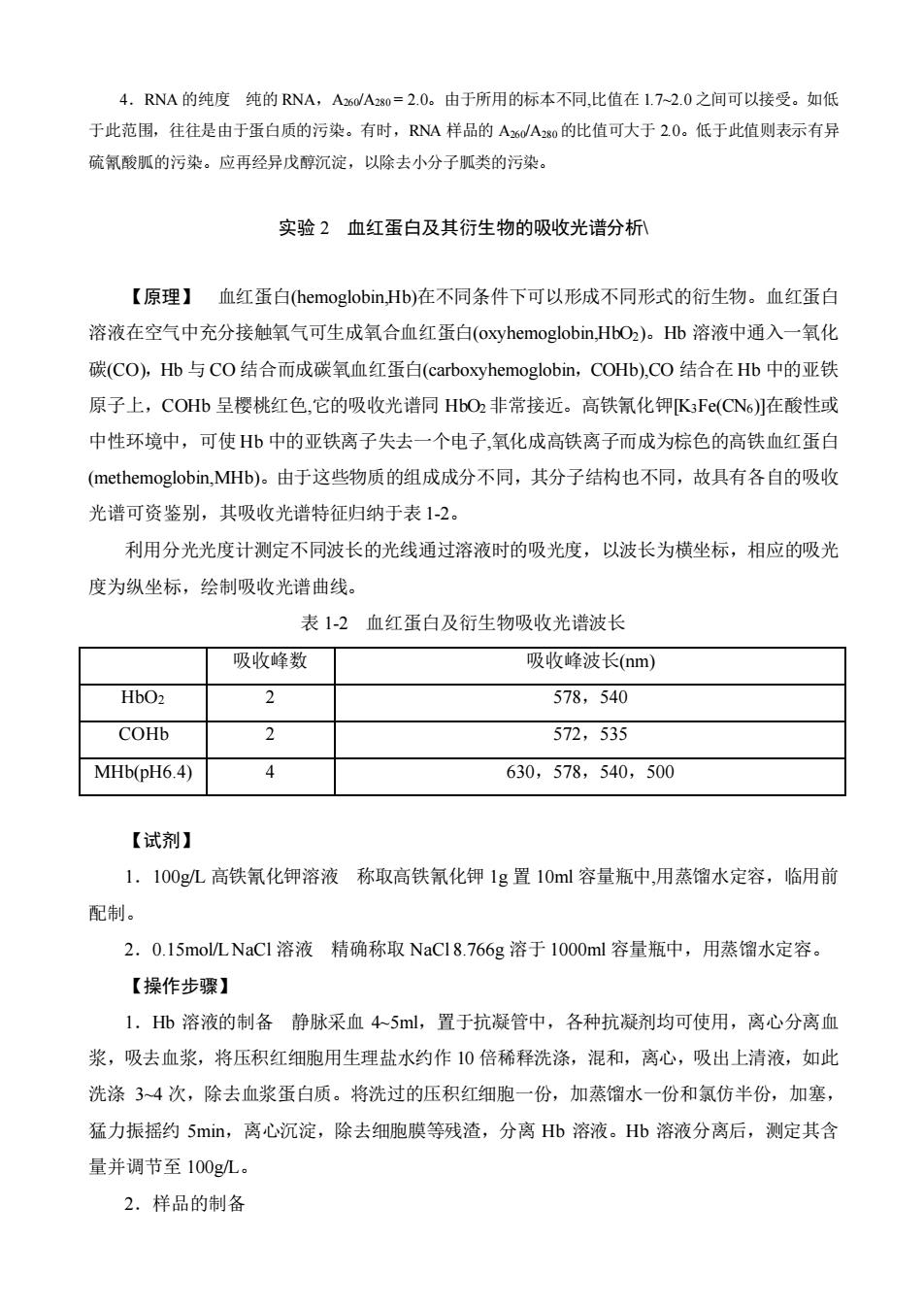
4.RNA的纯度纯的RNA,A26/A280=2.0。由于所用的标本不同,比值在1.7-2.0之间可以接受。如低于此范围,往往是由于蛋白质的污染。有时,RNA样品的A260/A280的比值可大于2.0。低于此值则表示有异硫氰酸胍的污染。应再经异戊醇沉淀,以除去小分子胍类的污染。实验2血红蛋白及其衍生物的吸收光谱分析【原理】血红蛋白(hemoglobin,Hb)在不同条件下可以形成不同形式的衍生物。血红蛋白溶液在空气中充分接触氧气可生成氧合血红蛋白(oxyhemoglobin,HbO2)。Hb 溶液中通入一氧化碳(CO),Hb 与CO结合而成碳氧血红蛋白(carboxyhemoglobin,COHb),cO结合在Hb中的亚铁原子上,COHb呈樱桃红色,它的吸收光谱同HbO2非常接近。高铁氰化钾K3Fe(CNo)I在酸性或中性环境中,可使Hb中的亚铁离子失去一个电子,氧化成高铁离子而成为棕色的高铁血红蛋白(methemoglobin,MHb)。由于这些物质的组成成分不同,其分子结构也不同,故具有各自的吸收光谱可资鉴别,其吸收光谱特征归纳于表1-2利用分光光度计测定不同波长的光线通过溶液时的吸光度,以波长为横坐标,相应的吸光度为纵坐标,绘制吸收光谱曲线。表 1-2血红蛋白及衍生物吸收光谱波长吸收峰数吸收峰波长(nm)Hb022578, 540COHb572, 5352MHb(pH6.4)630,578,540,500【试剂】1.100g/L高铁氰化钾溶液称取高铁氰化钾1g置10ml容量瓶中,用蒸馏水定容,临用前配制。2.0.15mol/LNaCl溶液精确称取NaC18.766g溶于1000ml容量瓶中,用蒸馏水定容。【操作步骤】1.Hb溶液的制备静脉采血4~5ml,置于抗凝管中,各种抗凝剂均可使用,离心分离血浆,吸去血浆,将压积红细胞用生理盐水约作10倍稀释洗涤,混和,离心,吸出上清液,如此洗涤3~4次,除去血浆蛋白质。将洗过的压积红细胞一份,加蒸馏水一份和氯仿半份,加塞,猛力振摇约5min,离心沉淀,除去细胞膜等残渣,分离Hb溶液。Hb溶液分离后,测定其含量并调节至100g/L。2.样品的制备
4.RNA 的纯度 纯的 RNA,A260/A280 = 2.0。由于所用的标本不同,比值在 1.7~2.0 之间可以接受。如低 于此范围,往往是由于蛋白质的污染。有时,RNA 样品的 A260/A280 的比值可大于 2.0。低于此值则表示有异 硫氰酸胍的污染。应再经异戊醇沉淀,以除去小分子胍类的污染。 实验 2 血红蛋白及其衍生物的吸收光谱分析\ 【原理】 血红蛋白(hemoglobin,Hb)在不同条件下可以形成不同形式的衍生物。血红蛋白 溶液在空气中充分接触氧气可生成氧合血红蛋白(oxyhemoglobin,HbO2)。Hb 溶液中通入一氧化 碳(CO),Hb 与 CO 结合而成碳氧血红蛋白(carboxyhemoglobin,COHb),CO 结合在 Hb 中的亚铁 原子上,COHb 呈樱桃红色,它的吸收光谱同 HbO2非常接近。高铁氰化钾[K3Fe(CN6)]在酸性或 中性环境中,可使 Hb 中的亚铁离子失去一个电子,氧化成高铁离子而成为棕色的高铁血红蛋白 (methemoglobin,MHb)。由于这些物质的组成成分不同,其分子结构也不同,故具有各自的吸收 光谱可资鉴别,其吸收光谱特征归纳于表 1-2。 利用分光光度计测定不同波长的光线通过溶液时的吸光度,以波长为横坐标,相应的吸光 度为纵坐标,绘制吸收光谱曲线。 表 1-2 血红蛋白及衍生物吸收光谱波长 吸收峰数 吸收峰波长(nm) HbO2 2 578,540 COHb 2 572,535 MHb(pH6.4) 4 630,578,540,500 【试剂】 1.100g/L 高铁氰化钾溶液 称取高铁氰化钾 1g 置 10ml 容量瓶中,用蒸馏水定容,临用前 配制。 2.0.15mol/L NaCl 溶液 精确称取 NaCl 8.766g 溶于 1000ml 容量瓶中,用蒸馏水定容。 【操作步骤】 1.Hb 溶液的制备 静脉采血 4~5ml,置于抗凝管中,各种抗凝剂均可使用,离心分离血 浆,吸去血浆,将压积红细胞用生理盐水约作 10 倍稀释洗涤,混和,离心,吸出上清液,如此 洗涤 3~4 次,除去血浆蛋白质。将洗过的压积红细胞一份,加蒸馏水一份和氯仿半份,加塞, 猛力振摇约 5min,离心沉淀,除去细胞膜等残渣,分离 Hb 溶液。Hb 溶液分离后,测定其含 量并调节至 100g/L。 2.样品的制备

(1)HbO2溶液:取Hb溶液4滴,加蒸馏水5ml。(2)COHb溶液:取Hb溶液3滴,加蒸馏水5ml,再加辛醇1滴,摇匀,用滴管通入CO2~3min呈樱桃红色。(3)MHb溶液:取Hb溶液3滴,加蒸馏水5ml,加新鲜配制的100g/L高铁氰化钾3滴,混匀,呈棕色,尽可能快比色。3.测定分别取上述溶液3ml盛于比色杯内,以蒸馏水作空白,在波长470~650nm范围内,每隔20nm测吸光度一次,在接近吸收高峰时,每隔2nm测吸光度一次。每测一次波长必须重新校正零点,再测吸光度。以入射光波长为横坐标,各相应的吸光度为纵坐标,分别绘出各物质的吸收光谱曲线。【注意事项】1.必须对所用的分光光度计进行波长校正。2.高铁氰化钾临用前配制,贮存于棕色瓶中。3.如果没有CO发生器,可用煤气替代。实验3荧光光度法测定β-N-乙酰氨基葡萄糖苷酶含量荧光分析(fluorimetry)是一种分子发光分析技术,是利用某些物质受紫外光照射后发出特有的荧光,藉此对物质进行定性和定量分析。用于荧光分析的仪器叫荧光计或荧光分光光度计。物质中的分子吸收光能可由基态跃迁至激发态,当从激发态返回基态时,发出【原理】比原激发光频率较低的荧光。激发光一般为紫外光,而发出的荧光多为可见光。对于一种浓度较小的荧光物质,在一定浓度范围内,其荧光强度与溶液浓度呈线性关系,据此可测定荧光物质的含量。在定量测定时,应选择荧光物质的最大激发波长(入ex)和最大荧光波长(入em),这就需要先获知激发光谱和荧光光谱。测定不同波长激发光时的荧光强度,以激发光波长为横坐标,荧光强度为纵坐标,所得曲线即表示激发光谱。荧光强度最大时激发光波长称为最大激发波长;与此类似,在最大激发波长时测定不同波长的荧光强度,以荧光波长为横坐标,荧光强度为纵坐标作图,所得曲线便是荧光光谱。荧光底物4-甲基伞形酮N-乙酰-β-D-氨基葡萄糖苷,在 β-N-乙酰氨基葡萄糖苷酶(NAG)作用下水解,释放出游离的4-甲基伞形酮(4-MU)。后者在碱性条件下变构,受激发产生荧光。根据荧光强度在标准曲线上查得4-MU含量,通过计算得出酶活力单位。【试剂】
(1) HbO2 溶液:取 Hb 溶液 4 滴,加蒸馏水 5ml。 (2) COHb 溶液:取Hb 溶液 3 滴,加蒸馏水 5ml,再加辛醇 1 滴,摇匀,用滴管通入CO 2~3min 呈樱桃红色。 (3) MHb 溶液:取 Hb 溶液 3 滴,加蒸馏水 5ml,加新鲜配制的 100g/L 高铁氰化钾 3 滴, 混匀,呈棕色,尽可能快比色。 3.测定 分别取上述溶液 3ml 盛于比色杯内,以蒸馏水作空白,在波长 470~650nm 范围 内,每隔 20nm 测吸光度一次,在接近吸收高峰时,每隔 2nm 测吸光度一次。每测一次波长, 必须重新校正零点,再测吸光度。以入射光波长为横坐标,各相应的吸光度为纵坐标,分别绘 出各物质的吸收光谱曲线。 【注意事项】 1.必须对所用的分光光度计进行波长校正。 2.高铁氰化钾临用前配制,贮存于棕色瓶中。 3.如果没有 CO 发生器,可用煤气替代。 实验 3 荧光光度法测定 β-N-乙酰氨基葡萄糖苷酶含量 荧光分析(fluorimetry)是一种分子发光分析技术,是利用某些物质受紫外光照射后发出特 有的荧光,藉此对物质进行定性和定量分析。用于荧光分析的仪器叫荧光计或荧光分光光度计。 【原理】 物质中的分子吸收光能可由基态跃迁至激发态,当从激发态返回基态时,发出 比原激发光频率较低的荧光。激发光一般为紫外光,而发出的荧光多为可见光。对于一种浓度 较小的荧光物质,在一定浓度范围内,其荧光强度与溶液浓度呈线性关系,据此可测定荧光物 质的含量。 在定量测定时,应选择荧光物质的最大激发波长(λex)和最大荧光波长(λem),这就需要先 获知激发光谱和荧光光谱。测定不同波长激发光时的荧光强度,以激发光波长为横坐标,荧光 强度为纵坐标,所得曲线即表示激发光谱。荧光强度最大时激发光波长称为最大激发波长;与 此类似,在最大激发波长时测定不同波长的荧光强度,以荧光波长为横坐标,荧光强度为纵坐 标作图,所得曲线便是荧光光谱。 荧光底物 4-甲基伞形酮 N-乙酰-β-D-氨基葡萄糖苷,在 β-N-乙酰氨基葡萄糖苷酶(NAG)作 用下水解,释放出游离的 4-甲基伞形酮(4-MU)。后者在碱性条件下变构,受激发产生荧光。根 据荧光强度在标准曲线上查得 4-MU 含量,通过计算得出酶活力单位。 【试剂】