
3、标准摩尔反应嫡变 标准摩尔反应熵变:当反应系统中各物质都处于标准 态,反应进度为1mol时,系统的熵变称为标准摩尔 反应嫡变,用符号△,S 表示。 对于0=∑yB 的化学反应来说,温度为T时的△,S9 为 8 △,SA(T)=∑yBSA(B,a,T) △,S册并不是实际反应过程中系统的熵变
• 3、标准摩尔反应熵变 • 标准摩尔反应熵变:当反应系统中各物质都处于标准 态,反应进度为1mol时,系统的熵变称为标准摩尔 反应熵变,用符号 表示。 • 对于 的化学反应来说,温度为T时的 为 • 并不是实际反应过程中系统的熵变。 O r m ∆ S 0 BB B = ∑v O r m ∆ S ( ) ( , , ) O O S T v Sm B T B ∆r m = ∑ B α O r m ∆ S
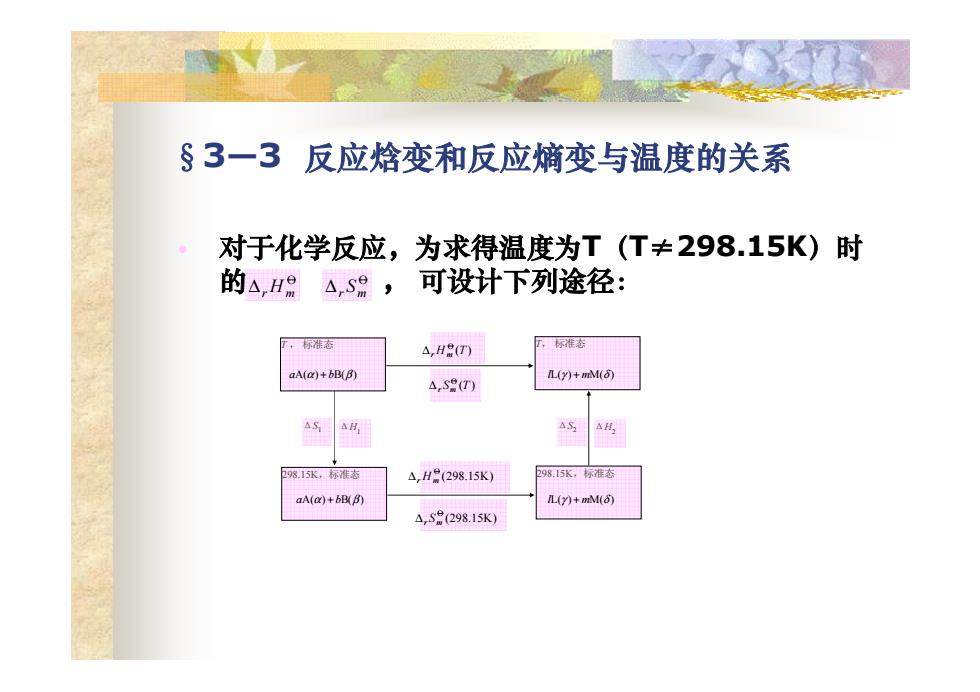
§3一3反应焓变和反应嫡变与温度的关系 对于化学反应,为求得温度为T(T≠298.15K)时 的△,H △,S,可设计下列途径: 丁,标准态 △,HR(T) 厂,标淮态 aA(a)+bB(B) L(y)+mM(6 A,S(T) AS AH, 298.15水,标准态 △,HR(298.15K) 298.15K,标准态 aA(a)+bBB) L(y)+mM( △S9(298.15K)
T , 标准态 T, 标准态 Δ ΔH1 S1 Δ ΔH2 S2 298.15K,标准态 298.15K,标准态 §3—3 反应焓变和反应熵变与温度的关系 • 对于化学反应,为求得温度为T(T≠298.15K)时 的 , 可设计下列途径: O ∆r Hm O ∆r Sm aA(α) + bB(β) lL(γ ) + mM(δ ) ( ) O ∆r Hm T ( ) O ∆r Sm T aA(α) + bB(β) lL(γ ) + mM(δ ) (298.15K) O ∆r Hm (298.15K) O ∆r Sm

1、反应焓变与温度的关系 △,HR(T)=△H1+△,HR(29815K)+△H2 AH,=,1 [@C4.四+bCn(B,Hr HC(+mC(M.5)T △,Cp.m=lCpm(L,Y)+nCp.m(M,δ)-aCp,m(Aa)-bCp,m(B,B) △,Cpm=∑'BCpm(B) △,H90=△,H929815K)+∫815△,Cpd7 此式即是反应焓变与温度的关系式,称为基尔霍夫公 式
• 1、反应焓变与温度的关系 • 此式即是反应焓变与温度的关系式,称为基尔霍夫公 式。 2 O 1 O ∆r Hm (T) = ∆H + ∆r Hm (29815K) + ∆H H lC L mC M T H aC A bC B T p m p m T p m p m T [ ( , ) ( , )]d [ ( , ) ( , )]d , , 298.15K 2 , , 298.15K 1 γ δ α β ∆ = + ∆ = + ∫ ∫ ( , ) ( , ) ( , ) ( , ) ∆rCp,m = lCp,m L γ + mCp,m M δ − aCp,m A α − bCp,m B β ( ) C , v Cp,m B B ∆r p m = ∑ B H T H rCp m T T r m r m ( ) (298.15K) d , 298.15K O O ∆ = ∆ + ∆ ∫

必须指出: (1)·若在T1到T2的温度范围内,物质相态发生变 化,则不能直接使用基尔霍夫公式。 例如,若已知反应H2(g,p)+I2(s)→2HI(g p)在298.15K的摩尔反应焓(T1) 4,HG) 要求反应H2(g,p)+I2(9,p)→2HI(9,p)在 400K的摩尔反应焓 △,H8(T) 400K H2(g,p)+12(gp)4) 2HI(g,p9)) △H L2(g,387K) △H △gH △H L(S,387K) △H 298.15K H2(g,p9)+L(S) △,H(T) 2H(g,p9)》
• 必须指出: • (1).若在T1到T2的温度范围内,物质相态发生变 化,则不能直接使用基尔霍夫公式。 • 例如,若已知反应 H2(g, pθ) + I2(s) → 2HI(g, pθ) 在298.15K的摩尔反应焓(T1) • 要求反应H2(g, pθ) + I2(g, pθ) → 2HI(g, pθ)在 400K的摩尔反应焓 O 1 ( ) ∆r m H T O 2 ( ) ∆r m H T ΔH2 I2(g,387K) ΔH1 ΔgsH ΔH5 I2(s,387K) ΔH4 298.15K H2(g, pθ) + I2(s) 2HI(g, pθ) 400K H2(g, pθ) + I2(g, pθ) 2HI(g, pθ) O 2 ( ) ∆r m H T O 1 ( ) ∆r m H T