Valine Leucine Isoleucine Methionine (Val,V) (Lev,L) (le,) (Met,M) H3C、 CH3 CH3 CH3 HgC SH一CH3 H>C 一CH3 H2C H CH2 H CH +H3N +H3N C00 HgN 5ee2p2f4n 2007 W.H.Freeman and Compary CH3 CH3 CH3 -CH3 CH2 CH2 H CH3 CH2 H- CH3 CH2 +H3N C00 *H2N- -C00 +H3N- c00 +H2N- C00 H H H Valine Leucine Isoleucine Methionine (Val,V) (Leu,L) (lle,I) (Met,M) Figure 2-8 part 3 Biochemistry,Sixth Edition 2007 W.H.Freeman and Compary 图28侧链是烷基的氨基酸。用*号标出了异亮氨酸的另一个手性碳原子。 H2 CH2 H2C CH2 C00 H2 H2 Proline (Pro,P) 图2.9脯氨酸的环状结构。氨基酸的侧链既与a-碳原子结合又与a-氨基N-原子结合。 有三个氨基酸的侧链有芳香环(图2.10)。苯丙氨酸是苯环替代丙氨酸的一个氢原子。酪 氨酸的芳香环有一个羟基。与其他氨基酸侧链呈化学惰性相比,酪氨酸的羟基有化学反应性。 色氨酸的吲引哚基团替代丙氨酸侧链的氢原子。吲引哚基团有的两个环融合在一起,一个环有N州 基团。苯丙氨酸是疏水氨基酸,但是酪氨酸和色氨酸疏水性弱,因为它们的侧链有羟基或州 基
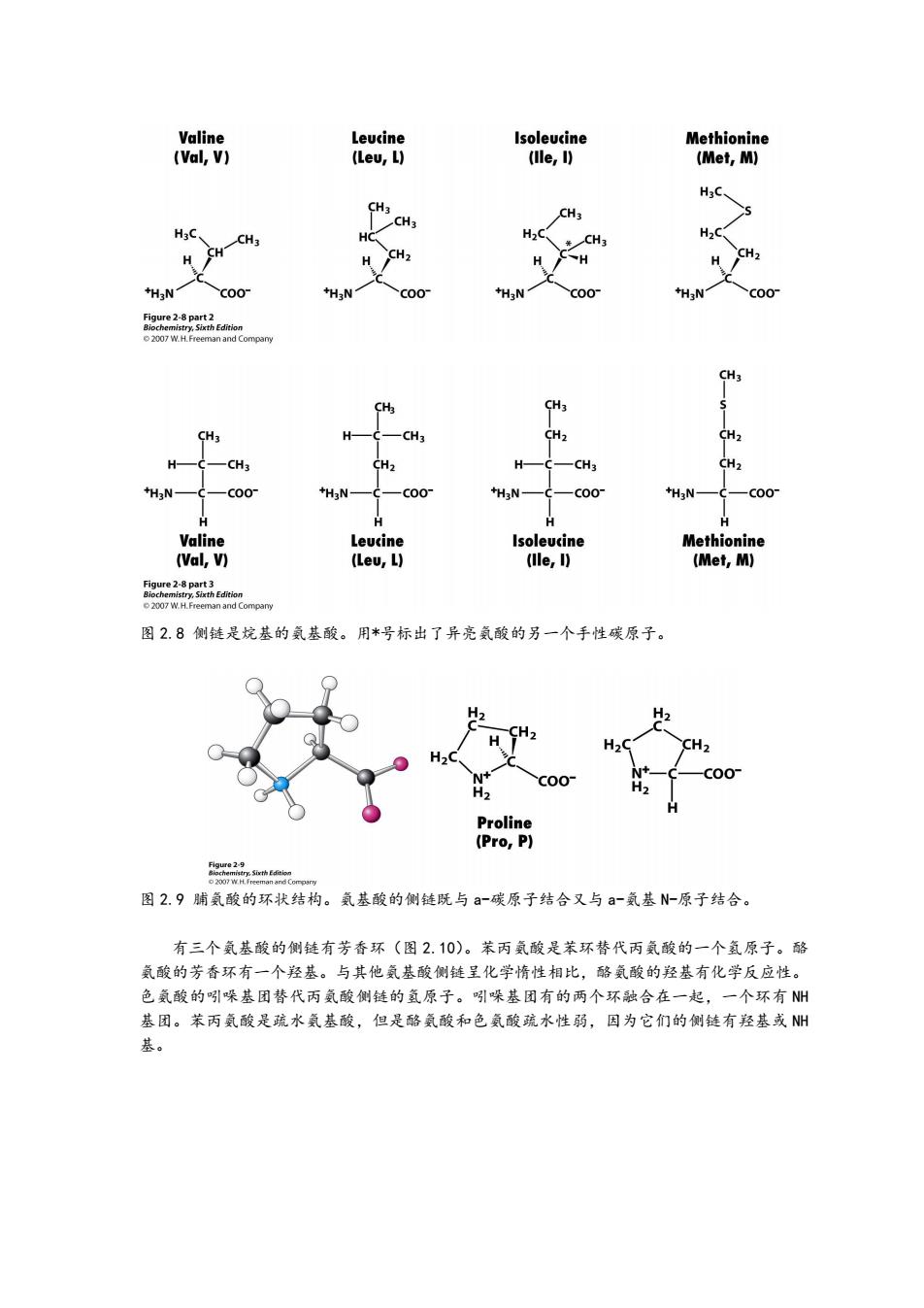
图 2.8 侧链是烷基的氨基酸。用*号标出了异亮氨酸的另一个手性碳原子。 图 2.9 脯氨酸的环状结构。氨基酸的侧链既与 a-碳原子结合又与 a-氨基 N-原子结合。 有三个氨基酸的侧链有芳香环(图 2.10)。苯丙氨酸是苯环替代丙氨酸的一个氢原子。酪 氨酸的芳香环有一个羟基。与其他氨基酸侧链呈化学惰性相比,酪氨酸的羟基有化学反应性。 色氨酸的吲哚基团替代丙氨酸侧链的氢原子。吲哚基团有的两个环融合在一起,一个环有 NH 基团。苯丙氨酸是疏水氨基酸,但是酪氨酸和色氨酸疏水性弱,因为它们的侧链有羟基或 NH 基
Phenylalanine Tyrosine Tryptophan (Phe,F) (yr,) (Trp,W) +H, C00 H HO HN CH2 CH2 CH, +H3N- C00 +H3N- C00 +H3N- coo H H H Phenylalanine Tyrosine Tryptophan (Phe,F) (Tyr,Y) (Trp,W) Figure 2-10 Biochemistry,Sixth Edition 2007 W.H.Freeman and Company 图2.10侧链有芳香基团的氨基酸。苯丙氨酸、酪氦酸和色氨酸有疏水性,但是色氨酸和酪氨 酸也有亲水性,因为它们的侧链有-N州基团或-OH基团。 有5种氨基酸的侧链有极性但不带电荷。其中两个氨基酸侧链有羟基与脂肪链相连(图 2.11)。丝氨酸是结合一个羟基的丙氨酸衍生物,而苏氨酸类似于顿氨酸,但用羟基替代了颉氨 酸的一个甲基。羟基的存在使苏氨酸和丝氨酸亲水,其反应活性比丙氨酸和颉氨酸大得多。与 异亮氨酸一样,苏氨酸也有第二个不对称碳原子,但蛋白质的苏氨酸只有一种构型
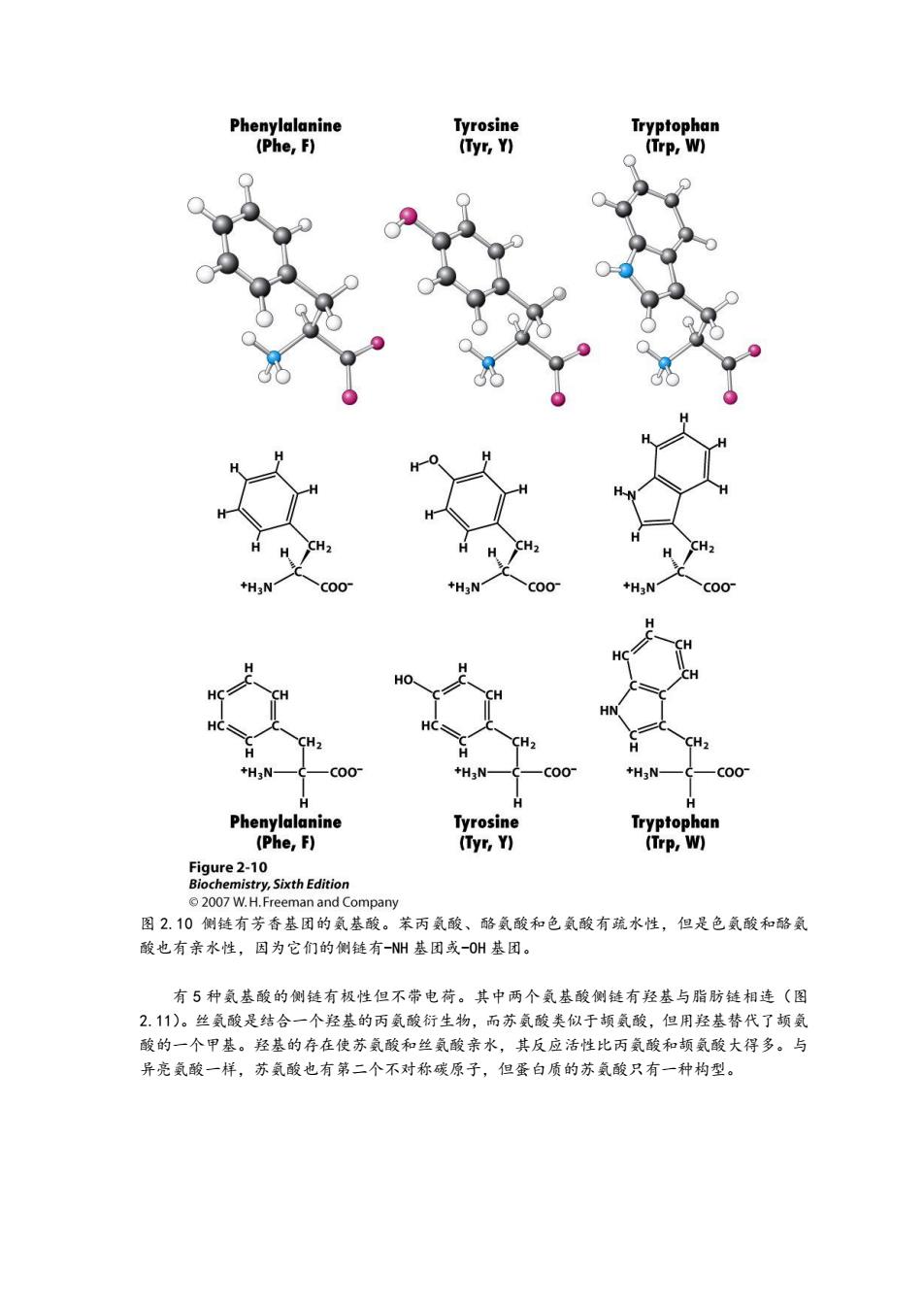
图 2.10 侧链有芳香基团的氨基酸。苯丙氨酸、酪氨酸和色氨酸有疏水性,但是色氨酸和酪氨 酸也有亲水性,因为它们的侧链有-NH 基团或-OH 基团。 有 5 种氨基酸的侧链有极性但不带电荷。其中两个氨基酸侧链有羟基与脂肪链相连(图 2.11)。丝氨酸是结合一个羟基的丙氨酸衍生物,而苏氨酸类似于颉氨酸,但用羟基替代了颉氨 酸的一个甲基。羟基的存在使苏氨酸和丝氨酸亲水,其反应活性比丙氨酸和颉氨酸大得多。与 异亮氨酸一样,苏氨酸也有第二个不对称碳原子,但蛋白质的苏氨酸只有一种构型
Serine Threonine (Ser,S) (Thr,T) H +H3N C00- +H3N C00 OH OH CH2 H —CH3 +H3N一 -C00 +H3N- -C00 H H Serine Threonine (Ser,S) (Thr,T) Figure 2-11 Biochemistry,Sixth Edition 2007 W.H.Freeman and Company 图2.11含有脂肪羟基的氨基酸。丝氨酸和苏氨酸侧链的羟基使这两种氨基酸亲水。苏氨酸的 另一个不对称碳原子用*标出。 谷氨酰胺和天冬酰胺的侧链也是极性但不带电荷。这两种氨基酸侧链的末端是酰胺而不是 羧酸(图2.12)。谷氨酰胺的侧链比天冬酰胺的侧链多一个亚甲基。 Glutamine (GIn,Q) - H义 H *H3N- NH NH .H3 +H]N- HgN- Asparagine Glutamine 《asn,N) (GIn,Q) 8aoy 图2.12天冬酰胺和谷氨酰胺的结构。这两种氨基酸是含有酰胺的极性氨基酸
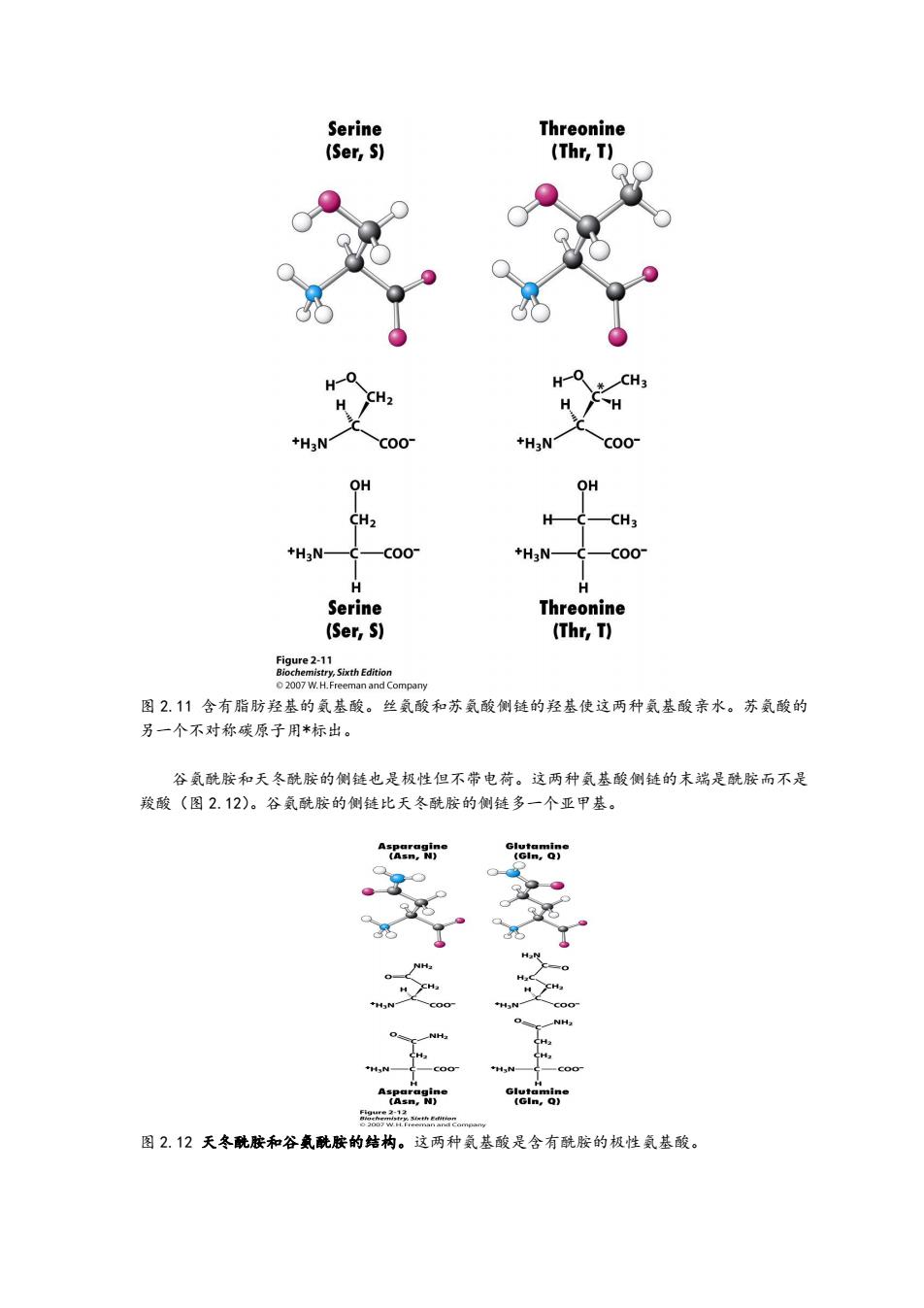
图 2.11 含有脂肪羟基的氨基酸。丝氨酸和苏氨酸侧链的羟基使这两种氨基酸亲水。苏氨酸的 另一个不对称碳原子用*标出。 谷氨酰胺和天冬酰胺的侧链也是极性但不带电荷。这两种氨基酸侧链的末端是酰胺而不是 羧酸(图 2.12)。谷氨酰胺的侧链比天冬酰胺的侧链多一个亚甲基。 图 2.12 天冬酰胺和谷氨酰胺的结构。这两种氨基酸是含有酰胺的极性氨基酸
半胱氨酸在结构上类似苏氨酸,但是用巯基替代了羟基(图2.13)。巯基比羟基活泼。一 对巯基靠近可以形成二硫键,稳定蛋白质的结构。后面我们将简短地讨论这种情况。 SH H-S H CH2 CH2 +H3N- coo +H3N Cysteine (Cys,C) 图2.13半胱氨酸的结构。 下面我们讨论带电荷的氨基酸,它们都是高度亲水的氨基酸。赖氨酸和精氨酸的侧链长, 在中性p州时侧链末端带正电荷。赖氨酸侧链的末瑞是氨基,精氨酸侧链的末端是胍基。组氨酸 含有咪唑基,咪唑基是芳香环,也能被质子化后带正电荷(图2.14)。 Lysine Arginine Histidine (Lys,K) (Arg,R) (His,H) +H:N NH3+ CH2 NH CH CH2 CH2 CH2 CH H3N- +H3N- H3N一 Lysine Arginine Histidine (Lys,K) (Arg,R) (His,H) Figure 2-14 Biochemistry,Sixth Edition 2007 W.H.Freeman and Company 图2.14碱性氨基酸:赖氨酸,精氨酸和组氨酸
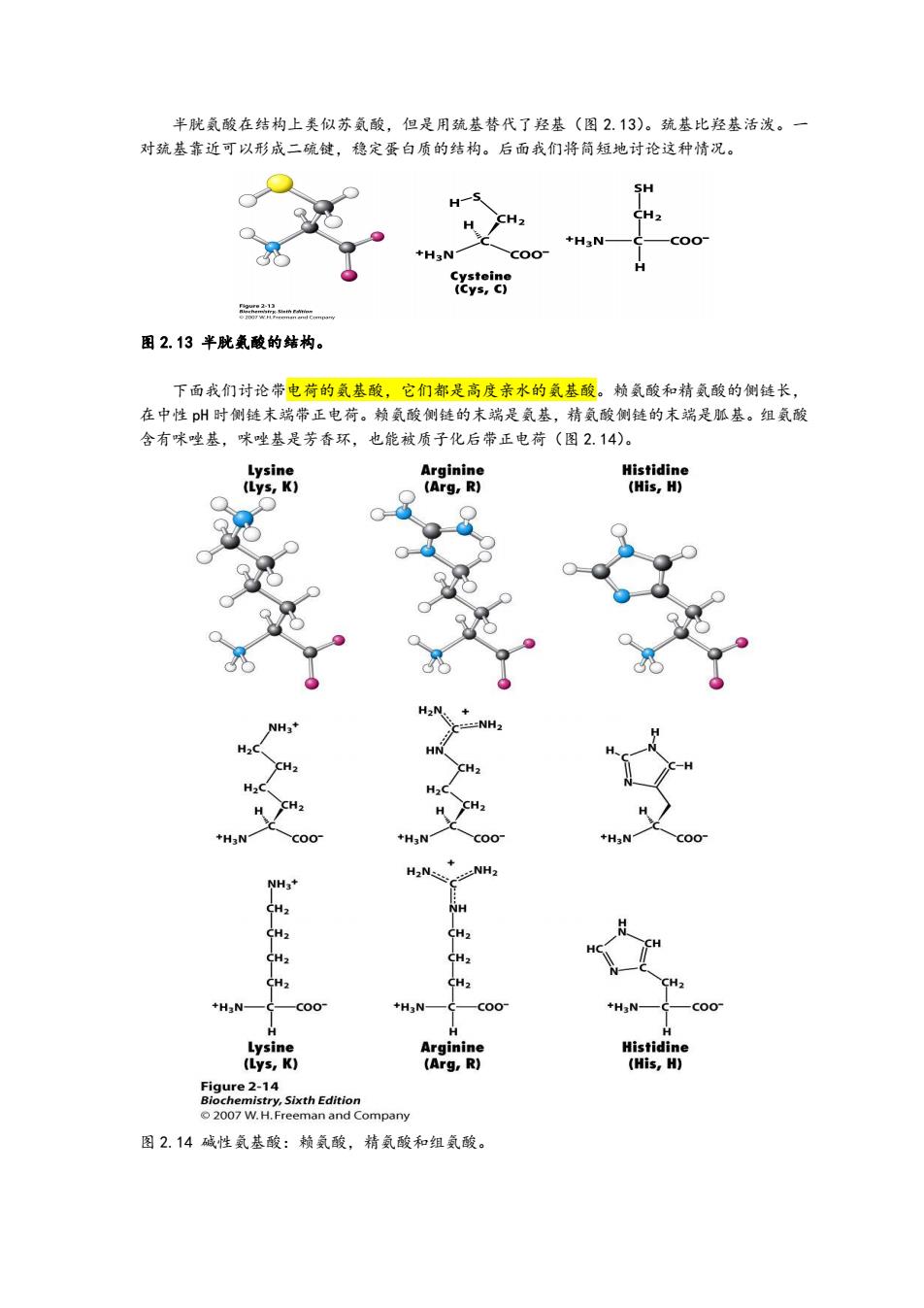
半胱氨酸在结构上类似苏氨酸,但是用巯基替代了羟基(图 2.13)。巯基比羟基活泼。一 对巯基靠近可以形成二硫键,稳定蛋白质的结构。后面我们将简短地讨论这种情况。 图 2.13 半胱氨酸的结构。 下面我们讨论带电荷的氨基酸,它们都是高度亲水的氨基酸。赖氨酸和精氨酸的侧链长, 在中性 pH 时侧链末端带正电荷。赖氨酸侧链的末端是氨基,精氨酸侧链的末端是胍基。组氨酸 含有咪唑基,咪唑基是芳香环,也能被质子化后带正电荷(图 2.14)。 图 2.14 碱性氨基酸:赖氨酸,精氨酸和组氨酸
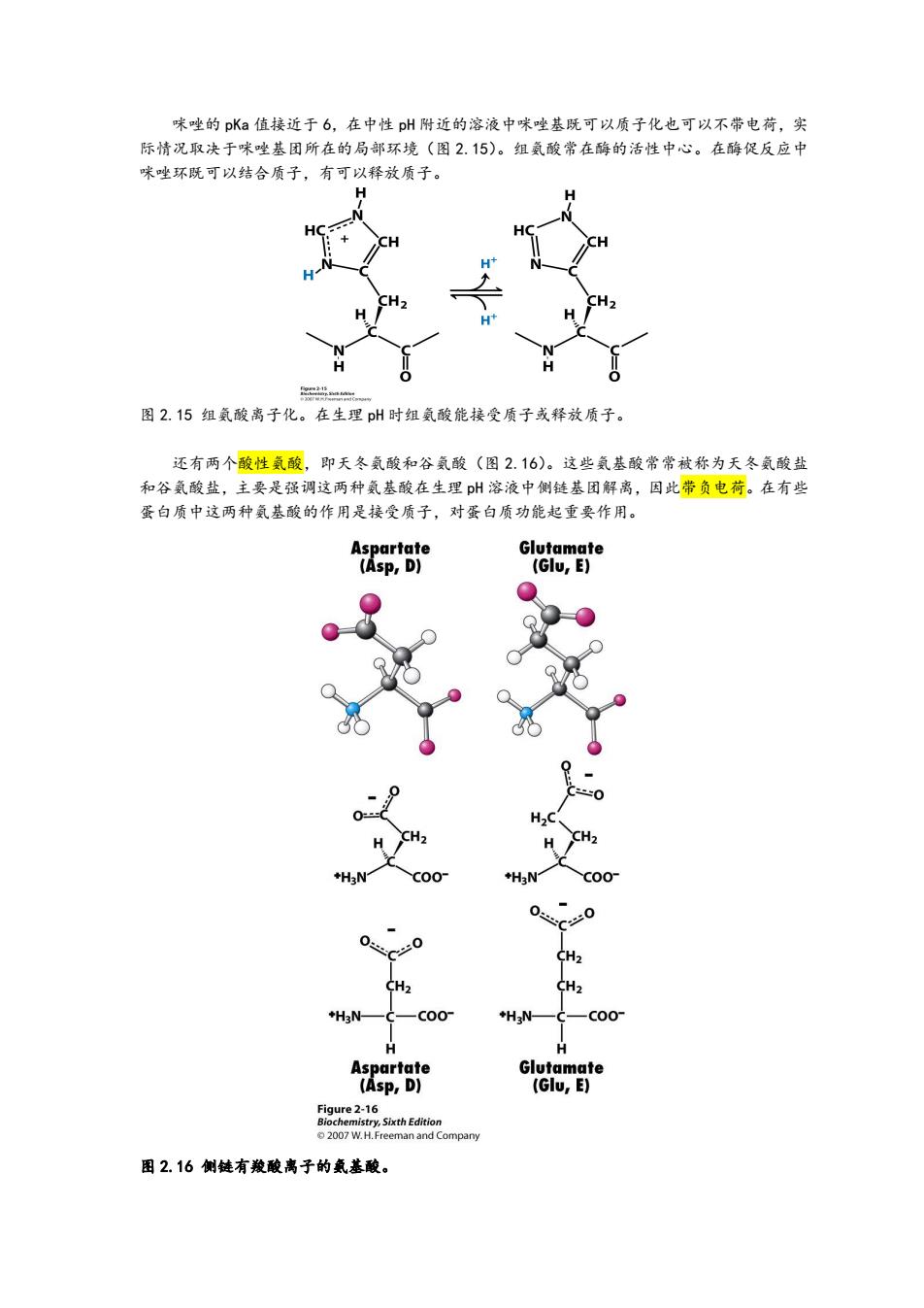
味唑的pKa值接近于6,在中性p州附近的溶液中咪唑基既可以质子化也可以不带电荷,实 际情况取决于咪唑基团所在的局部环境(图2.15)。组氨酸常在酶的活性中心。在酶促反应中 咪唑环既可以结合质子,有可以释放质子。 H 图2.15组氨酸离子化。在生理pH时组氨酸能接受质子或释放质子。 还有两个酸性氨酸,即天冬氨酸和谷氨酸(图2.16)。这些氨基酸常常被称为天冬氨酸盐 和谷氨酸盐,主要是强调这两种氨基酸在生理p州溶液中侧链基团解离,因此带负电荷。在有些 蛋白质中这两种氨基酸的作用是接受质子,对蛋白质功能起重要作用。 Aspartate Glutamate (Asp,D) (Glu,E) ℃0 CH2 CH2 CH2 +H3N- C00° +H3N- -C00 H Aspartate Glutamate (Asp,D) (Glu,E) Figure 2-16 Biochemistry,Sixth Edition 2007 W.H.Freeman and Company 图2.16侧链有羧酸离子的氨基酸
咪唑的 pKa 值接近于 6,在中性 pH 附近的溶液中咪唑基既可以质子化也可以不带电荷,实 际情况取决于咪唑基团所在的局部环境(图 2.15)。组氨酸常在酶的活性中心。在酶促反应中 咪唑环既可以结合质子,有可以释放质子。 图 2.15 组氨酸离子化。在生理 pH 时组氨酸能接受质子或释放质子。 还有两个酸性氨酸,即天冬氨酸和谷氨酸(图 2.16)。这些氨基酸常常被称为天冬氨酸盐 和谷氨酸盐,主要是强调这两种氨基酸在生理 pH 溶液中侧链基团解离,因此带负电荷。在有些 蛋白质中这两种氨基酸的作用是接受质子,对蛋白质功能起重要作用。 图 2.16 侧链有羧酸离子的氨基酸