
●i 酸和碱的中和反应 H+ H,O(aq)+OH(aq)=H,O(1)+H2O(1) H+ H,O(aq)+NH;(aq)=NH(aq)+H2O(1) H HAc(aq)+OH-(aq)=H,O(1)+Ac(aq) ● 盐的水解 H H'O) Vc_(sd)=HYc(sd)+OH_(sd) H* MH:(sd)+HO(I)=HO.(sd)+ MH(sd) H+ Cu(HO)+HO(1)=H,O"(aq)+Cu(OH)(HO)(aq) 11 上页下页 节首节尾
11 H O (aq) OH (aq) H O(l) H O(l) 3 2 2 H O (aq) NH (aq) NH (aq) H O(l) 3 3 4 2 HAc(aq) OH (aq) H O(l) Ac (aq) 2 ● 酸和碱的中和反应 H+ H+ H+ H O(l) Ac (aq) HAc(aq) OH (aq) 2 NH (aq) H O(l) H O (aq) NH (aq) 4 2 3 3 Cu(H O) H O(l) H O (aq) Cu(OH)(HO) (aq) 2 3 2 3 2 2 4 ● 盐的水解 H+ H+ H+

5.1.3布朗斯特平衡(Brφnsted's equilibrium) HB(ag)+HO(1 B-(ag)+H.O(ag) 该反应的标准平衡常数K叫酸性常数(Acidity constant), 也叫酸的电离常数(Acid ionization constant) {c(B-)/mol-dm-3){c(HO+)/mol-dm-3) {c(HB)/mol.dm-3) 下表列出一些常见酸的电离常数,使用时应该注意: 人9值越大,酸性越强,K大于1时的酸为强酸,K小于1的酸 为弱酸。 pK的值可跨越24个数量级,常数用pKg代替:pk=-lgPK 对二元和三元酸(如HS和HPO4)而.言,还有第二步和第三步质子 转移反应的相应常数 12 上页下页 节首节尾
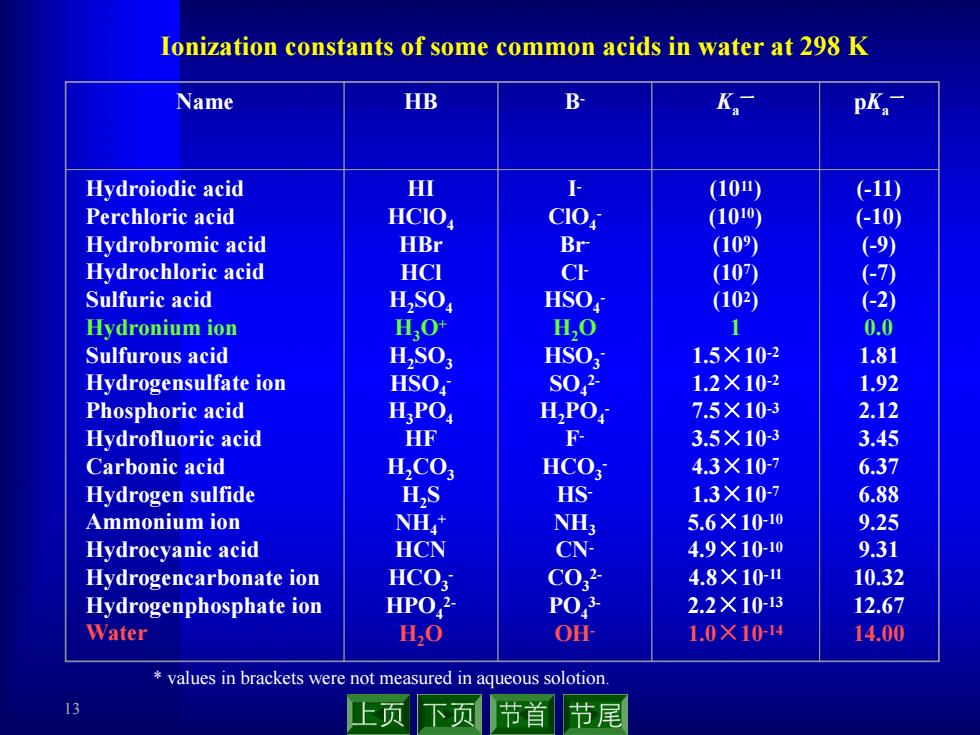
12 5.1.3 布朗斯特平衡 (Brfnsted’s equilibrium) 下表列出一些常见酸的电离常数,使用时应该注意: HB(aq) + H2O(l) B-(aq) + H3O+(aq) 该反应的标准平衡常数 叫酸性常数(Acidity constant), 也叫酸的电离常数(Acid ionization constant) θ Ka {c(B-)/mol·dm-3} {c(H3O+)/mol·dm-3} = ———————————————— {c(HB)/mol·dm-3} θ Ka ▲ 值越大,酸性越强. 大于1时的酸为强酸, 小于1的酸 为弱酸. θ Ka ▲ 对二元和三元酸(如H2S和H3PO4)而.言,还有第二步和第三步质子 转移反应的相应常数. ▲ 的值可跨越24个数量级,常数用 代替: θ Ka θ Ka θ a pK θ a pK θ a θ a pK lg pK
Ionization constants of some common acids in water at 298 K Name HB B K pK. Hydroiodic acid HI (10) (-11) Perchloric acid HCIO CIO (1010) (-10) Hydrobromic acid HBr Br (10) (9) Hydrochloric acid HCI (107) ←7) Sulfuric acid HSO HSO (102 (-2) Hydronium ion HO H,O 1 0.0 Sulfurous acid H,SO: HSO 1.5×10-2 1.81 Hydrogensulfate ion HSO S02 1.2×10-2 1.92 Phosphoric acid H.PO HPO 7.5×10-3 2.12 Hydrofluoric acid HF 3.5×103 3.45 Carbonic acid H,CO HCO 4.3×10-7 6.37 Hydrogen sulfide H,S HS 1.3X10-7 6.88 Ammonium ion NH NH; 5.6×10-10 9.25 Hydrocyanic acid HCN CN- 4.9×10-10 9.31 Hydrogencarbonate ion HCO; C032 4.8×10 10.32 Hydrogenphosphate ion HPO,2 P03 2.2×1013 12.67 Water H,O OH 1.0×1014 14.00 values in brackets were not measured in aqueous solotion 下页 节首 节尾
13 Ionization constants of some common acids in water at 298 K * values in brackets were not measured in aqueous solotion. Name HB B- Ka一 pKa一 Hydroiodic acid Perchloric acid Hydrobromic acid Hydrochloric acid Sulfuric acid Hydronium ion Sulfurous acid Hydrogensulfate ion Phosphoric acid Hydrofluoric acid Carbonic acid Hydrogen sulfide Ammonium ion Hydrocyanic acid Hydrogencarbonate ion Hydrogenphosphate ion Water HI HClO4 HBr HCl H2SO4 H3O+ H2SO3 HSO4 - H3PO4 HF H2CO3 H2S NH4 + HCN HCO3 - HPO4 2- H2O I - ClO4 - Br - Cl - HSO4 - H2O HSO3 - SO4 2- H2PO4 - F- HCO3 - HS- NH3 CN- CO3 2- PO4 3- OH- (1011) (1010) (109) (107) (102) 1 1.5×10-2 1.2×10-2 7.5×10-3 3.5×10-3 4.3×10-7 1.3×10-7 5.6×10-10 4.9×10-10 4.8×10-11 2.2×10-13 1.0×10-14 (-11) (-10) (-9) (-7) (-2) 0.0 1.81 1.92 2.12 3.45 6.37 6.88 9.25 9.31 10.32 12.67 14.00
质子转移发生在两个相同分子之间,其平衡常数又叫质子自递常数 例如: H2O(+H2O(OH-(aq)+HO+(aq) K={c(H3O)/mol-dm-3fc(OH)/mol-dm3) H内 1014 14 -1 MNaOH p Ko =-1g Kov 103 13 Basic 102 Ammonia (Household 不同温度时水的pK 1011 cleaner) 1010 10 109 9● T/K pKa 108 8■ -Blood 273 0.13×10-14 Neutral 107 7 Pure water Milk 283 0.36×10-14 106 6 291 0.74×10-14 105 295 1.00×10-14 10 103 -Vinegar 298 1.27×10-14 -Lemon juice Acidic 102 Stomach acid 313 3.80×10-14 10 333 12.60×10-14 -1 MHCI 14 上页 下页 节首 节尾
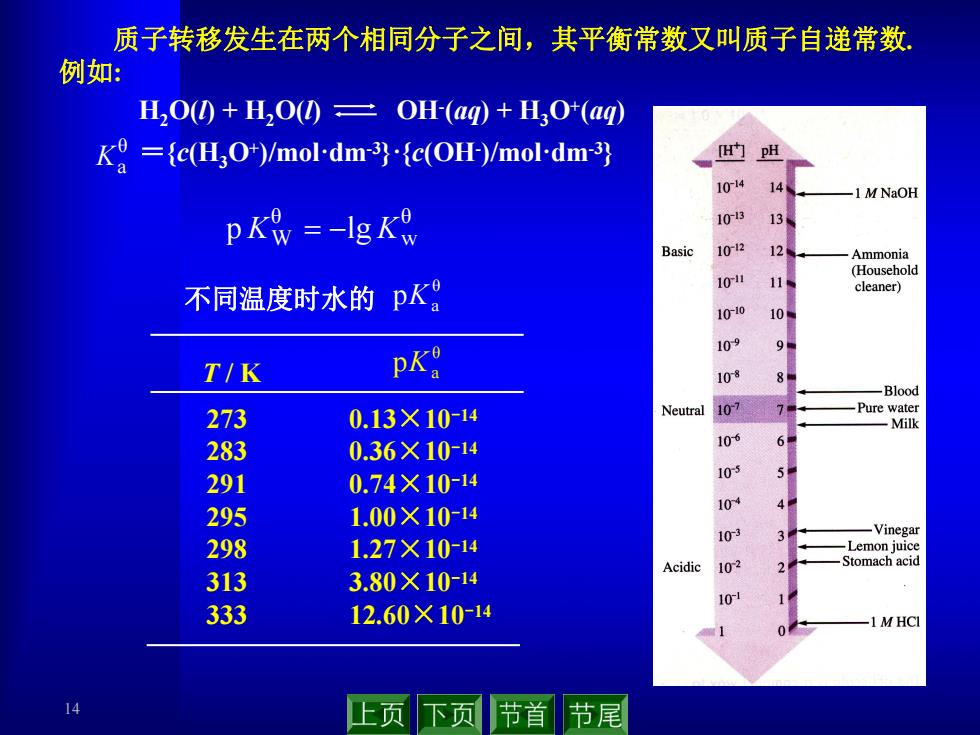
14 T / K θ a pK 273 283 291 295 298 313 333 0.13×10-14 0.36×10-14 0.74×10-14 1.00×10-14 1.27×10-14 3.80×10-14 12.60×10-14 质子转移发生在两个相同分子之间,其平衡常数又叫质子自递常数. 例如: H2O(l) + H2O(l) OH-(aq) + H3O+(aq) ={c(H3O+)/mol·dm-3}·{c(OH-)/mol·dm-3} θ w θ p KW lg K θ Ka 不同温度时水的 θ a pK
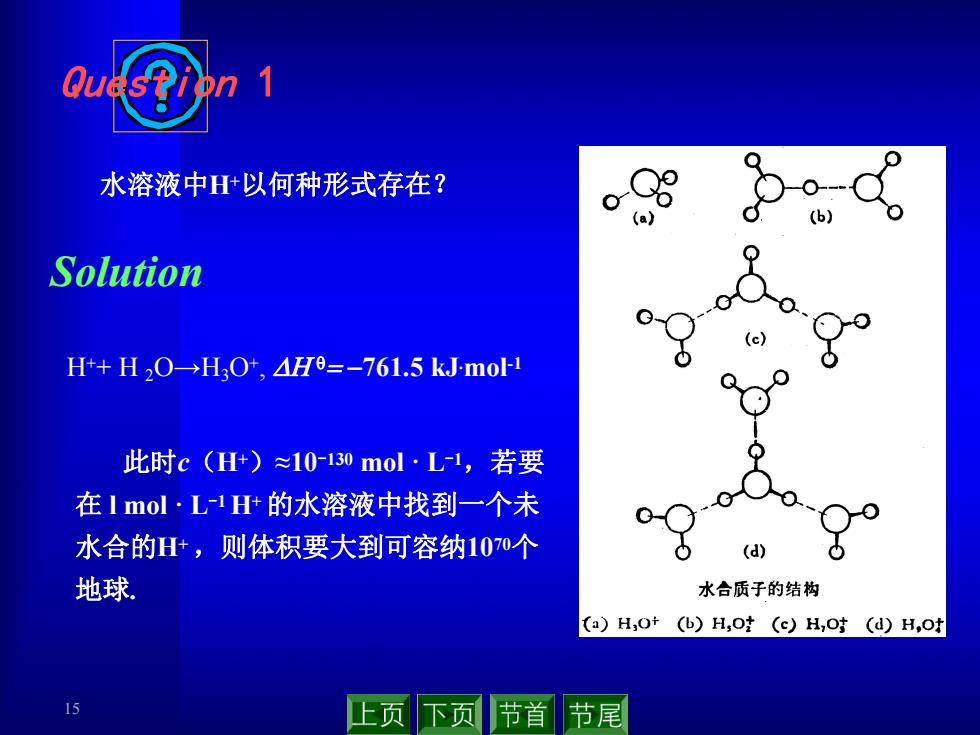
水溶液中以何种形式存在? C o-d (b) Solution H+H2O→H3O,△H=-761.5kJmo 此时c(+)≈10-130mol·L1,若要 在1mol·L-1H±的水溶液中找到一个未 水合的H,则体积要大到可容纳100个 ca) 地球 水合质子的结构 (a)H,O+(b)H,o (c)H,o (d)H,o 15 一页 下页 节首 节尾
15 此时c(H+)≈10-130 mol · L-1,若要 在 l mol · L-1 H+的水溶液中找到一个未 水合的H+ ,则体积要大到可容纳1070个 地球. H++ H 2O→H3O+ , DH q 761.5 kJ.mol -1 水溶液中H+以何种形式存在? Solution Question 1