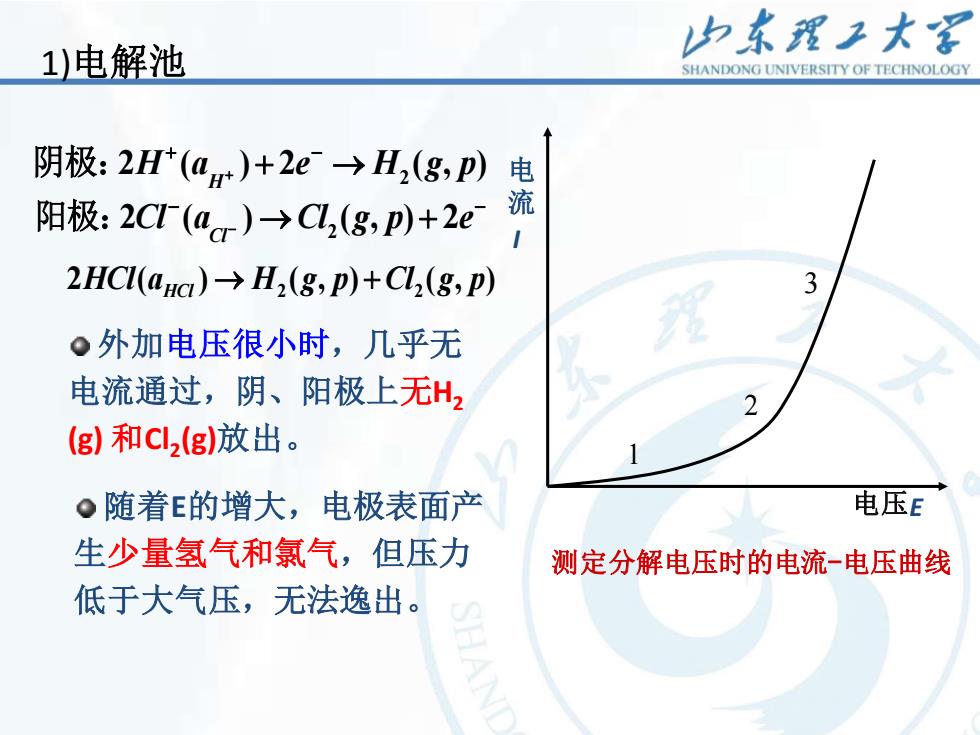
归东理工大 1)电解池 SHANDONG UNIVERSITY OF TECHNOLOGY 阴极:2H+(a)+2e→H,(g,p))电 阳极:2CT(ao)-→C,(g,p)+2e 2HCI(arc)>H2(g,p)+Cl2(g,p) 。外加电压很小时,几乎无 电流通过,阴、阳极上无H2 (g和Cl2(g)放出。 。随着E的增大,电极表面产 电压E 生少量氢气和氯气,但压力 测定分解电压时的电流一电压曲线 低于大气压,无法逸出
7 外加电压很小时,几乎无 电流通过,阴、阳极上无H2 (g) 和Cl2 (g)放出。 随着E的增大,电极表面产 生少量氢气和氯气,但压力 低于大气压,无法逸出。 电 流 I 电压E 1 2 3 测定分解电压时的电流-电压曲线 2 2 ( ) 2 ( , ) H H a e H g p + + − 阴极: + →2 2 ( ) ( , ) 2 Cl Cl a Cl g p e − 阳极: − − → + 2 2 2 ( ) ( , ) ( , ) HCl a H g p Cl g p HCl → + 1)电解池
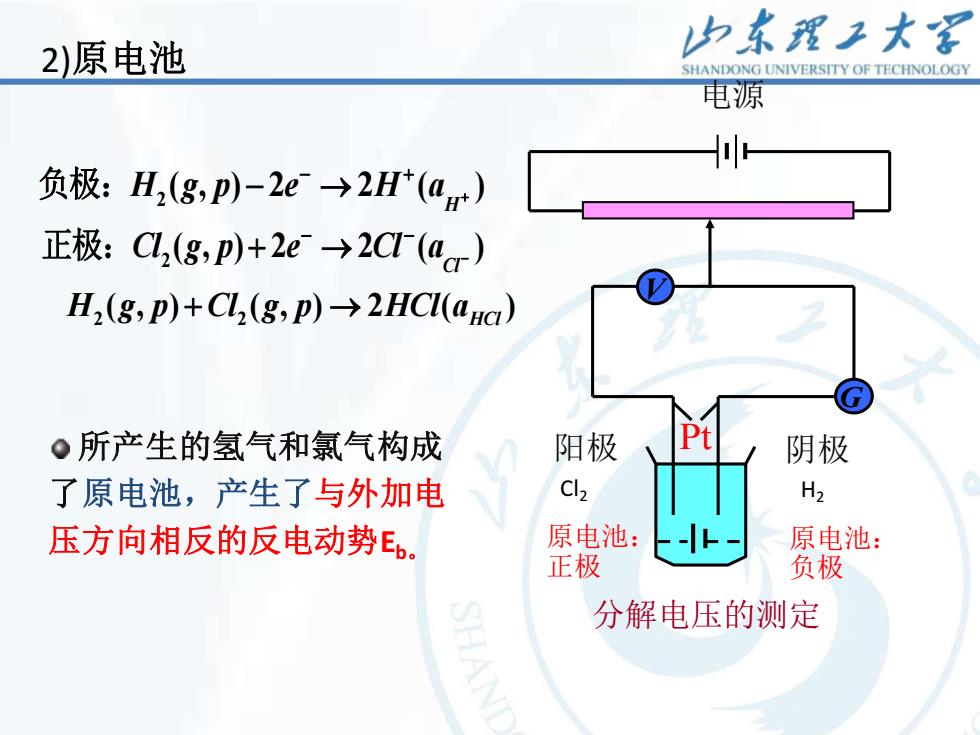
2)原电池 中东理子大 SHANDONG UNIVERSITY OF TECHNOLOGY 电源 负极:H2(g,p)-2e→2H*(a) 正极:CL,(g,p)+2e-→2C(a) H(g,p)+Ch(g,p)>2HCl(ana) 。所产生的氢气和氯气构成 阳极 阴极 了原电池,产生了与外加电 c H2 压方向相反的反电动势E。 原电池: 原电池: 正极 负极 分解电压的测定
8 电源 分解电压的测定 阳极 Pt 阴极 V G 所产生的氢气和氯气构成 了原电池,产生了与外加电 压方向相反的反电动势Eb。 2 ( , ) 2 2 ( ) H H g p e H a + − + 负极: − → 2 ( , ) 2 2 ( ) Cl Cl g p e Cl a − − − 正极: + → 2)原电池 2 2 ( , ) ( , ) 2 ( ) H g p Cl g p HCl aHCl + → Cl2 H2 原电池: 正极 原电池: 负极
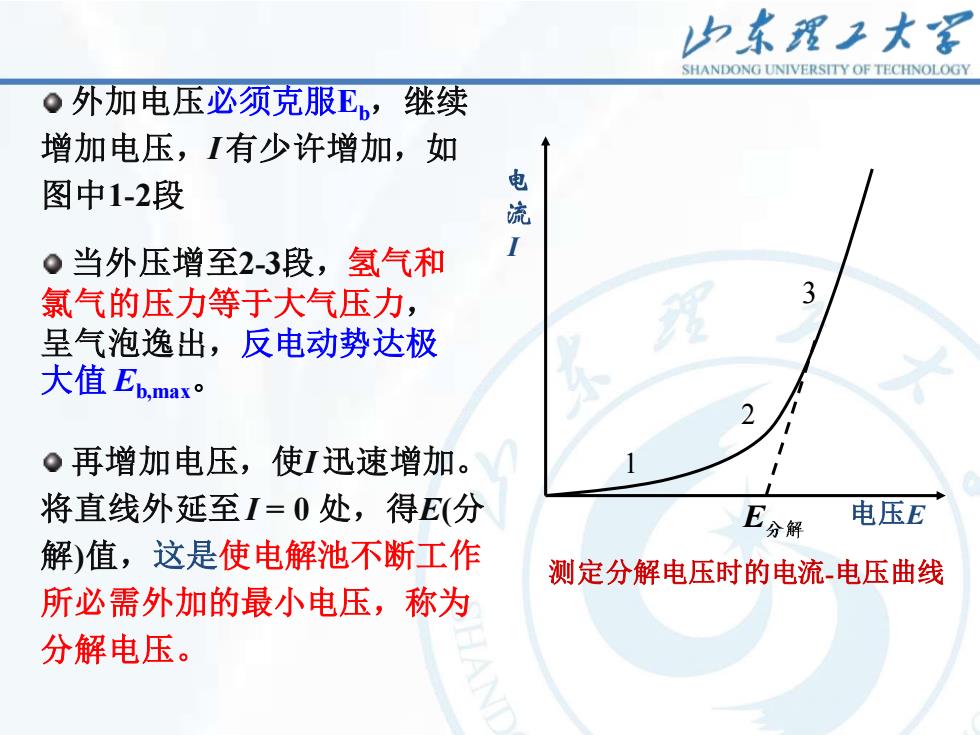
归东理工大 SHANDONG UNIVERSITY OF TECHNOLOGY 。外加电压必须克服E,继续 增加电压,有少许增加,如 图中1-2段 流 。当外压增至2-3段,氢气和 氯气的压力等于大气压力, 3 呈气泡逸出,反电动势达极 大值Eb,maxo Q再增加电压,使I迅速增加。 将直线外延至I=0处,得E(分 E分解 电压E 解)值,这是使电解池不断工作 测定分解电压时的电流电压曲线 所必需外加的最小电压,称为 分解电压
9 当外压增至2-3段,氢气和 氯气的压力等于大气压力, 呈气泡逸出,反电动势达极 大值 Eb,max。 再增加电压,使I 迅速增加。 将直线外延至I = 0 处,得E(分 解)值,这是使电解池不断工作 所必需外加的最小电压,称为 分解电压。 E I 电压E 1 2 3 测定分解电压时的电流-电压曲线 外加电压必须克服Eb,继续 增加电压,I 有少许增加,如 图中1-2段
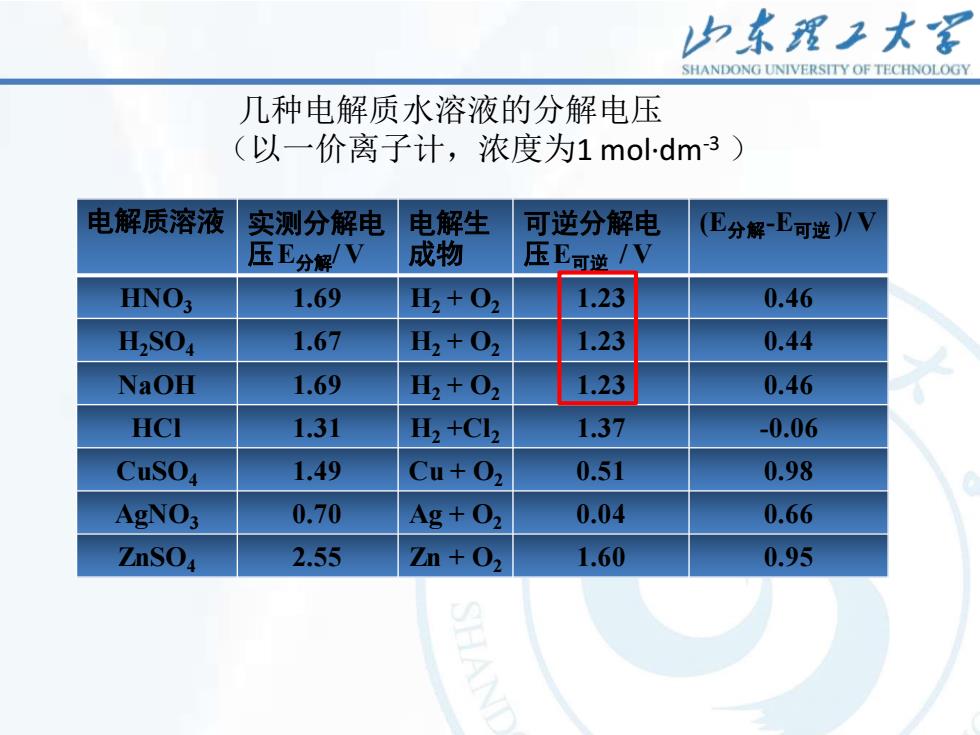
归东理王大 SHANDONG UNIVERSITY OF TECHNOLOGY 几种电解质水溶液的分解电压 (以一价离子计,浓度为1 mol-dm3) 电解质溶液 实测分解电 电解生 可逆分解电 (E分解-E可逆/V 压E分解V 成物 压E可逆/V HNO3 1.69 H2+02 1.23 0.46 H2S04 1.67 H2+02 1.23 0.44 NaOH 1.69 H2+02 1.23 0.46 HCI 1.31 H2+C2 1.37 -0.06 CuSO4 1.49 Cu+02 0.51 0.98 AgNO3 0.70 Ag+02 0.04 0.66 ZnSO 2.55 Zn+02 1.60 0.95
10 几种电解质水溶液的分解电压 (以一价离子计,浓度为1 mol·dm-3 ) 电解质溶液 实测分解电 压E分解/ V 电解生 成物 可逆分解电 压E可逆 / V (E分解-E可逆 )/ V HNO3 1.69 H2 + O2 1.23 0.46 H2SO4 1.67 H2 + O2 1.23 0.44 NaOH 1.69 H2 + O2 1.23 0.46 HCl 1.31 H2 +Cl2 1.37 -0.06 CuSO4 1.49 Cu + O2 0.51 0.98 AgNO3 0.70 Ag + O2 0.04 0.66 ZnSO4 2.55 Zn + O2 1.60 0.95

口东理王大 3.实际分解电压 SHANDONG UNIVERSITY OF TECHNOLOGY 要使电解池顺利地进行连续反应,除了克服作 为原电池时的可逆电动势外,还要克服由于极化在 阴、阳极上产生的超电势7阴和n卿,以及克服电 池电阻所产生的电位降R。这三者的加和就称为实 际分解电压。 E(分解)=E(可逆)+△E(不可逆)+IR △E(不可逆)=7)+7阴例) 显然分解电压的数值会随着通入电流强度的增加而 增加
11 E E E IR ( ) ( ) ( ) 分解 可逆 不可逆 = + + 要使电解池顺利地进行连续反应,除了克服作 为原电池时的可逆电动势外,还要克服由于极化在 阴、阳极上产生的超电势 和 ,以及克服电 池电阻所产生的电位降 。这三者的加和就称为实 际分解电压。 ( ) 阴 ( ) 阳 IR 显然分解电压的数值会随着通入电流强度的增加而 增加。 3.实际分解电压 = + E( ) ( ) ( ) 不可逆 阳 阴