
山东理工大客$9.5电动势产生的机理SHANDONGUNIVERSITYOFTECHNOLOGY电极与电解质溶液界面间电势差的形成接触电势强2液体接界电势*液接电势的计算公式电池电动势的产生2025/4/4
1 2025/4/4 1 §9.5 电动势产生的机理 电极与电解质溶液界面间电势差的形成 接触电势 液体接界电势 *液接电势的计算公式 电池电动势的产生
山东理工大客$ 9.5电动势产生的机理SHANDONGUNIVERSITYOFTECHNOLOGY电极与电解质溶液界面间电势差的形成负极|溶液1|溶液2|正极如: CuZn| ZnSO4CuSO|Cu界面电势差P扩散甲接触Ap-△p+ZnCuCusO4ZnSO42
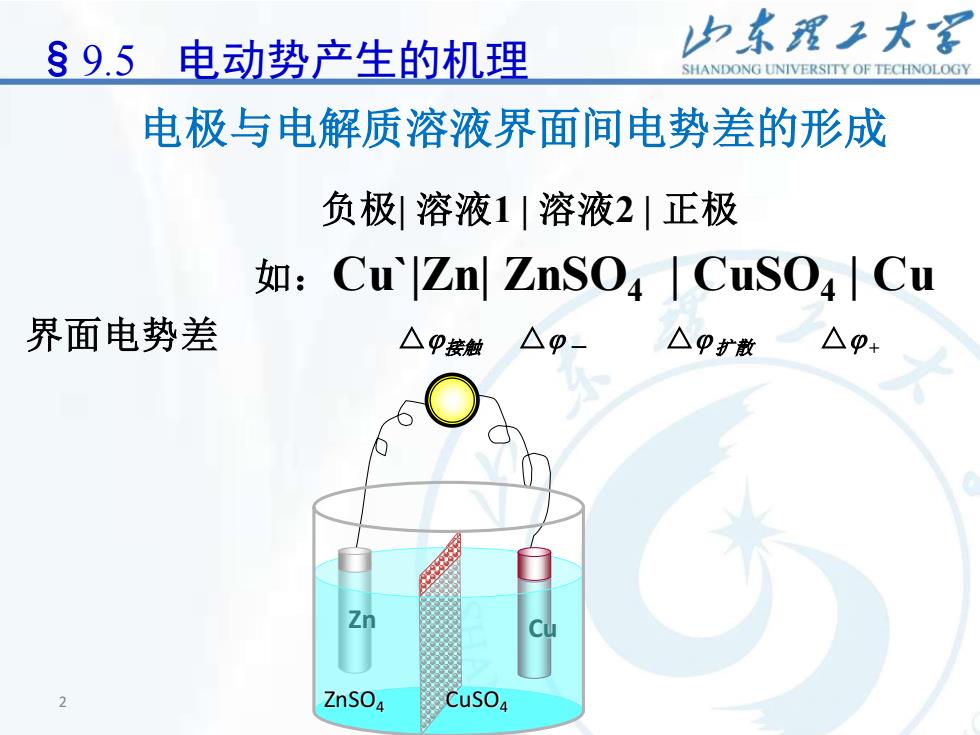
2 2 负极| 溶液1 | 溶液2 | 正极 如:Cu`|Zn| ZnSO4 | CuSO4 | Cu 界面电势差 △接触 △ - △ 扩散 △ + Cu Zn ZnSO4 CuSO4 §9.5 电动势产生的机理 电极与电解质溶液界面间电势差的形成
山东理工大客$ 9.5电动势产生的机理SHANDONGUNIVERSITYOFTECHNOLOGY电极与电解质溶液界面间电势差的形成双电层形成原因:两相化学势不等,如u,(Zn2+)>μu(Zn2+)金属①Zn2+进入溶液,在电极表面留下负电荷②当u,(Zn2+)= u(Zn2+)后,电极表面负电荷不再增加,Zn→Zn?+,和Zn2+→Zn达动态平衡;溶液③电极表面的电荷层与溶液中多余的反号离子层形成了双电层。+++++++++++++++电极①正离子受到电极表面负电荷的吸引,排板表面列在电极表面附近;②部分正离子由于热运动而分散在电极表面附近。3
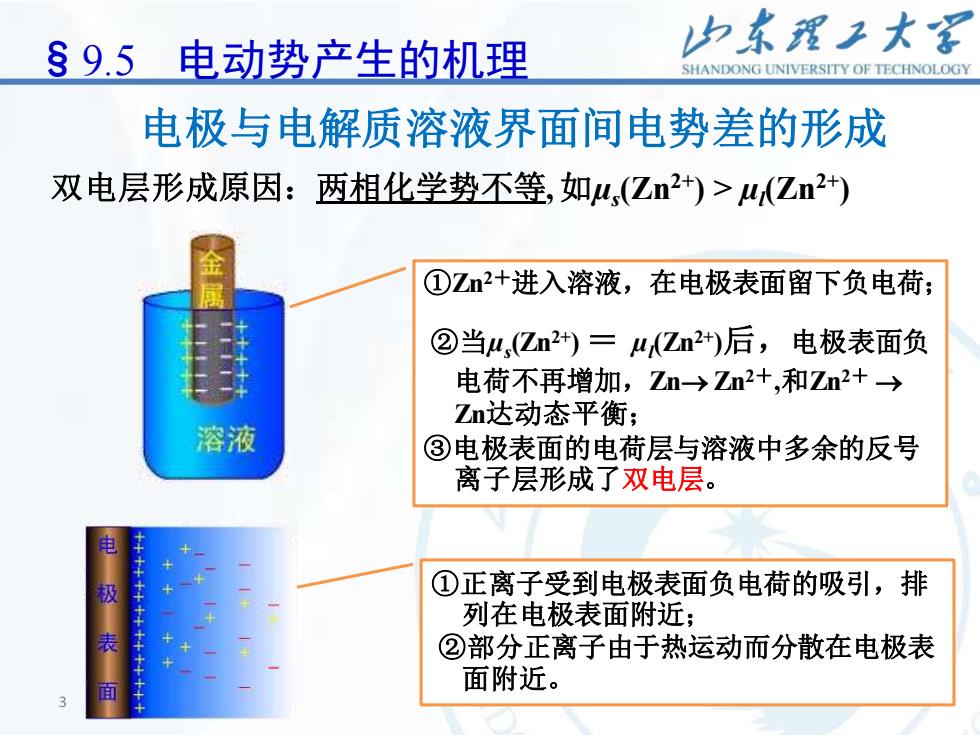
3 3 ①Zn2+进入溶液,在电极表面留下负电荷; ②当µs (Zn2+) = µl (Zn2+)后,电极表面负 电荷不再增加,Zn→ Zn2+ ,和Zn2+ → Zn达动态平衡; ③电极表面的电荷层与溶液中多余的反号 离子层形成了双电层。 双电层形成原因:两相化学势不等, 如µs (Zn2+) > µl (Zn2+) §9.5 电动势产生的机理 电极与电解质溶液界面间电势差的形成 ①正离子受到电极表面负电荷的吸引,排 列在电极表面附近; ②部分正离子由于热运动而分散在电极表 面附近
山东理工大客$9.5电动势产生的机理SHANDONGUNIVERSITYOFTECHNOLOGY电极与电解质溶液界面间电势差的形成+在金属与溶液的界面上G由于正、负离子静电吸引和+热运动两种效应的结果,溶液中的反离子只有一部分紧一密地排在固体表面附近,相距约一、二个离子厚度称为d:紧密层厚度~10-10mS:分散层厚度10-10~10-6m紧密层;与溶液的浓度、金属所带电另一部分离子按一定的荷与温度等有关:浓度梯度扩散到本体溶液中,称为扩散层浓度越大,8越小2025/4/44
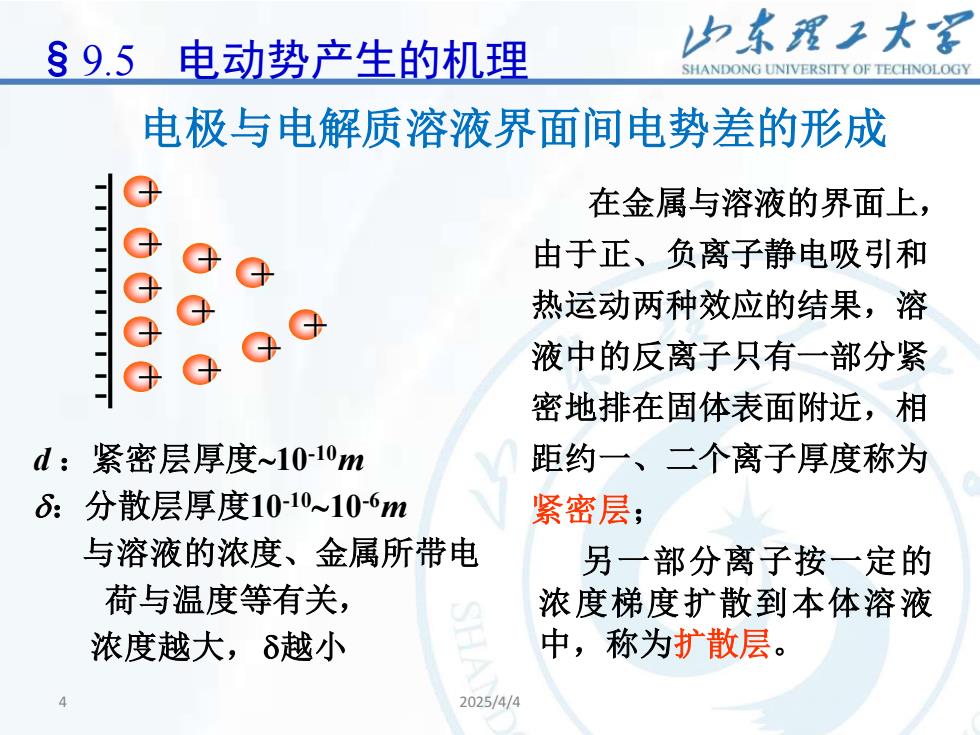
4 2025/4/4 4 在金属与溶液的界面上, 由于正、负离子静电吸引和 热运动两种效应的结果,溶 液中的反离子只有一部分紧 密地排在固体表面附近,相 距约一、二个离子厚度称为 紧密层; 另一部分离子按一定的 浓度梯度扩散到本体溶液 中,称为扩散层。 电极与电解质溶液界面间电势差的形成 §9.5 电动势产生的机理 d :紧密层厚度10-10m :分散层厚度10-1010-6m 与溶液的浓度、金属所带电 荷与温度等有关, 浓度越大,越小 + - - - - - - - - - - - + + + + + + + + + +
山东理工大客$ 9.5电动势产生的机理SHANDONGUNIVERSITY OFTECHNOLOGY电极与电解质溶液界面间电势差的形成+金属表面与溶液本体之间的电势差即+为界面电势差2电极电势PM:△qP:本体溶液电势Ae△?:界面电势差。与电极的种类,温度,离子浓度有关。△P2Φ1= / m-ii+25d
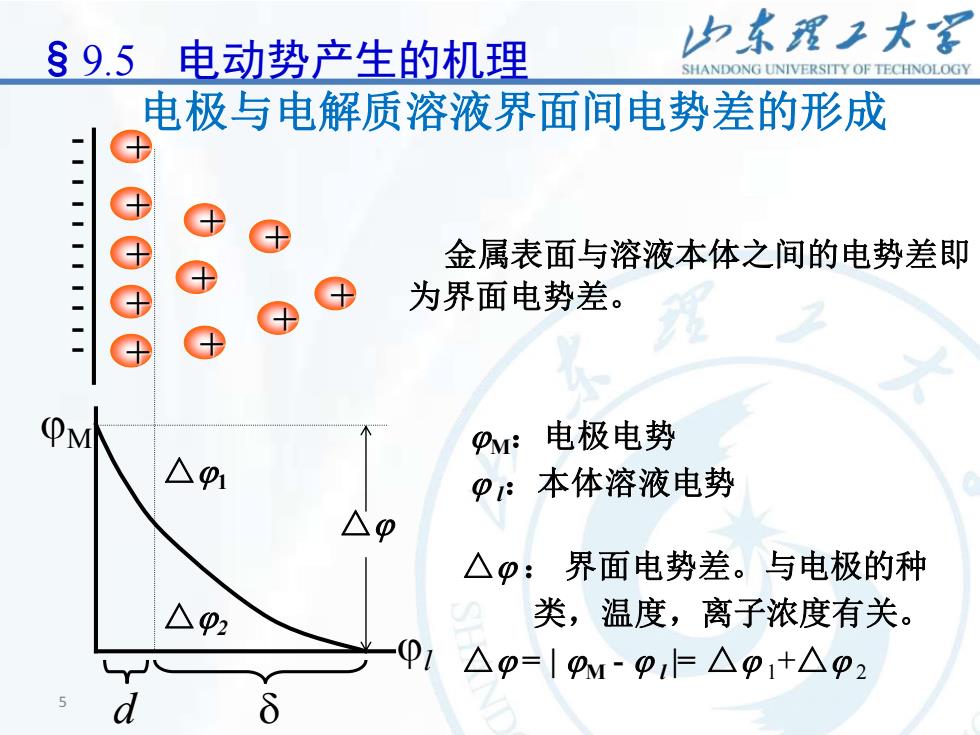
5 5 + - - - - - - - - - - - + + + + + + + + + + M l △1 △2 d △ M:电极电势 l:本体溶液电势 电极与电解质溶液界面间电势差的形成 §9.5 电动势产生的机理 金属表面与溶液本体之间的电势差即 为界面电势差。 △ : 界面电势差。与电极的种 类,温度,离子浓度有关。 △ = | M - l |= △ 1+△ 2