
s 12.9催化反应动力学催化剂与催化作用均相酸碱催化络合催化酶催化反应2025/4/4
2025/4/4 §12.9 催化反应动力学 催化剂与催化作用 均相酸碱催化 酶催化反应 络合催化

催化剂与催化作用可明显改变反应速率,而本身在反应前后数量和化学性质保持不变的物质称为催化剂。可加速反应速率的,称为正催化剂;可降低反应速率的,称为阻化剂或负催化剂工业上大部分用的是正催化剂。而塑料和橡胶中的防老剂,金属防腐用的缓蚀剂和汽油燃烧中的防爆震剂等都是阻化剂注意:催化剂是参与反应的,其物理性质有可能改变。2025/4/4
2025/4/4 催化剂与催化作用 可明显改变反应速率,而本身在反应前后数量和化学 性质保持不变的物质称为催化剂。 可加速反应速率的,称为正催化剂; 可降低反应速率的,称为阻化剂或负催化剂。 工业上大部分用的是正催化剂。而塑料和橡胶中的 防老剂,金属防腐用的缓蚀剂和汽油燃烧中的防爆震剂 等都是阻化剂 注意:催化剂是参与反应的,其物理性质有可能改变

催化剂与催化作用催化剂与反应系统处在同一个相的称为均相催化如用硫酸作催化剂使乙醇和乙酸生成乙酸乙酯的反应是液相均相反应。催化剂与反应系统处在不同相的称为多相催化。如用固体超强酸作催化剂使乙醇和乙酸生成乙酸乙酯的反应是多相催化反应。石油裂解、直链烷烃芳构化等反应也是多相催化反应。2025/4/4
2025/4/4 催化剂与反应系统处在同一个相的称为均相催化。 石油裂解、直链烷烃芳构化等反应也是多相催化反应。 如用硫酸作催化剂使乙醇和乙酸生成乙酸乙酯的反应 是液相均相反应。 催化剂与反应系统处在不同相的称为多相催化。 如用固体超强酸作催化剂使乙醇和乙酸生成乙酸乙酯 的反应是多相催化反应。 催化剂与催化作用

催化剂与催化作用ko→AB设某基元反应为A+B活化能为E。加入催化剂K后的反应机理为kAK(1) A+K(快平衡)k2ksAK+B>AB+K(2) (慢反应)用平衡假设法推导速率方程k.d[AB][AK][A][K]k,[AK][B]r=dt得:k,kk,k.[K]K[K][A][B] = k[A][B]k2k22025/4/4
2025/4/4 设某基元反应为 A B AB 0k + ⎯⎯→ 活化能为 E0 加入催化剂 K 后的反应机理为 (快平衡) 3 (2) AK B AB K k + ⎯⎯→ + (慢反应) 用平衡假设法推导速率方程 3 d[AB] [AK][B] dt r k = = 1 2 [AK] [A][K] k k = 得: 1 3 2 [K][A][B] k k r k = = k[A][B] 1 3 2 [K] k k k k = 催化剂与催化作用
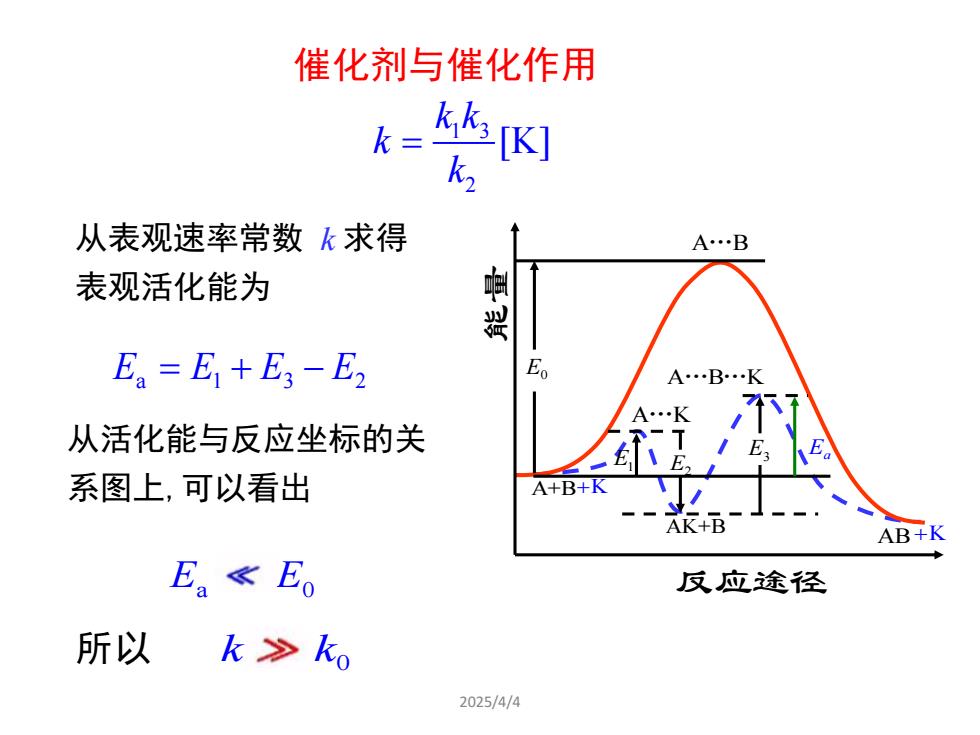
催化剂与催化作用k,k[K]k =k2从表观速率常数k求得A.B鲁骐表观活化能为EoE, = E, + E - E,A...B...K不A..K从活化能与反应坐标的关-TV/EsE1E系图上,可以看出A+B+K业AK+BAB+KE.< Eo反应途径所以k>ko2025/4/4
2025/4/4 1 3 2 [K] k k k k = 从表观速率常数 k 求得 表观活化能为 E E E E a 1 3 2 = + − 从活化能与反应坐标的关 系图上,可以看出 E E a 0 所以 k k0 A B . A B K . . A K . A+B AK+B AB E1 反应途径 能量 E0 E2 E3 Ea +K +K 催化剂与催化作用