
导航 课前·基础认知 一、物质的量及其单位 1.定义:物质的量是一个 ,表示含有 的集合体。符号为 2.单位:单位为 ,简称摩,符号为
导航 一、物质的量及其单位 1.定义:物质的量是一个 物理量 ,表示含有 一定数目粒 子 的集合体。符号为 n 。 2.单位:单位为 摩尔 ,简称摩,符号为 mol 。 课前·基础认知

导 3.衡量标准:国际上规定,1ol粒子集合体所含的粒子数约 为6.02×1023。 4.阿伏加德罗常数: 任何粒子的粒子数叫做阿伏 加德罗常数,符号为 ,通常用 表 示。 5.物质的量、阿伏加德罗常数与粒子数之间的关系: 。其中表示物质的量,N表示阿伏加德罗常数,N表 示
导航 3.衡量标准:国际上规定,1 mol粒子集合体所含的粒子数约 为6.02×1023 。 4.阿伏加德罗常数: 1 mol 任何粒子的粒子数叫做阿伏 加德罗常数,符号为 NA ,通常用 6.02×1023 mol-1 表 示。 5.物质的量、阿伏加德罗常数与粒子数之间的关系: n= 。其中n表示物质的量,NA表示阿伏加德罗常数,N表 示 粒子数 。 𝑵 𝑵𝐀

导航 微判断1(1)物质的量就是物质的质量。(×) (2)设N代表阿伏加德罗常数的值。2mol氧中所含氧原子 的个数为2NA·(×) (3)1 mol NH3所含原子数约是2.408×1024。(√) (4)物质的量是指物质所含粒子的数目。(×) (⑤)物质的量的单位一摩尔只适用于分子、原子和离子。 (X)
导航 微判断1(1)物质的量就是物质的质量。( ) (2)设NA代表阿伏加德罗常数的值。2 mol氧中所含氧原子 的个数为2NA。( ) (3)1 mol NH3所含原子数约是2.408×1024 。( ) (4)物质的量是指物质所含粒子的数目。( ) (5)物质的量的单位——摩尔只适用于分子、原子和离子。 ( ) × × √ × ×
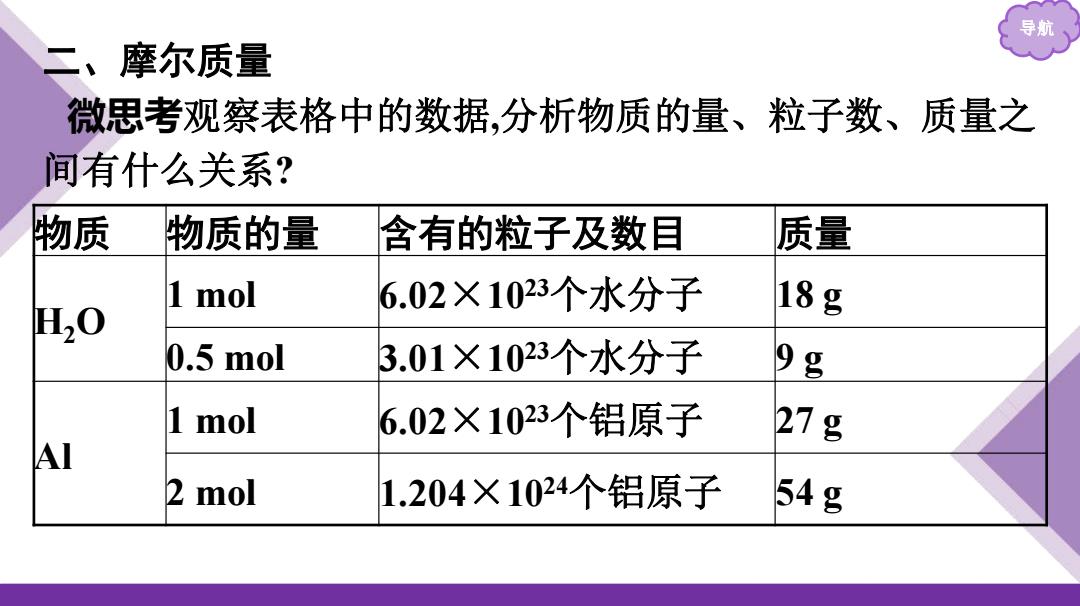
导 二、摩尔质量 微思考观察表格中的数据,分析物质的量、粒子数、质量之 间有什么关系? 物质 物质的量 含有的粒子及数目 质量 1 mol 6.02×1023个水分子 H20 18g 0.5 mol 3.01×1023个水分子 9g 1 mol 6.02×1023个铝原子 27g A 2 mol 1.204×1024个铝原子 54g
导航 二、摩尔质量 微思考观察表格中的数据,分析物质的量、粒子数、质量之 间有什么关系? 物质 物质的量 含有的粒子及数目 质量 H2O 1 mol 6.02×1023个水分子 18 g 0.5 mol 3.01×1023个水分子 9 g Al 1 mol 6.02×1023个铝原子 27 g 2 mol 1.204×1024个铝原子 54 g

导航 提示:1)1ol不同物质中所含的粒子数是相同的,但由于不 同粒子的质量不同,1m0l不同物质的质量也不同。 (2)1m0l任何粒子集合体都约含有6.02×1023个粒子;而1 0l任何粒子或物质的质量以克为单位时,其数值都与该粒子 的相对原子质量或相对分子质量相等
导航 提示:(1)1 mol不同物质中所含的粒子数是相同的,但由于不 同粒子的质量不同,1 mol不同物质的质量也不同。 (2)1 mol任何粒子集合体都约含有6.02×1023个粒子;而1 mol任何粒子或物质的质量以克为单位时,其数值都与该粒子 的相对原子质量或相对分子质量相等