§11.7绝热过程 一,绝热过程 系统在绝热过程中始终不与外界交换热量。 ·良好绝热材料包围的系统发生的过程 ·进行得较快,系统来不及和外界交换热量的过程 1.过程方程 对无限小的准静态绝热过程有 dA+dE=0◆pdV=-vCdT pV=vRT-pdv+Vdp=v RdT (Cy R)pdy+CrVdp=0
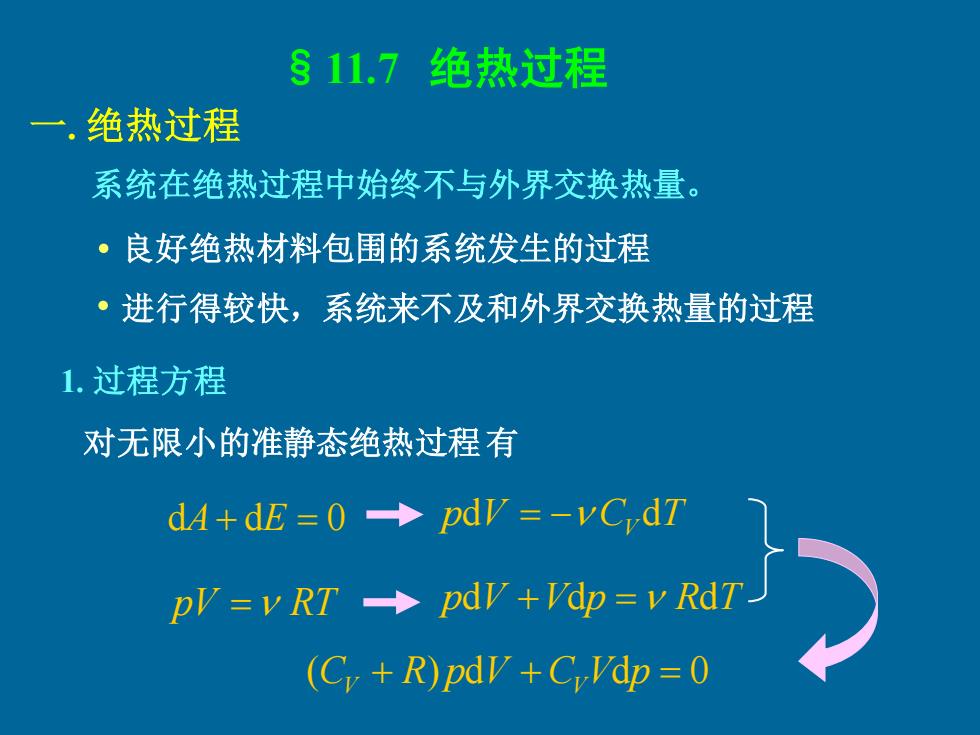
§11.7 绝热过程 一. 绝热过程 系统在绝热过程中始终不与外界交换热量。 良好绝热材料包围的系统发生的过程 进行得较快,系统来不及和外界交换热量的过程 1. 过程方程 对无限小的准静态绝热过程有 · · dA+ dE = 0 pdV = − CV dT pV = RT pdV +Vdp = RdT (C + R) pdV + C Vdp = 0 V V
=0 pl7 C p 利用上式和状态方程可得 TV-C, p-T C, 2.过程曲线 绝热线 pVr=C dp d 微分 等温线 pV C dp d 由于y>1,所以绝热线要比 等温线陡一些
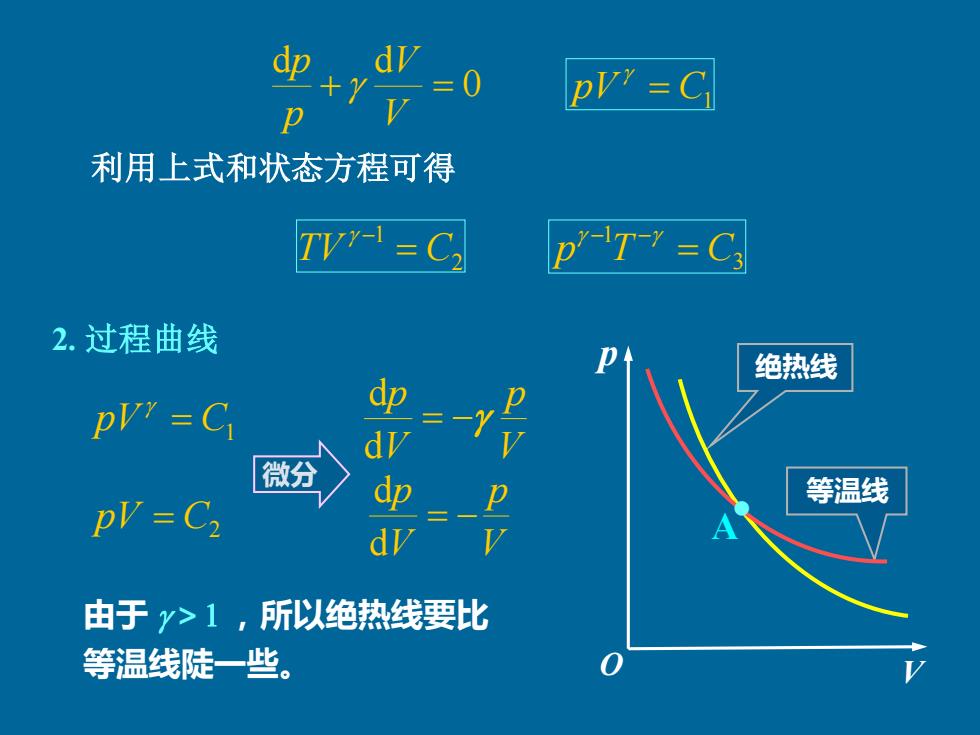
0 d d + = V V p p pV = C1 2 1 TV = C − 3 1 p T = C − − 利用上式和状态方程可得 2. 过程曲线 V p V p = − d d pV = C2 C1 pV = V p V p = − d d 微分 A 绝热线 等温线 由于 >1 ,所以绝热线要比 等温线陡一些。 • V p O

3.绝热过程中功的计算 A=-(E2-E)=-vC(T3-I) A=r=所p=,-p》 绝热过程中,理想气体不吸收热量,系统减少的内能,等 于其对外作功
绝热过程中 ,理想气体不吸收热量,系统减少的内能,等 于其对外作功 。 = = 2 1 2 1 d d 1 1 V V V V V V A p V pV ( ) 1 1 p1V1 − p2V2 − = 3. 绝热过程中功的计算 ( ) A = − E2 − E1 ( ) = − CV T2 −T1

例一定量氮气,其初始温度为300K,压强为1atm。将其绝热 压缩,使其体积变为初始体积的1/5。 求压缩后的压强和温度 解氮气是双原子分子 (7/5)7 C (5/2)5 根据绝热过程方程的p、V关系,有 7 p2=p,(W/W2)Y=1x55=9.52atm 根据绝热过程方程的T、V关系,有 T=T(W/VY=300×55=571K
一定量氮气,其初始温度为300K,压强为1atm。将其绝热 压缩,使其体积变为初始体积的1/5。 解 例 求 压缩后的压强和温度 ( ) 1 5 5 9.52atm 7 2 = 1 1 2 = = p p V V ( ) 300 5 571K 1 5 7 1 2 = 1 1 2 = = − − T T V V 5 7 (5 2) (7 5) = = = V p C C 根据绝热过程方程的p﹑V 关系,有 根据绝热过程方程的T﹑V 关系,有 氮气是双原子分子
例温度为25℃,压强为1atm的1mol刚性双原子分子理想气 体经等温过程体积膨胀至原来的3倍。 求()该过程中气体对外所作的功: (2)若气体经绝热过程体积膨胀至原来的3倍,气体对外所 作的功。 解(1)由等温过程可得 =r- =R71n=2.72×10J 2)根据绝热过程方程,有 37 T3=T(V/)Y1=192K
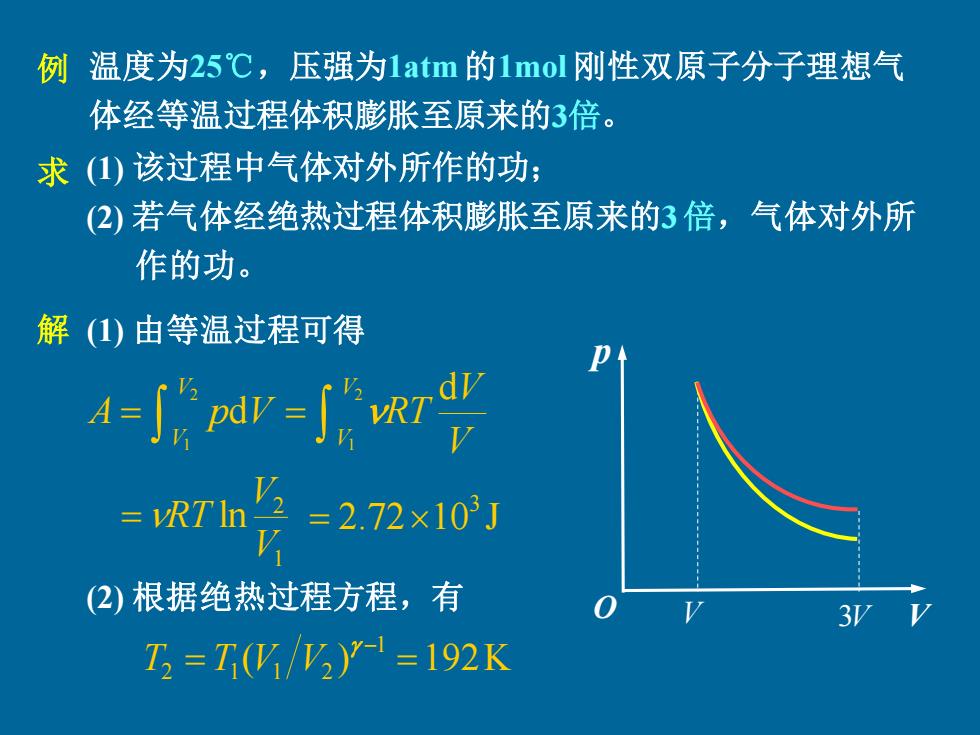
温度为25℃,压强为1atm 的1mol 刚性双原子分子理想气 体经等温过程体积膨胀至原来的3倍。 (1) 该过程中气体对外所作的功; (2) 若气体经绝热过程体积膨胀至原来的3 倍,气体对外所 作的功。 解 例 求 V p O V 3V = = 2 1 2 1 d d V V V V V V A p V RT 1 2 ln V V =RT (1) 由等温过程可得 2.72 10 J 3 = (2) 根据绝热过程方程,有 ( ) 192K 1 2 = 1 1 2 = − T T V V