
【注意事项】由于CEA提纯和单克隆抗体制备的技术很复杂,目前临床上多购买厂家生产的试剂盒进行测定。不同厂家生产的CEA诊断试剂,由于方法学及抗血清特异性的差异,测定值可能会有差别。不同批号的试剂严禁混合使用。试剂盒应4℃存放,并避免强光照射。2.20孔反应板及试管使用后,反应板可用洗板机清洗;也可用水洗净,后浸泡于硫酸铬酸洗液中,再经自来水、蒸馏水冲洗干净,干燥后可再次使用。3.基质液配制与使用过程中,禁与金属物品或其他氧化物接触。不得使用塑料容器。4.受检血清应新鲜,避免反复冻融。【临床意义】1.测定胃液和睡液的CEA对胃癌的诊断较有意义。胃液中的CEA含量一般高于血清中含量的1.5~15.5倍,而且较血中CEA升高较早。如果血中CEA在高水平上波动,而胃血CEA比值>1,则有利于胃癌的诊断,预后不良。唾液中的CEA更高于胃液,睡液CEA显著升高时与胃癌诊断的符合率高达90%。2.CEA是各脏器癌的广谱肿瘤标记,特异差,无助于各种肿瘤的早期诊断。但有助于鉴别肿瘤的良性和恶性。CEA测定可作为肿瘤手术成败的检测指标,对肿瘤的复发、转移及预后判断有一定的价值。3.高浓度的血清CEA含量与结肠癌相关,但无早期诊断价值。CEA升高也见于肠梗阻胆道梗阻、尿毒症、胰腺炎、肝硬化、结肠或直肠息肉、溃疡性结肠炎、局限性肠炎和溃疡病。附:放射免疫法测定癌胚抗原利用均相竞争性抑制原理,采用非饱和(顺序饱和)法对病人血清、血浆、胸水、腹水以及【原理】其它体液进行直接测定。样品中的CEA与限量的抗体预先反应一段时间,然后加入1251-CEA参与竞争剩余的抗体结合位。当样品的CEA浓度高时,剩余的抗体结合位就少,从而与抗体结合的1251-CEA就少。用分离剂分离出抗原-抗体复合物,并测定结合物中的放射性,发现1251-CEA的结合量与样品的CEA浓度呈函数关系。把标准点的数据绘成函数曲线后,便可算出检样中的CEA浓度。【试剂】有成套商品试剂盒供应。1.CEA标准品有0、5、10、20、40、80ng/ml共6种标准冻干品,使用时用蒸馏水1.0ml溶解2.1251-CEA冻干品,使用时用蒸馏水10ml溶解。3.抗CEA冻干品使用时用蒸馏水溶解(参照试剂说明书)。4.分离剂摇匀后直接使用。5所用试剂溶解后4℃保存,有效期2周。不允许不同批试剂相互替用。第6页共18页
第 6 页 共 18 页 【注意事项】 1.由于 CEA 提纯和单克隆抗体制备的技术很复杂,目前临床上多购买厂家生产的试剂 盒进行测定。不同厂家生产的 CEA 诊断试剂,由于方法学及抗血清特异性的差异,测定值 可能会有差别。不同批号的试剂严禁混合使用。试剂盒应 4℃存放,并避免强光照射。 2.20 孔反应板及试管使用后,反应板可用洗板机清洗;也可用水洗净,后浸泡于硫酸- 铬酸洗液中,再经自来水、蒸馏水冲洗干净,干燥后可再次使用。 3.基质液配制与使用过程中,禁与金属物品或其他氧化物接触。不得使用塑料容器。 4.受检血清应新鲜,避免反复冻融。 【临床意义】 1.测定胃液和唾液的 CEA 对胃癌的诊断较有意义。胃液中的 CEA 含量一般高于血清中 含量的 1.5~15.5 倍,而且较血中 CEA 升高较早。如果血中 CEA 在高水平上波动,而胃血 CEA 比值>1,则有利于胃癌的诊断,预后不良。唾液中的 CEA 更高于胃液,唾液 CEA 显著 升高时与胃癌诊断的符合率高达 90%。 2.CEA 是各脏器癌的广谱肿瘤标记,特异差,无助于各种肿瘤的早期诊断。但有助于 鉴别肿瘤的良性和恶性。CEA 测定可作为肿瘤手术成败的检测指标,对肿瘤的复发、转移及 预后判断有一定的价值。 3.高浓度的血清 CEA 含量与结肠癌相关,但无早期诊断价值。CEA 升高也见于肠梗阻、 胆道梗阻、尿毒症、胰腺炎、肝硬化、结肠或直肠息肉、溃疡性结肠炎、局限性肠炎和溃疡 病。 附:放射免疫法测定癌胚抗原 【原理】 利用均相竞争性抑制原理,采用非饱和(顺序饱和)法对病人血清、血浆、胸水、腹水以及 其它体液进行直接测定。样品中的 CEA 与限量的抗体预先反应一段时间,然后加入 125I-CEA 参与竞争剩 余的抗体结合位。当样品的 CEA 浓度高时,剩余的抗体结合位就少,从而与抗体结合的 125I-CEA 就少。 用分离剂分离出抗原-抗体复合物,并测定结合物中的放射性,发现 125I-CEA 的结合量与样品的 CEA 浓度 呈函数关系。把标准点的数据绘成函数曲线后,便可算出检样中的 CEA 浓度。 【试剂】 有成套商品试剂盒供应。 1.CEA 标准品 有 0、5、10、20、40、80ng/ml 共 6 种标准冻干品,使用时用蒸馏水 1.0ml 溶解。 2.125I-CEA 冻干品,使用时用蒸馏水 10ml 溶解。 3.抗 CEA 冻干品 使用时用蒸馏水溶解(参照试剂说明书)。 4.分离剂 摇匀后直接使用。 5.所用试剂溶解后 4℃保存,有效期 2 周。不允许不同批试剂相互替用
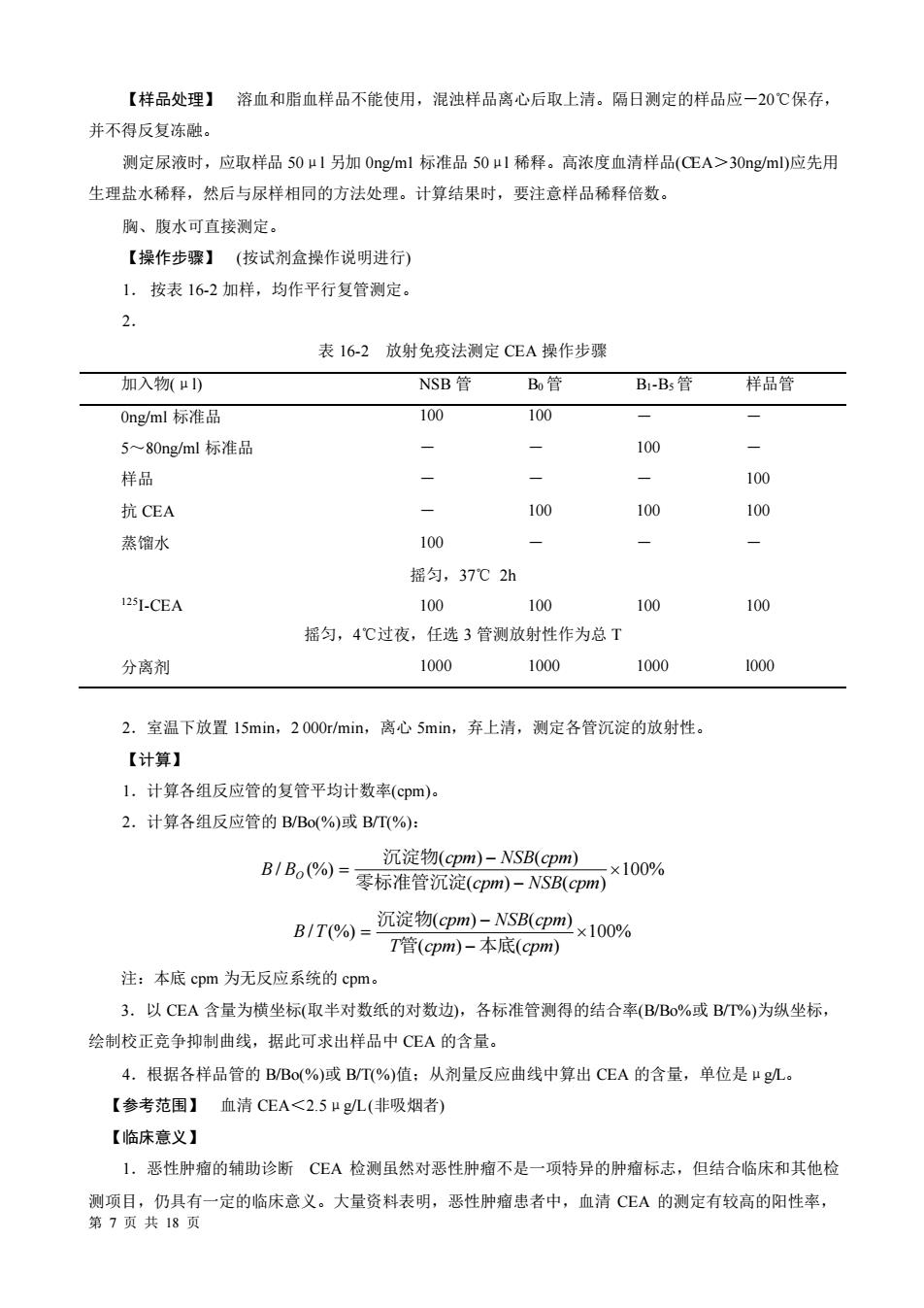
【样品处理】溶血和脂血样品不能使用,混浊样品离心后取上清。隔日测定的样品应一20℃保存,并不得反复冻融。测定尿液时,应取样品50uI另加0ng/ml标准品50u1稀释。高浓度血清样品(CEA>30ng/ml)应先用生理盐水稀释,然后与尿样相同的方法处理。计算结果时,要注意样品稀释倍数。胸、腹水可直接测定。(按试剂盒操作说明进行)【操作步骤】按表16-2加样,均作平行复管测定。1.2.表16-2放射免疫法测定CEA操作步骤加入物(μl)NSB管Bo管Bl-Bs管样品管1001000ng/ml标准品-100--5~80ng/ml标准品-100样品一100100抗CEA1100100蒸馏水摇匀,37℃2h121-CEA10100100100摇匀,4℃过夜,任选3管测放射性作为总T1000分离剂1000100010002.室温下放置15min,2000r/min,离心5min,弃上清,测定各管沉淀的放射性。【计算】1.计算各组反应管的复管平均计数率(cpm)。2.计算各组反应管的B/Bo(%)或B/I(%):沉淀物(cpm)-NSB(cpm)B / Bo(%) = ×100%零标准管沉淀(cpm)-NSB(cpm)沉淀物(cpm)-NSB(cpm)×10% B / T(%) =T管(cpm)-本底(cpm)注:本底cpm为无反应系统的cpm3.以CEA含量为横坐标(取半对数纸的对数边),各标准管测得的结合率(B/Bo%或B/T%)为纵坐标绘制校正竞争抑制曲线,据此可求出样品中CEA的含量。4.根据各样品管的B/Bo(%)或B/(%)值;从剂量反应曲线中算出CEA的含量,单位是gL。【参考范围】血清CEA<2.5μg/L(非吸烟者)【临床意义】1.恶性肿瘤的辅助诊断CEA 检测虽然对恶性肿瘤不是一项特异的肿瘤标志,但结合临床和其他检测项目,仍具有一定的临床意义。大量资料表明,恶性肿瘤患者中,血清CEA的测定有较高的阳性率,第7页共18页
第 7 页 共 18 页 【样品处理】 溶血和脂血样品不能使用,混浊样品离心后取上清。隔日测定的样品应-20℃保存, 并不得反复冻融。 测定尿液时,应取样品 50μl 另加 0ng/m1 标准品 50μl 稀释。高浓度血清样品(CEA>30ng/ml)应先用 生理盐水稀释,然后与尿样相同的方法处理。计算结果时,要注意样品稀释倍数。 胸、腹水可直接测定。 【操作步骤】 (按试剂盒操作说明进行) 1. 按表 16-2 加样,均作平行复管测定。 2. 表 16-2 放射免疫法测定 CEA 操作步骤 加入物(μl) NSB 管 B0 管 B1-B5 管 样品管 0ng/ml 标准品 100 100 - - 5~80ng/ml 标准品 - - 100 - 样品 - - - 100 抗 CEA - 100 100 100 蒸馏水 100 - - - 摇匀,37℃ 2h 125I-CEA 100 100 100 100 摇匀,4℃过夜,任选 3 管测放射性作为总 T 分离剂 1000 1000 1000 l000 2.室温下放置 15min,2 000r/min,离心 5min,弃上清,测定各管沉淀的放射性。 【计算】 1.计算各组反应管的复管平均计数率(cpm)。 2.计算各组反应管的 B/Bo(%)或 B/T(%): 100% ( ) ( ) ( ) ( ) / (%) − − = cpm NSB cpm cpm NSB cpm B BO 零标准管沉淀 沉淀物 100% ( ) ( ) ( ) ( ) / (%) − − = T cpm cpm cpm NSB cpm B T 管 本底 沉淀物 注:本底 cpm 为无反应系统的 cpm。 3.以 CEA 含量为横坐标(取半对数纸的对数边),各标准管测得的结合率(B/Bo%或 B/T%)为纵坐标, 绘制校正竞争抑制曲线,据此可求出样品中 CEA 的含量。 4.根据各样品管的 B/Bo(%)或 B/T(%)值;从剂量反应曲线中算出 CEA 的含量,单位是μg/L。 【参考范围】 血清 CEA<2.5μg/L (非吸烟者) 【临床意义】 1.恶性肿瘤的辅助诊断 CEA 检测虽然对恶性肿瘤不是一项特异的肿瘤标志,但结合临床和其他检 测项目,仍具有一定的临床意义。大量资料表明,恶性肿瘤患者中,血清 CEA 的测定有较高的阳性率