
第二章烷烃 只由碳和氢两种元素组成的有机化合物叫做碳氢化合物,简称为烃(hydrocarbon)。“烃” 字是取“碳”字中的“火”和“氢”字中的“圣”合并而成的,我们首先讨论烃类,不仅是因为烃是 最简单的有机化合物,更主要的是因为烃是各种有机物的母体,其他各类的有机物都可以看作 是烃的衍生物。 烃的种类很多,根据烃分子中碳原子连接的方式,烃可以分为三类: 1.脂肪烃 又叫开链烃。根据分子中碳和氢的比例,又可分为饱和烃(saturated hydrocarbon)和不 饱和烃(unsaturated hydrocarbon)。凡分子中与碳结台的氢原子数已达到饱和程度的烃叫做 饱和烃,开链的饱和烃也称为烷烃(alkane)。在链烃分子中所含的氢原子数比相应的烷烃为 少的叫不饱和烃,如烯烃(alkene),炔烃(alkyne)等。 2.脂环经 分子中碳原子联结成闭合的碳环。脂环烃也有饱和和不饱和之分。 3.芳香烃 一类特殊结构的烃,分子中大多含有六个碳原子组成的苯环,可以看作一类“特殊”的不饱 和环烯烃。 本章主要讨论饱和的脂肪烃 烷烃。不饱和脂肪烃,脂环烃和芳香烃将在以后的章节 中讨论。 2.1烷烃的同系列、通式和同分异构现象 最简单的烷烃是甲烷(CH),其次是乙烷(CeH),丙烷(CH)、丁烷(CHo).比较它 们的分子式,可看出任何两个相邻的烷烃在组成上都相差CH2。这样的一系列化合物叫做同 系列(homologous series)。同系列中的化合物互称为同系物(homologs)。相邻的同系物在组 成上相差的CHz叫同系差。在同系列中还可以看到在每个烷烃中的氢原子数是碳原子数的 两倍多两个,所以烷烃的通式是C,H+。我们以后将看到有机物除了烷烃同系列以外,还有 其他同系列。同系列是有机化学的普遍现象。我们了解这一概念很重要,因为一般讲来,各同 系列中的同系物的性质(特别是高级系物)很相似。因此在每一个系列里,只要研究几个化合 物的性质就可以推论出同系物中其他成员的性质,为我们学习和研究有机化合物带来很多的 方便。当然,要注意同系列的共性,也要注意它们的个性(特别是同系物中的头一个化合物往 往有较突出的特性),从分子结构上的差异来理解性质上的异同,这是我们学习有机化学的基 本方法之一。 在烷烃的同系列中,从丁烷起就有同分异构现象。丁烷有两个同分异构体,它们的构造式 21
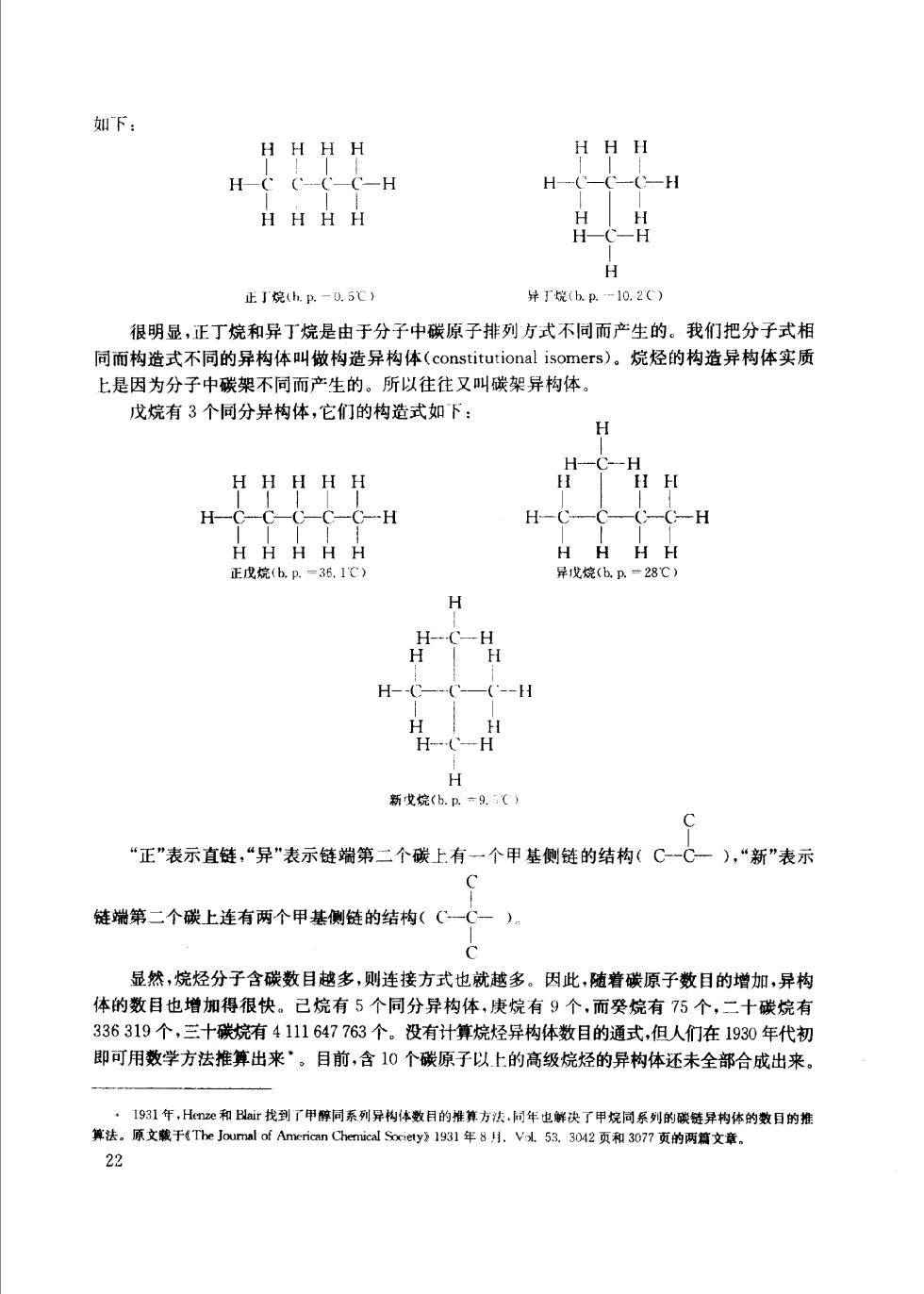
如下: HHHH H HH H-C-C-C-H H HH H 月用 H 正打烷(h.n.-0.5℃) +】丁皖hB.-10.2C) 很明显,正丁烧和异丁烷是由于分子中碳原子排列方式不同而产生的。我们把分子式相 同而构造式不同的异构体叫做构造异构体(constitutional isomers)。烷烃的构造异构体实质 上是因为分子中碳架不同而产生的。所以往往又叫碳架异构体。 戈烷有3个同分异构体,它们的构造式如下: H H HHHH HH H-C HHHHH H HHH 正h=36.1) 异巾使(hD.=28℃) H H-C-(- (-H H 新曳烷(6.取=9,( C “正”表示直链,“异"表示链端第二个碳上有一个甲基侧链的结构(C-C一),“新”表示 链端第二个碳上连有两个甲基侧链的结构(C 显然,烷烃分子含碳数目越多,则连接方式也就越多。因此,随着碳原子数目的增加,异构 体的数目也增加得很快。己烷有5个同分异构体,庚烷有9个,而癸烷有75个,二十碳烷有 336319个,三十碳烷有4111647763个。没有计算烷烃异构体数目的通式,但人们在1930年代初 即可用数学方法推算出来·。目前,含10个碳原子以上的高级烷烃的异构体还未全部合成出来。 101任. 算法。原文代 到了甲碎 系牙体用的推方时年电解决了甲同系列的碳链异体的数日的推 ery 13. 3042页和3077页的两文章

一个分子式究竞有多少个异构体,其书写的基本步骤是: (1)先写出这个烷烃的最长直链式。例如,己烷CH:的最长直链式为 H3一(H2-('Ha一('H-CH-CH3 (i) (2)写出少一个碳原子的直链式,把余下的-·个碳原子(即甲基)当作支链加在主链上,并 依次变动支链的位置。例如,己烷少一个碳原子的直链用甲基接上去的可能性有两种: CH-CH-CH,-C-CH (i) H CH,-CH:-CH-(H-(H, (in) CH. (3)再写少两个碳原子的直链式,把剩余的两个碳原子当作一个支链(即乙基)或两个支 链(即两个甲基)加在主链上。例如,己烷照此办法加上去的可能性有: CH:-CH-CH-CHs (iv) CH:CH H CH-C-CH:-'H (v) CH CH:-CH-CH-(H, (vi) CH CH 其中(vi)和(i)相同,故已烷的同分异构体只有3个:即(i)~(v). 从上面我们已经清楚地看到构造式不仅能代表化合物分子的组成,而且还能表明分子中 各原子的结合次序。书写构造式时,为了方便起见,可以用简式表示,如: CH.CH2CH-CH:CH:CH,:CH,CH(CH,)CH.CH2CH 分析下面烷烃分子链上碳原子和氢原子的连接情况,可以将它们分为几种不同的类型: CH. CHCH 其中有的碳与一个碳原子相连的,我们把它叫做一级碳原子,或叫第一(伯)碳原子,可用】表 示。直接与两个碳原子相连的,叫做二级碳原子,或叫第二(仲)碳原子,可用2°表示。直接与 三个碳原子相连的,叫做三级碳原子,或叫第三(叔)碳原子,可用3°表示。直接与四个碳原子 相连的,叫做四级碳原子,或叫第四(季)碳原子,可用4表示。 氢原子则按其与一级、一级或三级碳原子结合而分别称为第一、第二、第三氢原子。不同 类型的氢原子的活泼性不同。在研究烷烃分子中各部分的相对反应活性时,将经常用到这些 名称 烷烃分千中去掉一个氢原子形成的-一价基叫烷基,通式为C,H+1。通常烷基可用R表 23
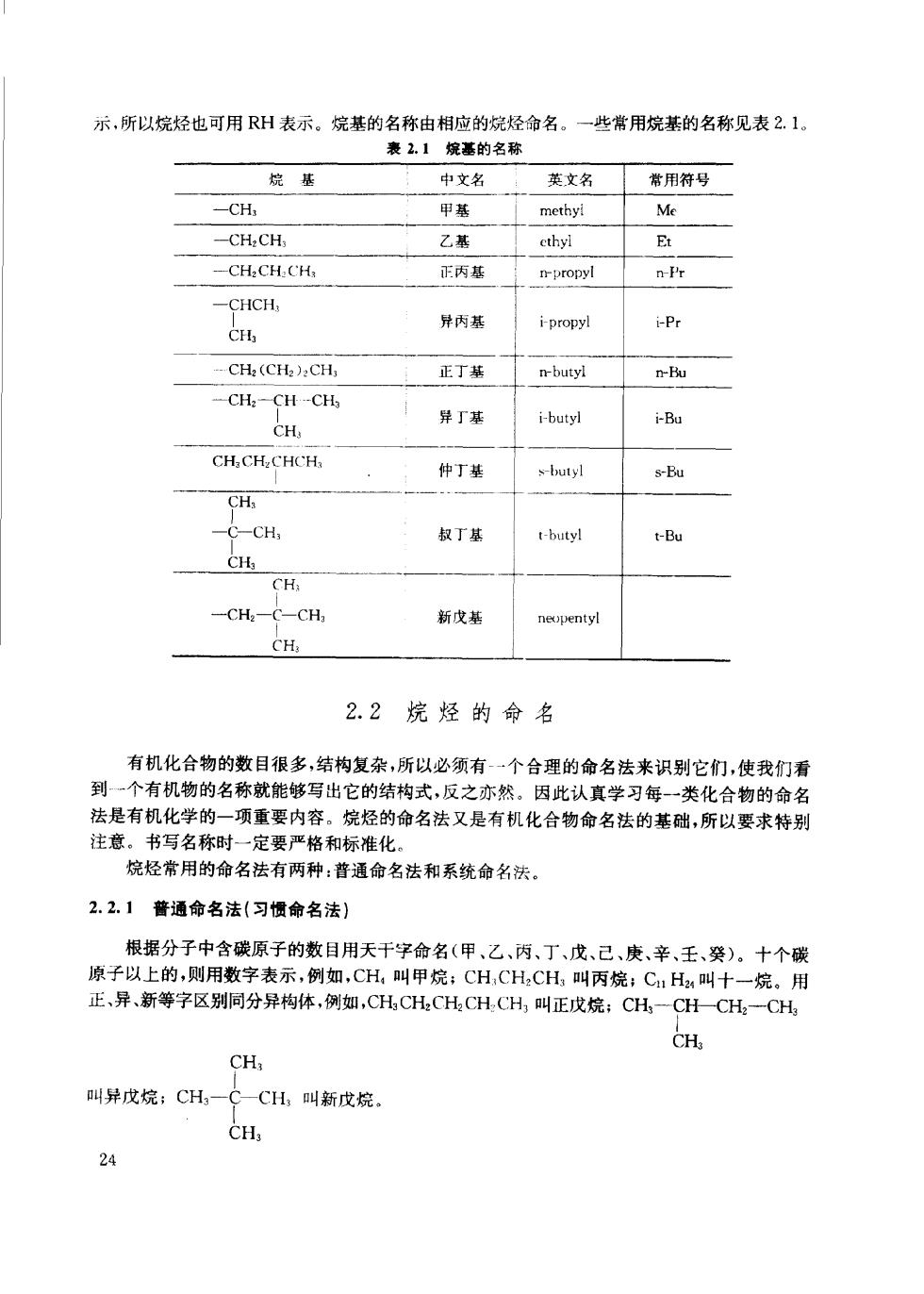
示,所以烷烃也可用RH表示。烷基的名称由相应的烷烃命名。一些常用烷基的名称见表2.1。 表2.1烷基的名称 烧基 中文名 英文名 常用符号 -CH, 甲基 methyl Me -CH:CH 乙基 ethyl E -CH.CH.CH. 正丙基 mpropyl nPr CHa 异内基 i-propyl i-Pr -CH:(CH:):CH, 正丁基 nbutyl n-Bu CH:-CH -CHs 异丁基 i-butyl i-Bu CH CH.CH.CHCHs 仲丁基 s-butyl s-Bu CH -C-CH 叔丁基 t-butyl t-Bu CHy CH 一CH2- -CH, 新戊基 neopentyl CH: 2.2烷烃的命名 有机化合物的数目很多,结构复杂,所以必须有-一个合理的命名法来识别它们,使我们看 到一个有机物的名称就能够写出它的结构式,反之亦然。因此认真学习每-一类化合物的命名 法是有机化学的一项重要内容。烷烃的命名法又是有机化合物命名法的基础,所以要求特别 注意。书写名称时一定要严格和标准化。 烧烃常用的命名法有两种:普通命名法和系统命名法 2.2.1普通命名法(习惯命名法) 根据分子中含碳原子的数目用天干字命名(甲、乙、丙、丁、戊、己、庚、辛、壬、癸)。十个碳 原子以上的,则用数字表示,例如,CH,叫甲烷;CH,CH,CH,叫丙烷:CH叫十一烷。用 正,异、新等字区别同分异构体,例如,CH.CH.CH,.CH,CH,叫正戊烷:CH,一CH一CH一CH CH CH: 叫异戊烷;CH,一CCH,叫新戊烷。 CH

显然,普通命名法对于较复杂的烷烃不能适用,例如普通命名法就无法区别己烷的五个异 构体。所以,对于比较复杂的烧烃必须使用系统命名法。 2.2.2系统命名法 为了解决有机化合物命名的困难,求得名词的统一,1892年许多国家的化学家在日内瓦 召开了国际化学会议,拟定了一种系统的有机化合物命名法,叫做日内瓦命名法。其基本精神 是体现化合物的系列和结构的特点。后来又经因际理论和应用化学联合会(International Union of Pure and Applied Chemistry,简称IUPAC)作了几次修改,最后一次修订是19T9年 进行的。IUPAC命名法的原则已普遍为各国所采用我国所用的系统命名法也是根据IU P八C系统的原则,结合我国文字的特点制定的。其要点如下: (1)对于直链烷烃和普通命名法基本相同,仅不写“正”字。例如: CH:-CH,-CH-CI-CH 普通命名法:正戊烷 系统命名法:戊烷 (2)对于支链烷烃,选择最长的直链烷烃导出其名称,支链作为取代基。其命名步骤如下: ①选择最长的碳链作主链。按主链所含碳原子数称为某烷,并以它作母体。例如: CH,一CH2-CH-CH2-(CcH2CH,←母体 CH3取代基 ②主链碳原子编号。从靠近取代基一头开始,依次用1,2,3.编号。使取代基的位次 最小。将取代基的位置(用阿拉伯数字表示)和名称放在母体名称的前面,二者之间加一对开 线。例如: CH-CH:-CHz-CH:-CH-CH, 叫2甲基己烷 CH. ③如果含有几个相同的取代基,则把它们合并起来。取代基的数目用二,三,四.表示。 写在取代基的前面,其位次必须逐个注明。位次的数字之间要用逗号隔开。如果含有儿个不 同的取代基时,应按“次序规则”(详见8.4节)将优先的基团排在后面,这里只列出几种烷基的 次序:甲基,乙基,丙基,丁基,戊基,异戊基,异丁基,新戍基,异丙基,仲丁基,叔丁基。 例如 CH CH,-CH-C-CH:-CH2-CH, 叫2,3,3三甲基已烷 CH,CH, CH,一CHCH-CH2一CHCH叫2,3,5三甲基纪烷 CHa CH CH 〔照取代基编号依次最小规则,不叫2,4,5三甲基己烷》 25