
Ho-gas CI CH, (2)链的重排 ①分子间一分子内聚合 非共轭二烯烃环化聚合属于此类,如á,“一型二烯烃异构化聚合模式: ②跨环聚合 降冰片烯阳离子聚合过程可能有两种形式: NMR和IR光谱分析结果表示最终聚合物是这两种结构的共聚物 ③释放应力的开环聚合(polymerization by strain relief) B-蒎(pinene)聚合时只得到单环结构的聚合物,反应如下; CH,R 形成的聚合物结构为: 4.2.4链转移和链终止反应 离子聚合的增长活性中心带有相同电荷,不能双分子终止,因此离子聚合不 会出现自动加速现象

链转移反应能导致阳离子聚合反应中聚合物链的增长停止,但不能是动力学 链终止。而与反离子反应形成共价键,动力学链终止。另外,某些化合物与活性 中心反应后生成无引发活性的离子对,同样也造成了动力学链终止。 4.2.4.1向单体链转移 对很多单体来说,向单体链转移是最常见的反应。不发生单体链转移的聚合 反应为数不多。 CH H -CHzC'[BF,OH]+H2C=C 一CH= [BF,OH] CHs CH2 CH。 ocH CH[BF,OH CH3 CH 另一类比较重要的向单体链转移反应,涉及到增长物种由单体夺取氢负离子。 CH, CH-C[BF,oH+Ch-C→→CH一CH+a-G CH CH, 这两类向单体链转移反应在动力学上是不可区分的。 4.2.4.2向抗衡离子转移 活性中心通过消除反应得到具有末端不饱和结构的聚合物分子,同时又生成 一个新的活性中心 CH CH 这类链终止也叫自发终止,再生出的引发剂一共引发剂络合物可以再引发聚合 4.2.4.3其它的链转移反应 在任何一个特定的聚合体系中还可能有一种或树种不可忽视的其它链转移反 应。链转移剂可能是溶剂、杂质或有意添加到反应体系中的物质,其通式为: (z+XA一Ht+X(Z 水、醇、酸、酸酐和酯都有不同的链转移作用。芳香族化合物、醚、卤代烷 是比较弱的链转移剂。向芳香族化合物的转移主要是通过芳环的烷基化米进行。 向聚合物的链转移在某种程度上也会发生。向聚合物的链转移可能是α-烯烃 (如丙烯)只能合成低相对分子质量的聚合物的原因。 R H CH-(R+CH →(H(R H 4.2.4.4与抗衡离子结合 增长碳正离子与抗衡离子结合造成链终止。例如,在苯乙烯的三氟乙酸催化聚合

反应: CHCH(0CXFCH-CH-CXCOXCE 另外,增长离子也可能与反离子的一部分负电部分结合,例如 CHC-[aOH一-GCq+oaH CH, 采用烷基铝-卤代烷类引发剂-助引发剂体系,可以发生烷基基团转移终止: CH: H -(CH)AX--CH-C-CH+(CHb)aAlX C 其中X为卤素原子。 当A1上有B氢时,总是优先发生氢转移。 一G-H+(CHAX4Ch-G H 4.2.5影响阳离子聚合的因素 这节主要讨论聚合温度、反应介质和反离子等对聚合反应速率和数均聚合度 的影响。 4.2.5.1反应介质的能响 离子聚合中,活性种总是以式(4一1)所示的离子对形式存在,并且被此处 于平衡之中。不同状态的活性种对聚合反应速率和聚合物的相对分子质量的影响 不同。阳离子聚合的k,要比k±大1~3个数量级,即使自由离子只占活性种的很少 部分,它对总的聚合速率的贡献也比离子对大得多。由于聚合体系中,常常存在 着不止一种的活性种的形式,因此,实验所测的聚合反应速率常数叫做表观速率 常数k明 不同的反应介质,它的极性和溶剂化能力是不同的。因此,会改变活性中心 和反离子之间的结合能及两者之间的距离,使式(4一1)的平衡发生移动,从而 使活性种在体系中的存在状态及相对含量发生改变。在极性和溶剂化能力的溶剂 中,自由离子和离子对中松对的比例都增加,因此使聚合速率和聚合物的相对分 子质量都增大。表4-2列出了碘引发对-甲氧基苯乙烯在不同溶剂中聚合时测得的 表观速率常数,从低介电常数的四氯化碳(=2.2)到高介电常数的二氯甲烷(
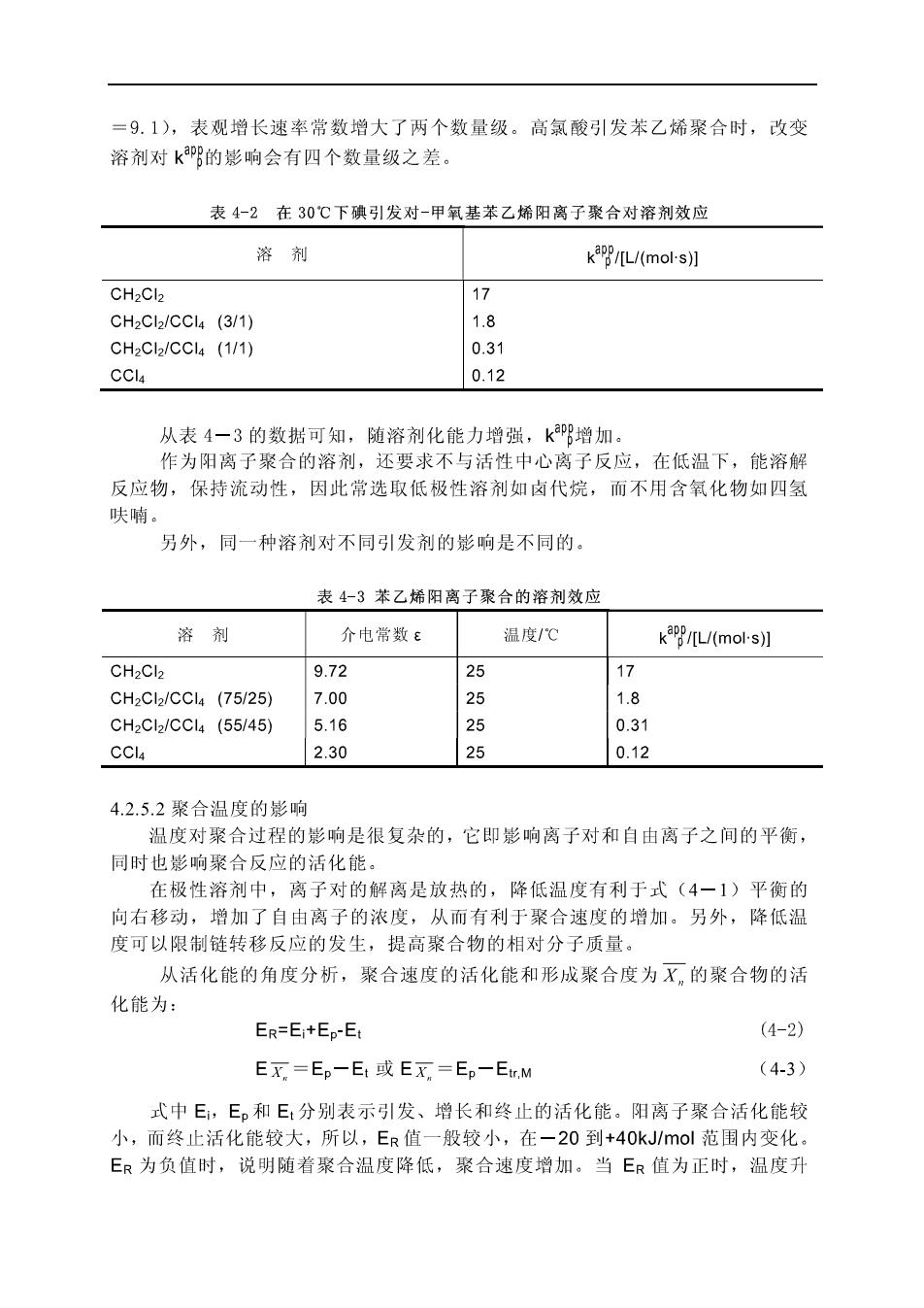
=9.1),表观增长速率常数增大了两个数量级。高氯酸引发苯乙烯聚合时,改变 溶剂对k阳的影响会有四个数量级之差。 表4-2在30℃下碘引发对-甲氧基苯乙烯阳离子聚合对溶剂效应 溶剂 kaP/L/(mol-s)] CH2Cl2/CCL (3/1) 1.8 CH2C2/CC4(1/1) 0.31 CCla 0.12 从表4一3的数据可知,随溶剂化能力增强,k增加 作为阳离子聚合的溶剂,还要求不与活性中心离子反应,在低温下,能溶解 反应物,保持流动性,因此常选取低极性溶剂如卤代烷,而不用含氧化物如四氢 呋喃。 另外,同一种溶剂对不同引发剂的影响是不同的。 表43苯乙烯阳离子聚合的溶剂效应 溶剂 介电常数e 温度/℃ /L/(mol-s)] CH2Cl2 9.72 25 17 CH2Cl21CCl4(75/25) 7.00 25 1. CH2Cl2/CCL4(55/45) 5.16 25 0.31 CCl4 2.30 25 0.12 4.2.5.2聚合温度的影响 温度对聚合过程的影响是很复杂的,它即影响离子对和自由离子之间的平衡, 同时也影响聚合反应的活化能 在极性溶剂中,离子对的解离是放热的,降低温度有利于式(4一1)平衡的 向右移动,增加了自由离子的浓度,从而有利于聚合速度的增加。另外,降低温 度可以限制链转移反应的发生,提高聚合物的相对分子质量。 从活化能的角度分析,聚合速度的活化能和形成聚合度为X。的聚合物的活 化能为: ER=E+Ep-Et (4-2) Ex=Ep一E!或Ex=Ep-EM (4-3) 式中E,E。和E1分别表示引发、增长和终止的活化能。阳离子聚合活化能较 小,而终止活化能较大,所以,E值一般较小,在一20到+40 kJ/mol范围内变化 ER为负值时,说明随着聚合温度降低,聚合速度增加。当ER值为正时,温度升

高,R,增加。但ER值比自由基聚合的值小得多(自由基聚合ER=80~90kJ/mol)。 故其聚合速率随温度变化较小。不同的单体有不同的ER值。即使是同一单体,E 值也随所使用的引发剂、助引发剂、溶剂等而变化。表44列出苯乙烯阳离子聚 合在不同条件下的ER值 表44苯乙烯阳离子聚合的活化能 引发体系 溶剂 ER/(Ki/mol) TiCl-H2O CH2Cl2 355 TIClA-CCICOOH PhCH3 -6.3 CClCOoH C2HsBr 126 SnCl4-H2O PhH 23 33.5 CChCOOH CHaNO2 58.6 由于Ex=Ep一E,或者Ex=Ep-EM,通常Ex为负值,即阳离子聚合随着 温度升高X变小。当终止方式主要为链转移反应时,Ex为更大的负值。因为结 合终止和自发终止的活化能较链转移反应的活化能大。因此降低温度有利于抑制 链终止和链转移,有利于相对分子质量的提高。 102 45 6 图4一1在A1C3引发的丁烯聚合反应中,X。对温度的依赖关系 图4一1是在二氯甲烷溶剂中,AIC3引发异丁烯聚合所得聚合物的数均聚合 度X,与温度的依濑关系。直线在-100℃附近有一个转变,即在-100℃以上Ex -23.4kJ/mol,而在-100℃以下Ex=-3.1kJ/mol。这是因为在-100℃以上,终止是 通过对溶剂链转移实现的。在-100℃以下,终止主要是对单体链转移的结果。 4.2.5.3反离子的影响