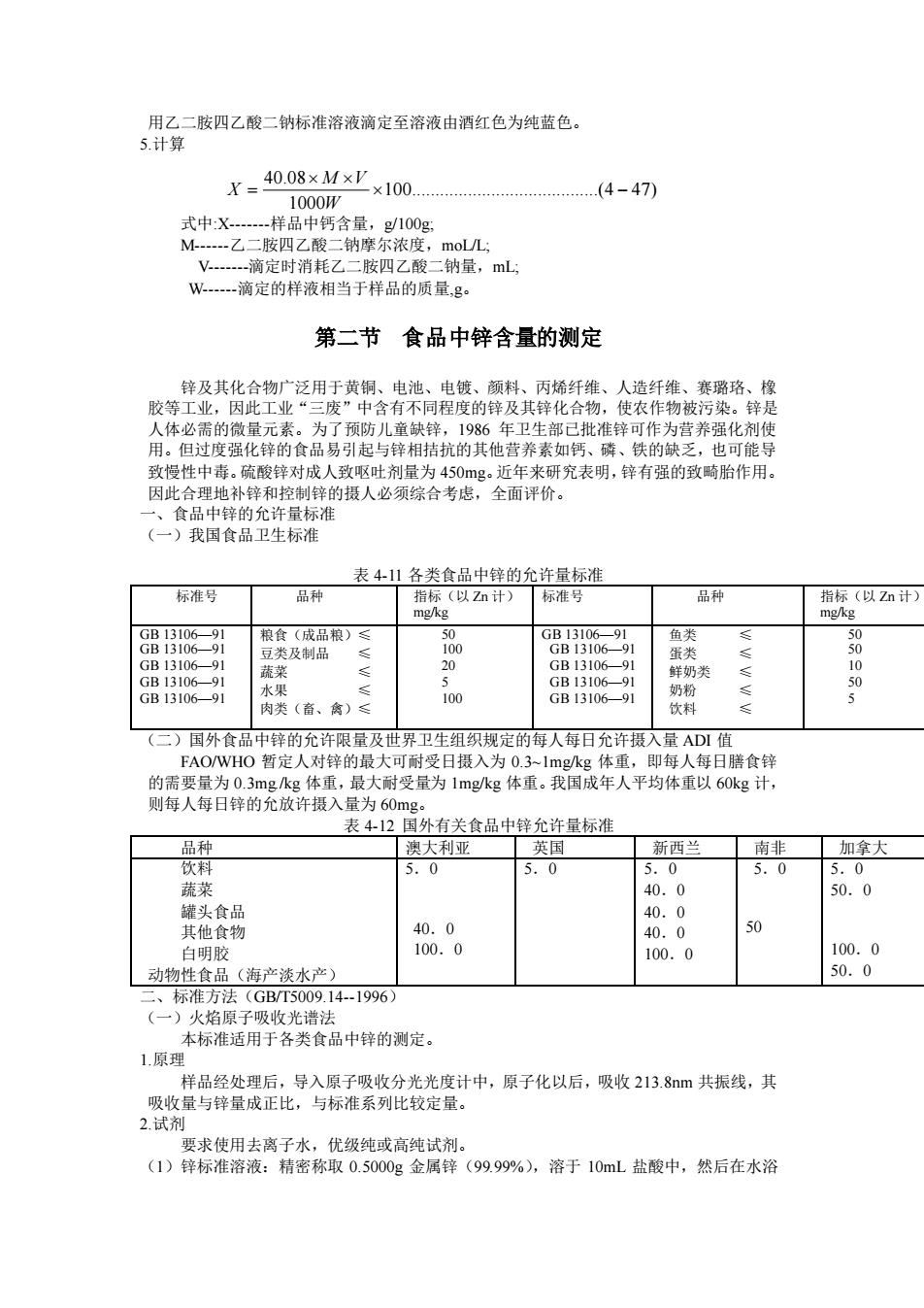
用乙二胺四乙酸二钠标准溶液滴定至溶液由酒红色为纯蓝色。 5.计算 式中:X-样品中钙含量,g/100g; M-乙二胺四乙酸二钠摩尔浓度,moL/L; V-滴定时消耗乙二胺四乙酸二钠量,mL; W-滴定的样液相当于样品的质量,g。 第二节 食品中锌含量的测定 锌及其化合物广泛用于黄铜、电池、电镀、颜料、丙烯纤维、人造纤维、赛璐珞、橡 胶等工业,因此工业“三废”中含有不同程度的锌及其锌化合物,使农作物被污染。锌是 人体必需的微量元素。为了预防儿童缺锌,1986 年卫生部已批准锌可作为营养强化剂使 用。但过度强化锌的食品易引起与锌相拮抗的其他营养素如钙、磷、铁的缺乏,也可能导 致慢性中毒。硫酸锌对成人致呕吐剂量为 450mg。近年来研究表明,锌有强的致畸胎作用。 因此合理地补锌和控制锌的摄人必须综合考虑,全面评价。 一、食品中锌的允许量标准 (一)我国食品卫生标准 表 4-11 各类食品中锌的允许量标准 标准号 品种 指标(以 Zn 计) mg/kg 标准号 品种 指标(以 Zn 计) mg/kg GB 13106—91 GB 13106—91 GB 13106—91 GB 13106—91 GB 13106—91 粮食(成品粮)≤ 豆类及制品 ≤ 蔬菜 ≤ 水果 ≤ 肉类(畜、禽)≤ 50 100 20 5 100 GB 13106—91 GB 13106—91 GB 13106—91 GB 13106—91 GB 13106—91 鱼类 ≤ 蛋类 ≤ 鲜奶类 ≤ 奶粉 ≤ 饮料 ≤ 50 50 10 50 5 (二)国外食品中锌的允许限量及世界卫生组织规定的每人每日允许摄入量 ADI 值 FAO/WHO 暂定人对锌的最大可耐受日摄入为 0.3~1mg/kg 体重,即每人每日膳食锌 的需要量为 0.3mg./kg 体重,最大耐受量为 1mg/kg 体重。我国成年人平均体重以 60kg 计, 则每人每日锌的允放许摄入量为 60mg。 表 4-12 国外有关食品中锌允许量标准 品种 澳大利亚 英国 新西兰 南非 加拿大 饮料 蔬菜 罐头食品 其他食物 白明胶 动物性食品(海产淡水产) 5.0 40.0 100.0 5.0 5.0 40.0 40.0 40.0 100.0 5.0 50 5.0 50.0 100.0 50.0 二、标准方法(GB/T5009.14-1996) (一)火焰原子吸收光谱法 本标准适用于各类食品中锌的测定。 1.原理 样品经处理后,导入原子吸收分光光度计中,原子化以后,吸收 213.8nm 共振线,其 吸收量与锌量成正比,与标准系列比较定量。 2.试剂 要求使用去离子水,优级纯或高纯试剂。 (1)锌标准溶液:精密称取 0.5000g 金属锌(99.99%),溶于 10mL 盐酸中,然后在水浴 100.(4 47) 1000 40.08 − = W M V X
用乙二胺四乙酸二钠标准溶液滴定至溶液由酒红色为纯蓝色。 5.计算 式中:X-样品中钙含量,g/100g; M-乙二胺四乙酸二钠摩尔浓度,moL/L; V-滴定时消耗乙二胺四乙酸二钠量,mL; W-滴定的样液相当于样品的质量,g。 第二节 食品中锌含量的测定 锌及其化合物广泛用于黄铜、电池、电镀、颜料、丙烯纤维、人造纤维、赛璐珞、橡 胶等工业,因此工业“三废”中含有不同程度的锌及其锌化合物,使农作物被污染。锌是 人体必需的微量元素。为了预防儿童缺锌,1986 年卫生部已批准锌可作为营养强化剂使 用。但过度强化锌的食品易引起与锌相拮抗的其他营养素如钙、磷、铁的缺乏,也可能导 致慢性中毒。硫酸锌对成人致呕吐剂量为 450mg。近年来研究表明,锌有强的致畸胎作用。 因此合理地补锌和控制锌的摄人必须综合考虑,全面评价。 一、食品中锌的允许量标准 (一)我国食品卫生标准 表 4-11 各类食品中锌的允许量标准 标准号 品种 指标(以 Zn 计) mg/kg 标准号 品种 指标(以 Zn 计) mg/kg GB 13106—91 GB 13106—91 GB 13106—91 GB 13106—91 GB 13106—91 粮食(成品粮)≤ 豆类及制品 ≤ 蔬菜 ≤ 水果 ≤ 肉类(畜、禽)≤ 50 100 20 5 100 GB 13106—91 GB 13106—91 GB 13106—91 GB 13106—91 GB 13106—91 鱼类 ≤ 蛋类 ≤ 鲜奶类 ≤ 奶粉 ≤ 饮料 ≤ 50 50 10 50 5 (二)国外食品中锌的允许限量及世界卫生组织规定的每人每日允许摄入量 ADI 值 FAO/WHO 暂定人对锌的最大可耐受日摄入为 0.3~1mg/kg 体重,即每人每日膳食锌 的需要量为 0.3mg./kg 体重,最大耐受量为 1mg/kg 体重。我国成年人平均体重以 60kg 计, 则每人每日锌的允放许摄入量为 60mg。 表 4-12 国外有关食品中锌允许量标准 品种 澳大利亚 英国 新西兰 南非 加拿大 饮料 蔬菜 罐头食品 其他食物 白明胶 动物性食品(海产淡水产) 5.0 40.0 100.0 5.0 5.0 40.0 40.0 40.0 100.0 5.0 50 5.0 50.0 100.0 50.0 二、标准方法(GB/T5009.14-1996) (一)火焰原子吸收光谱法 本标准适用于各类食品中锌的测定。 1.原理 样品经处理后,导入原子吸收分光光度计中,原子化以后,吸收 213.8nm 共振线,其 吸收量与锌量成正比,与标准系列比较定量。 2.试剂 要求使用去离子水,优级纯或高纯试剂。 (1)锌标准溶液:精密称取 0.5000g 金属锌(99.99%),溶于 10mL 盐酸中,然后在水浴 100.(4 47) 1000 40.08 − = W M V X

上蒸发至近干,用少量水溶液后移入 1000mL 容量瓶中,以水稀释至刻度。贮于聚乙烯瓶 中,此溶液每毫升相当于 0.5mg 锌。 (2)锌标准使用液:吸取 10.0mL 锌标准溶液,置于 50mL 容量瓶中,以 0.1moL/L 盐酸 稀释至刻度,此溶液每毫升相当于 100μg 锌。 (3)1moL/L 盐酸:量取 10mL 盐酸,加水稀释至 120mL。 3.仪器 原子吸收分光光度计。 4.操作方法 (1)样品处理 ①谷类:去除其中杂物及尘土,必要时除去外壳,碾碎,过 40 目筛,混匀。称取 5.00~10.00g, 置于 50mL 瓷坩埚中,小火炭化至无烟,移入马弗炉中,500±25℃以下灰化约 8h 后,取 出坩埚,放冷后再加少量混合酸,小火加热,不使干涸,必要时再加少放混合酸,如此反 复处理,直至残渣中无炭粒,待坩埚稍冷,加 10mL 1moL/L 盐酸,溶解残渣并移入 50mL 溶量瓶中,再用 1moL/L 盐酸反复洗涤坩埚,洗液并入容量瓶中,并稀释至刻度,混匀备 用。 取与处理样品相同量的混合酸和 1moL/L 盐酸按同一操作方法做试剂空白试验。 ②蔬菜、瓜果及豆类:取可食部分洗净晾干,充分切碎混匀。称取 10.00~20.00g,置于瓷 坩埚中,加 1mL(1+10)磷酸,小火炭化,以下按谷样品自“然后移入马弗炉中”起,依法 操作。 ③禽、蛋、水产及乳制品:取可食部分充分混匀。称取 5.00~10.00g,置于瓷坩中,小火炭 化,以下按谷类样品自“然后移入马弗炉中”起,依法操作。 乳类经混匀后,量取 50mL,置于瓷坩埚中,加 1mL 磷酸(1+10),在水浴上蒸干, 再小火炭化,以下按谷类样品自“然后移入高温炉中”起,依法操作。 (2)测定 吸取 0.0, 0.1., 0.20, 0.4, 0.80mL 锌标准使用液,分别置于 50mL 容量瓶中,以 1moL/L 盐酸稀释至刻度,混匀(各容量瓶中每毫升分别相当于 0,0.2,0.4,0.8,1.6μg 锌)。 将处理后的样液、试剂空白液和各容量瓶中锌标准液分别导入火焰进行测定。测定条 件:灯电流 6mA,波长 213.8nm,狭缝 0.38nm,空气流量 10L/min,乙炔流量 2.3L/min, 灯头高度 3mm,氘灯背景校正(也可根据仪器型号,调至最佳条件),以锌含量对应浓度 吸光度,绘制标准曲线经比较。 (3)计算 式中: -样品中锌的含量,mg/kg 或,mg/L; A1-测定用样品液中锌的含量,μg/mL; A2-试剂空白液中锌的含量,μg/mL; M1-样品质量(体积),g(mL); V-样品处理液的总体积,mL。 5.说明 (1)一般食品通过样品处理后的试样水溶液直接喷雾进行原子吸收测定即可得出准确的结 果,但是当食盐、碱金属、碱土金属以及磷酸盐大量存在时,需用溶剂萃取法将提取出来, 排除共存盐类的影响,对锌较低的样品如蔬菜、水果等,也可采用萃取法将锌浓缩,以提 高测定灵敏度。 (2)锌的溶剂萃取常用 APDC-MIBK 提取方法,在 pH5~10 的介质中,锌都能与 APDC 生成 配合物被 MIBK 萃取,因而不必调整溶液的 pH 值。 (3)本法以稻米为样多次平行测定,标准偏差 1.59,相对标准偏差 3.4%,回收率 95%。 (4)实验前要以测空白值检查水、器皿的锌污染至稳定合格。 (二)二硫腙比色法 1.原理 .(4 15) 1000 ( ) 1000 1 1 2 1 − − = m A A V X X 1
上蒸发至近干,用少量水溶液后移入 1000mL 容量瓶中,以水稀释至刻度。贮于聚乙烯瓶 中,此溶液每毫升相当于 0.5mg 锌。 (2)锌标准使用液:吸取 10.0mL 锌标准溶液,置于 50mL 容量瓶中,以 0.1moL/L 盐酸 稀释至刻度,此溶液每毫升相当于 100μg 锌。 (3)1moL/L 盐酸:量取 10mL 盐酸,加水稀释至 120mL。 3.仪器 原子吸收分光光度计。 4.操作方法 (1)样品处理 ①谷类:去除其中杂物及尘土,必要时除去外壳,碾碎,过 40 目筛,混匀。称取 5.00~10.00g, 置于 50mL 瓷坩埚中,小火炭化至无烟,移入马弗炉中,500±25℃以下灰化约 8h 后,取 出坩埚,放冷后再加少量混合酸,小火加热,不使干涸,必要时再加少放混合酸,如此反 复处理,直至残渣中无炭粒,待坩埚稍冷,加 10mL 1moL/L 盐酸,溶解残渣并移入 50mL 溶量瓶中,再用 1moL/L 盐酸反复洗涤坩埚,洗液并入容量瓶中,并稀释至刻度,混匀备 用。 取与处理样品相同量的混合酸和 1moL/L 盐酸按同一操作方法做试剂空白试验。 ②蔬菜、瓜果及豆类:取可食部分洗净晾干,充分切碎混匀。称取 10.00~20.00g,置于瓷 坩埚中,加 1mL(1+10)磷酸,小火炭化,以下按谷样品自“然后移入马弗炉中”起,依法 操作。 ③禽、蛋、水产及乳制品:取可食部分充分混匀。称取 5.00~10.00g,置于瓷坩中,小火炭 化,以下按谷类样品自“然后移入马弗炉中”起,依法操作。 乳类经混匀后,量取 50mL,置于瓷坩埚中,加 1mL 磷酸(1+10),在水浴上蒸干, 再小火炭化,以下按谷类样品自“然后移入高温炉中”起,依法操作。 (2)测定 吸取 0.0, 0.1., 0.20, 0.4, 0.80mL 锌标准使用液,分别置于 50mL 容量瓶中,以 1moL/L 盐酸稀释至刻度,混匀(各容量瓶中每毫升分别相当于 0,0.2,0.4,0.8,1.6μg 锌)。 将处理后的样液、试剂空白液和各容量瓶中锌标准液分别导入火焰进行测定。测定条 件:灯电流 6mA,波长 213.8nm,狭缝 0.38nm,空气流量 10L/min,乙炔流量 2.3L/min, 灯头高度 3mm,氘灯背景校正(也可根据仪器型号,调至最佳条件),以锌含量对应浓度 吸光度,绘制标准曲线经比较。 (3)计算 式中: -样品中锌的含量,mg/kg 或,mg/L; A1-测定用样品液中锌的含量,μg/mL; A2-试剂空白液中锌的含量,μg/mL; M1-样品质量(体积),g(mL); V-样品处理液的总体积,mL。 5.说明 (1)一般食品通过样品处理后的试样水溶液直接喷雾进行原子吸收测定即可得出准确的结 果,但是当食盐、碱金属、碱土金属以及磷酸盐大量存在时,需用溶剂萃取法将提取出来, 排除共存盐类的影响,对锌较低的样品如蔬菜、水果等,也可采用萃取法将锌浓缩,以提 高测定灵敏度。 (2)锌的溶剂萃取常用 APDC-MIBK 提取方法,在 pH5~10 的介质中,锌都能与 APDC 生成 配合物被 MIBK 萃取,因而不必调整溶液的 pH 值。 (3)本法以稻米为样多次平行测定,标准偏差 1.59,相对标准偏差 3.4%,回收率 95%。 (4)实验前要以测空白值检查水、器皿的锌污染至稳定合格。 (二)二硫腙比色法 1.原理 .(4 15) 1000 ( ) 1000 1 1 2 1 − − = m A A V X X 1

样品经消化后,在 pH4.0~5.5 时,锌离子与二硫腙形成紫红色络合物,溶于四氯化碳, 加入硫代硫酸钠,防止铜、汞、铅、铋,银和镉等离子干扰,与标准系列比较定量。 2.试剂 (1)2moL/L 乙酸钠溶液:称取 68g 乙酸钠( )加水溶解后稀释至 250mL。 (2)2moL/L 乙酸:量取 10.0mL 冰乙酸,加水稀释至 85mL。 (3)乙酸-乙酸盐缓冲液:2moL/L 乙酸钠溶液与 2moL/L 乙酸等体积混合,此溶液 pH 为 4.7 左右,用(0.1g./L)二硫腙-四氯化碳溶液提取数次,每次 10mL,除去其中的锌,至四 氯化碳层绿色不变为止,弃去四氯化碳层,再有四氯化碳提取乙酸-乙酸盐缓冲液中过剩的 二硫腙,至四氯化碳层无色,弃去四氯化碳层。 (4)氨水(1+1). (5)2moL/L 盐酸:量取 10mL 盐酸,加水稀释至 60mL。 (6)0.02moL/L 盐酸:吸取 1mL 2moL/L 盐酸,加水稀释至 100mL。 (7) 1g/L 酚红指示液:称取 0.1g 酚红,加少量乙醇溶解,并稀释至 100mL。 (8)200g/L 盐酸羟胺溶液:称取 20g 盐酸羟胺,加 60mL 水,用 2moL/L 乙酸调节 pH 至 4.0~5.5,以下按 2.(3)用 0.1g/L 二硫腙-四氯化碳溶液处理,用水稀释至 100mL。 (9)250g/L 硫代硫酸钠溶液:称取 25g 硫代硫酸钠,加 60mL 水,用 2moL/L 乙酸调节 pH 至 4.0~5.5,以下按 2.用 0.1g/L 二硫腙-四氯化碳溶液处理,用水稀释至 100mL。 (10)0.1g/L 二硫腙-四氯化碳溶液。 (11)二硫腙使用液:吸取 1.0mL.0.1g/L 二硫腙-四氯化碳溶液,加四氯化碳至 10.0mL,混 匀。用 1cm 比色杯,以四氯化碳调节零点,于波长 530nm 处测吸光度(A)。用式(4-16) 计算出配制 100mL 二硫腙使用液(57%透光率)所需 0.1g/L 二硫腙四氯化碳溶液毫升数 (V)。 (12)锌标准溶液:精密称取 0.1000g 锌,加 10mL2moL/L 盐酸,溶解后移入 1000mL 容 量瓶中,加水稀释至刻度。此溶液每毫升相当于 100.0μg 锌。 (13)锌标准使用溶液:吸取 1.0mL 锌标准溶液,置于 100mL 容量瓶中,加 1mL,2moL/L 盐酸,以水稀释至刻度,此溶液每毫升相当于 1.0μg 锌。 3.仪器 分光光度计。 4.操作方法 (1)样品消化 同“食品中砷的标准测定方法”银盐法中样品的消化①硝酸-高氯酸-硫酸法和②硝 酸-硫酸法。 (2)测定 准确吸取 5.0~10.0mL 定容的消化液和相同量的试剂空白液,分别置于 125mL,分 液漏斗中,加 5mL 水,0.5mL 200g/L 盐酸羟胺溶液,摇匀,再加 2 滴酚红指示液,用氨 水(1+1)调节至红色,再加 5mL 0.1g/L 二硫腙-四氯化碳溶液,剧烈振摇 2min,静置分 层。将四氯化碳层移入另一分液漏斗中,水层再用少量二硫腙-四氯化碳溶液振摇提取, 每次 2~3mL,直至二硫腙-四氯化碳溶液绿色不变为止。合并提取液,用 5mL 水洗涤,四 氯化碳层用 0.02moL/L 盐酸提取 2 次,每次 10mL,提取时剧烈振摇 2min,合并 0.02moL/L 盐酸提取液,并有少量四氯化碳洗去残留的二硫腙。吸取 1.0 2.0 3.0 4.0 5.0mL 锌标准使 用液。(相当 0.0 1.0 2.0 3.0 4.0 5.0 mg)分别至于 125mL 分液漏斗中,各加盐酸(0.02moL/L) 至 20mL 于样品提取液、试剂空白提取液及锌标准溶液各分液漏斗中加 10mL 乙酸-乙酸 盐缓冲液、1mL 250mL 硫代硫酸钠溶液,摇匀,再各加入 10.0mL 二硫腙使用液,剧烈振 摇 2min。静至分层后,经脱脂棉将四氯化碳层滤入 1cm 比色杯中,以四氯化碳调节零点, 于波长 530nm 处测吸光度,绘制标准曲线比较。 (3)计算 CH3COONa 3H2O .(4 16) 10(2 lg 57) 2.44 = − − = A A V .(4 17) 1000 ( ) 1000 2 3 2 3 4 4 2 − − = V V m A A V X
样品经消化后,在 pH4.0~5.5 时,锌离子与二硫腙形成紫红色络合物,溶于四氯化碳, 加入硫代硫酸钠,防止铜、汞、铅、铋,银和镉等离子干扰,与标准系列比较定量。 2.试剂 (1)2moL/L 乙酸钠溶液:称取 68g 乙酸钠( )加水溶解后稀释至 250mL。 (2)2moL/L 乙酸:量取 10.0mL 冰乙酸,加水稀释至 85mL。 (3)乙酸-乙酸盐缓冲液:2moL/L 乙酸钠溶液与 2moL/L 乙酸等体积混合,此溶液 pH 为 4.7 左右,用(0.1g./L)二硫腙-四氯化碳溶液提取数次,每次 10mL,除去其中的锌,至四 氯化碳层绿色不变为止,弃去四氯化碳层,再有四氯化碳提取乙酸-乙酸盐缓冲液中过剩的 二硫腙,至四氯化碳层无色,弃去四氯化碳层。 (4)氨水(1+1). (5)2moL/L 盐酸:量取 10mL 盐酸,加水稀释至 60mL。 (6)0.02moL/L 盐酸:吸取 1mL 2moL/L 盐酸,加水稀释至 100mL。 (7) 1g/L 酚红指示液:称取 0.1g 酚红,加少量乙醇溶解,并稀释至 100mL。 (8)200g/L 盐酸羟胺溶液:称取 20g 盐酸羟胺,加 60mL 水,用 2moL/L 乙酸调节 pH 至 4.0~5.5,以下按 2.(3)用 0.1g/L 二硫腙-四氯化碳溶液处理,用水稀释至 100mL。 (9)250g/L 硫代硫酸钠溶液:称取 25g 硫代硫酸钠,加 60mL 水,用 2moL/L 乙酸调节 pH 至 4.0~5.5,以下按 2.用 0.1g/L 二硫腙-四氯化碳溶液处理,用水稀释至 100mL。 (10)0.1g/L 二硫腙-四氯化碳溶液。 (11)二硫腙使用液:吸取 1.0mL.0.1g/L 二硫腙-四氯化碳溶液,加四氯化碳至 10.0mL,混 匀。用 1cm 比色杯,以四氯化碳调节零点,于波长 530nm 处测吸光度(A)。用式(4-16) 计算出配制 100mL 二硫腙使用液(57%透光率)所需 0.1g/L 二硫腙四氯化碳溶液毫升数 (V)。 (12)锌标准溶液:精密称取 0.1000g 锌,加 10mL2moL/L 盐酸,溶解后移入 1000mL 容 量瓶中,加水稀释至刻度。此溶液每毫升相当于 100.0μg 锌。 (13)锌标准使用溶液:吸取 1.0mL 锌标准溶液,置于 100mL 容量瓶中,加 1mL,2moL/L 盐酸,以水稀释至刻度,此溶液每毫升相当于 1.0μg 锌。 3.仪器 分光光度计。 4.操作方法 (1)样品消化 同“食品中砷的标准测定方法”银盐法中样品的消化①硝酸-高氯酸-硫酸法和②硝 酸-硫酸法。 (2)测定 准确吸取 5.0~10.0mL 定容的消化液和相同量的试剂空白液,分别置于 125mL,分 液漏斗中,加 5mL 水,0.5mL 200g/L 盐酸羟胺溶液,摇匀,再加 2 滴酚红指示液,用氨 水(1+1)调节至红色,再加 5mL 0.1g/L 二硫腙-四氯化碳溶液,剧烈振摇 2min,静置分 层。将四氯化碳层移入另一分液漏斗中,水层再用少量二硫腙-四氯化碳溶液振摇提取, 每次 2~3mL,直至二硫腙-四氯化碳溶液绿色不变为止。合并提取液,用 5mL 水洗涤,四 氯化碳层用 0.02moL/L 盐酸提取 2 次,每次 10mL,提取时剧烈振摇 2min,合并 0.02moL/L 盐酸提取液,并有少量四氯化碳洗去残留的二硫腙。吸取 1.0 2.0 3.0 4.0 5.0mL 锌标准使 用液。(相当 0.0 1.0 2.0 3.0 4.0 5.0 mg)分别至于 125mL 分液漏斗中,各加盐酸(0.02moL/L) 至 20mL 于样品提取液、试剂空白提取液及锌标准溶液各分液漏斗中加 10mL 乙酸-乙酸 盐缓冲液、1mL 250mL 硫代硫酸钠溶液,摇匀,再各加入 10.0mL 二硫腙使用液,剧烈振 摇 2min。静至分层后,经脱脂棉将四氯化碳层滤入 1cm 比色杯中,以四氯化碳调节零点, 于波长 530nm 处测吸光度,绘制标准曲线比较。 (3)计算 CH3COONa 3H2O .(4 16) 10(2 lg 57) 2.44 = − − = A A V .(4 17) 1000 ( ) 1000 2 3 2 3 4 4 2 − − = V V m A A V X

式中: -样品中锌的含量,mg/kg 或 mg/L。 A3-测定用样品消化液中锌的含量,μg/mL。 A4-试剂空白液中锌的含量,μg/mL。 M2-样品质量(体积),g(mL); V2-样品消化液的总体积,mL。 V3-测定用消化液的体积,mL。 V4-提取液总体积,mL。 (三)二硫腙比色法(一次提取) 1.原理 同二硫腙比色法。 2.试剂 (1)01g/L 二硫腙-四氯化碳溶液。 (2)2g/L 甲基橙指示液:称取 0.2g 甲基橙,用乙醇(20%)溶解并稀释至 100mL。其他 试剂与二硫腙比色法同。 3.仪器 分光光度计。 4.操作方法 (1)样品消化 与二硫腙比色法同。 (2)测定 吸取 5.0~10.0mL 定容的消化液和相同量的试剂空白液,分别置于 125mL 分液漏斗中, 加水至 10mL。 吸取 0.0,1.0,2.0,3.0,4.0,5.0mL 锌标准使用液(相当 0,1.0,2.0,3.0,4.0,5.0μg 锌),分别 置于 125mL 分液漏斗中,各加水至 10mL。 于样品消化液、试剂空白液及锌标准液中各加 1 滴甲基橙 指示剂,用氨水调至由红 变 第三节 食品中铜的测定 铜是人体必需的微量元素,对造血、细胞生长、某些酶的活性及内发泌等功能有重要作 用,但摄入过多则会发生中毒。铜的盐类比金属铜毒性大。羊口服硫酸铜的一次最低致死量 为 5mg/kg 体重。人口服一次致吐量为 500mg,致死量为 10g。铜的化合物应用很广,在工 业上硫酸铜用作染色,农业上用以配制波尔多液等杀虫剂,医疗上用作眼药;碱性乙酸铜俗 称铜绿,用作油漆颜料、织物染色、杀虫剂、除霉剂等;氧化铜和氧化亚铜常用作玻璃着色 和电镀;碳酸铜用作杀虫剂、颜料、焰火、收敛剂等。食品中铜的来源一般为容器的污染、 杀虫剂、除霉剂的残留以及工业”三废”的污染。 一、食品中铜的允许量标准 (一)我国食品卫生标准 表 4-8 各类食品中铜的允许量标准 标准号 品种 指标(以 Cu 计) mg/kg 或 mg/L 标准号 品种 指标(以 Cu 计) mg/kg 或 mg/L GB2759.1-1996 GB2759.2-1996 GB 5410-85 GB 5411-85 冷冻食品≤ 碳酸饮料≤ 全脂乳粉≤ 脱脂乳粉≤ 5.0 5.0 4.0 4.0 GB 9679-88 GB 11671-89 GB 13099-91 茶叶 ≤ 果类罐头≤ 食品≤ 番茄酱罐头≤ 60.0 5.0 10.0 X2
式中: -样品中锌的含量,mg/kg 或 mg/L。 A3-测定用样品消化液中锌的含量,μg/mL。 A4-试剂空白液中锌的含量,μg/mL。 M2-样品质量(体积),g(mL); V2-样品消化液的总体积,mL。 V3-测定用消化液的体积,mL。 V4-提取液总体积,mL。 (三)二硫腙比色法(一次提取) 1.原理 同二硫腙比色法。 2.试剂 (1)01g/L 二硫腙-四氯化碳溶液。 (2)2g/L 甲基橙指示液:称取 0.2g 甲基橙,用乙醇(20%)溶解并稀释至 100mL。其他 试剂与二硫腙比色法同。 3.仪器 分光光度计。 4.操作方法 (1)样品消化 与二硫腙比色法同。 (2)测定 吸取 5.0~10.0mL 定容的消化液和相同量的试剂空白液,分别置于 125mL 分液漏斗中, 加水至 10mL。 吸取 0.0,1.0,2.0,3.0,4.0,5.0mL 锌标准使用液(相当 0,1.0,2.0,3.0,4.0,5.0μg 锌),分别 置于 125mL 分液漏斗中,各加水至 10mL。 于样品消化液、试剂空白液及锌标准液中各加 1 滴甲基橙 指示剂,用氨水调至由红 变 第三节 食品中铜的测定 铜是人体必需的微量元素,对造血、细胞生长、某些酶的活性及内发泌等功能有重要作 用,但摄入过多则会发生中毒。铜的盐类比金属铜毒性大。羊口服硫酸铜的一次最低致死量 为 5mg/kg 体重。人口服一次致吐量为 500mg,致死量为 10g。铜的化合物应用很广,在工 业上硫酸铜用作染色,农业上用以配制波尔多液等杀虫剂,医疗上用作眼药;碱性乙酸铜俗 称铜绿,用作油漆颜料、织物染色、杀虫剂、除霉剂等;氧化铜和氧化亚铜常用作玻璃着色 和电镀;碳酸铜用作杀虫剂、颜料、焰火、收敛剂等。食品中铜的来源一般为容器的污染、 杀虫剂、除霉剂的残留以及工业”三废”的污染。 一、食品中铜的允许量标准 (一)我国食品卫生标准 表 4-8 各类食品中铜的允许量标准 标准号 品种 指标(以 Cu 计) mg/kg 或 mg/L 标准号 品种 指标(以 Cu 计) mg/kg 或 mg/L GB2759.1-1996 GB2759.2-1996 GB 5410-85 GB 5411-85 冷冻食品≤ 碳酸饮料≤ 全脂乳粉≤ 脱脂乳粉≤ 5.0 5.0 4.0 4.0 GB 9679-88 GB 11671-89 GB 13099-91 茶叶 ≤ 果类罐头≤ 食品≤ 番茄酱罐头≤ 60.0 5.0 10.0 X2
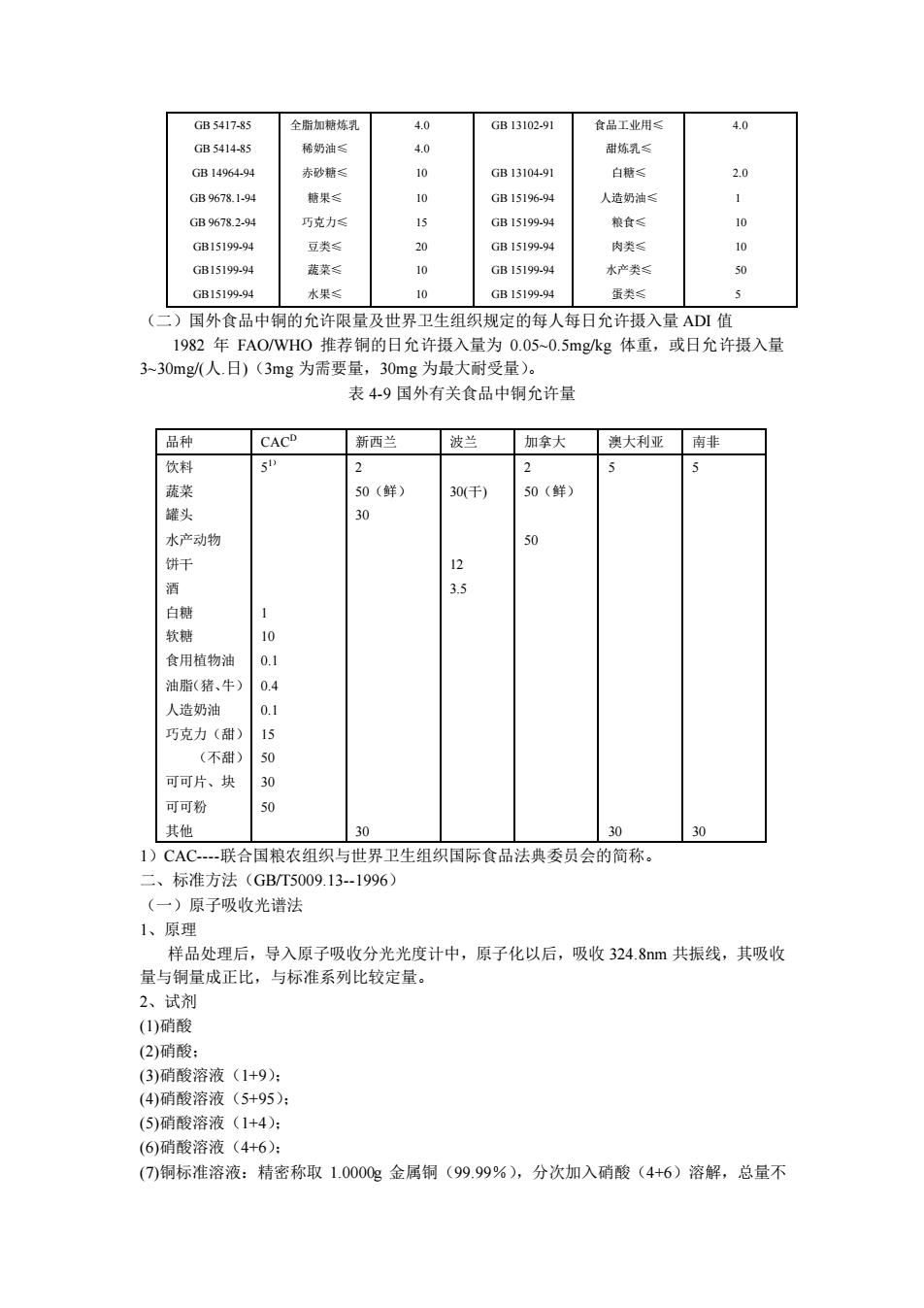
GB 5417-85 GB 5414-85 GB 14964-94 GB 9678.1-94 GB 9678.2-94 GB15199-94 GB15199-94 GB15199-94 全脂加糖炼乳 稀奶油≤ 赤砂糖≤ 糖果≤ 巧克力≤ 豆类≤ 蔬菜≤ 水果≤ 4.0 4.0 10 10 15 20 10 10 GB 13102-91 GB 13104-91 GB 15196-94 GB 15199-94 GB 15199-94 GB 15199-94 GB 15199-94 食品工业用≤ 甜炼乳≤ 白糖≤ 人造奶油≤ 粮食≤ 肉类≤ 水产类≤ 蛋类≤ 4.0 2.0 1 10 10 50 5 (二)国外食品中铜的允许限量及世界卫生组织规定的每人每日允许摄入量 ADI 值 1982 年 FAO/WHO 推荐铜的日允许摄入量为 0.05~0.5mg/kg 体重,或日允许摄入量 3~30mg/(人.日)(3mg 为需要量,30mg 为最大耐受量)。 表 4-9 国外有关食品中铜允许量 品种 CACD 新西兰 波兰 加拿大 澳大利亚 南非 饮料 蔬菜 罐头 水产动物 饼干 酒 白糖 软糖 食用植物油 油脂(猪、牛) 人造奶油 巧克力(甜) (不甜) 可可片、块 可可粉 其他 5 1) 1 10 0.1 0.4 0.1 15 50 30 50 2 50(鲜) 30 30 30(干) 12 3.5 2 50(鲜) 50 5 30 5 30 1)CAC-联合国粮农组织与世界卫生组织国际食品法典委员会的简称。 二、标准方法(GB/T5009.13-1996) (一)原子吸收光谱法 1、原理 样品处理后,导入原子吸收分光光度计中,原子化以后,吸收 324.8nm 共振线,其吸收 量与铜量成正比,与标准系列比较定量。 2、试剂 (1)硝酸 (2)硝酸; (3)硝酸溶液(1+9); (4)硝酸溶液(5+95); (5)硝酸溶液(1+4); (6)硝酸溶液(4+6); (7)铜标准溶液:精密称取 1.0000g 金属铜(99.99%),分次加入硝酸(4+6)溶解,总量不
GB 5417-85 GB 5414-85 GB 14964-94 GB 9678.1-94 GB 9678.2-94 GB15199-94 GB15199-94 GB15199-94 全脂加糖炼乳 稀奶油≤ 赤砂糖≤ 糖果≤ 巧克力≤ 豆类≤ 蔬菜≤ 水果≤ 4.0 4.0 10 10 15 20 10 10 GB 13102-91 GB 13104-91 GB 15196-94 GB 15199-94 GB 15199-94 GB 15199-94 GB 15199-94 食品工业用≤ 甜炼乳≤ 白糖≤ 人造奶油≤ 粮食≤ 肉类≤ 水产类≤ 蛋类≤ 4.0 2.0 1 10 10 50 5 (二)国外食品中铜的允许限量及世界卫生组织规定的每人每日允许摄入量 ADI 值 1982 年 FAO/WHO 推荐铜的日允许摄入量为 0.05~0.5mg/kg 体重,或日允许摄入量 3~30mg/(人.日)(3mg 为需要量,30mg 为最大耐受量)。 表 4-9 国外有关食品中铜允许量 品种 CACD 新西兰 波兰 加拿大 澳大利亚 南非 饮料 蔬菜 罐头 水产动物 饼干 酒 白糖 软糖 食用植物油 油脂(猪、牛) 人造奶油 巧克力(甜) (不甜) 可可片、块 可可粉 其他 5 1) 1 10 0.1 0.4 0.1 15 50 30 50 2 50(鲜) 30 30 30(干) 12 3.5 2 50(鲜) 50 5 30 5 30 1)CAC-联合国粮农组织与世界卫生组织国际食品法典委员会的简称。 二、标准方法(GB/T5009.13-1996) (一)原子吸收光谱法 1、原理 样品处理后,导入原子吸收分光光度计中,原子化以后,吸收 324.8nm 共振线,其吸收 量与铜量成正比,与标准系列比较定量。 2、试剂 (1)硝酸 (2)硝酸; (3)硝酸溶液(1+9); (4)硝酸溶液(5+95); (5)硝酸溶液(1+4); (6)硝酸溶液(4+6); (7)铜标准溶液:精密称取 1.0000g 金属铜(99.99%),分次加入硝酸(4+6)溶解,总量不