
第一章蛋白质 第一节蛋白质的基本结构单位—氨基酸 1.氨基酸的基本结构 1. 2.氨基酸的分类及其结构 (1) 非极性氨基酸:丙氨酸、缬氨酸、亮氨酸、异亮氨酸、 脯氨酸、色氨酸、苯丙氨酸、甲硫氨酸 (2)极性、不带电荷氨基酸:丝氨酸、甘氨酸、苏氨酸、半 胱氨酸、天门冬酰胺、谷氨酰胺、酪氨酸 (3) 酸性氨基酸:天门冬氨酸、谷氨酸 (4) 碱性氨基酸:精氨酸、 赖氨酸、组氨酸 .园 酒体 4蛋 点 。 ,因 文面5 本日6
第一章 蛋白质 第一节 蛋白质的基本结构单位——氨基酸 1.氨基酸的基本结构 1. 2.氨基酸的分类及其结构 (1) 非极性氨基酸:丙氨酸、 缬氨酸、 亮氨酸、 异亮氨酸、 脯氨酸、 色氨酸、 苯丙氨酸、 甲硫氨酸 (2) 极性、不带电荷氨基酸:丝氨酸、 甘氨酸、 苏氨酸、半 胱氨酸、 天门冬酰胺、 谷氨酰胺、 酪氨酸 (3) 酸性氨基酸:天门冬氨酸、 谷氨酸 (4) 碱性氨基酸:精氨酸、 赖氨酸、 组氨酸 1

中原心 商6 文国3 面中 西2 文:夏◆ 片圆悬 3.蛋白质中不常见的氨基酸 4.非蛋白质氨基酸
3.蛋白质中不常见的氨基酸 4.非蛋白质氨基酸 2

"-e 5.氨基酸的理化性质 (1)一般物理学性质 A.外观形状: 无色晶体或粉末状 B.熔点高:200-300℃ C.溶解性质: D.光学性质:旋光活性和紫外吸收 旋光活性:L型和D型氨基酸在旋光仪中的旋光方向相反,但 角度相同。溶液中的氨基酸使平面偏振光偏向左的为左旋异构体, 偏向右的为右旋异构体。 w
5.氨基酸的理化性质 (1) 一般物理学性质 A. 外观形状: 无色晶体或粉末状 B. 熔点高: 200-300 0 C C. 溶解性质: D.光学性质: 旋光活性和紫外吸收 旋光活性:L 型和 D 型氨基酸在旋光仪中的旋光方向相反,但 角度相同。溶液中的氨基酸使平面偏振光偏向左的为左旋异构体, 偏向右的为右旋异构体。 3
色氨酸:279nm苯丙氨酸;259nm酪氨酸:275nm (②)氨基酸的化学性质 A.氨基酸的酸碱性质 plI Net charge pH7 Net charge 0 -n 里w Cationic form Anlonie form B.等电点:pl(等电pH) 在一定的p州条件下,氨基酸分子中所带的正电荷和负电荷数 相等,即净电荷为零,此时溶液的p州称为该氨基酸的等电点 (isoelectric point),用pl表示.氨基酸在等电点时溶解 度最小。 pK值:指某种解离基团有一半被解离时的pH值。 计算pl pl 1/2 pK:+pK2) pl=1/2(pK1+pK2)=12/2.34+9.6)=5.97
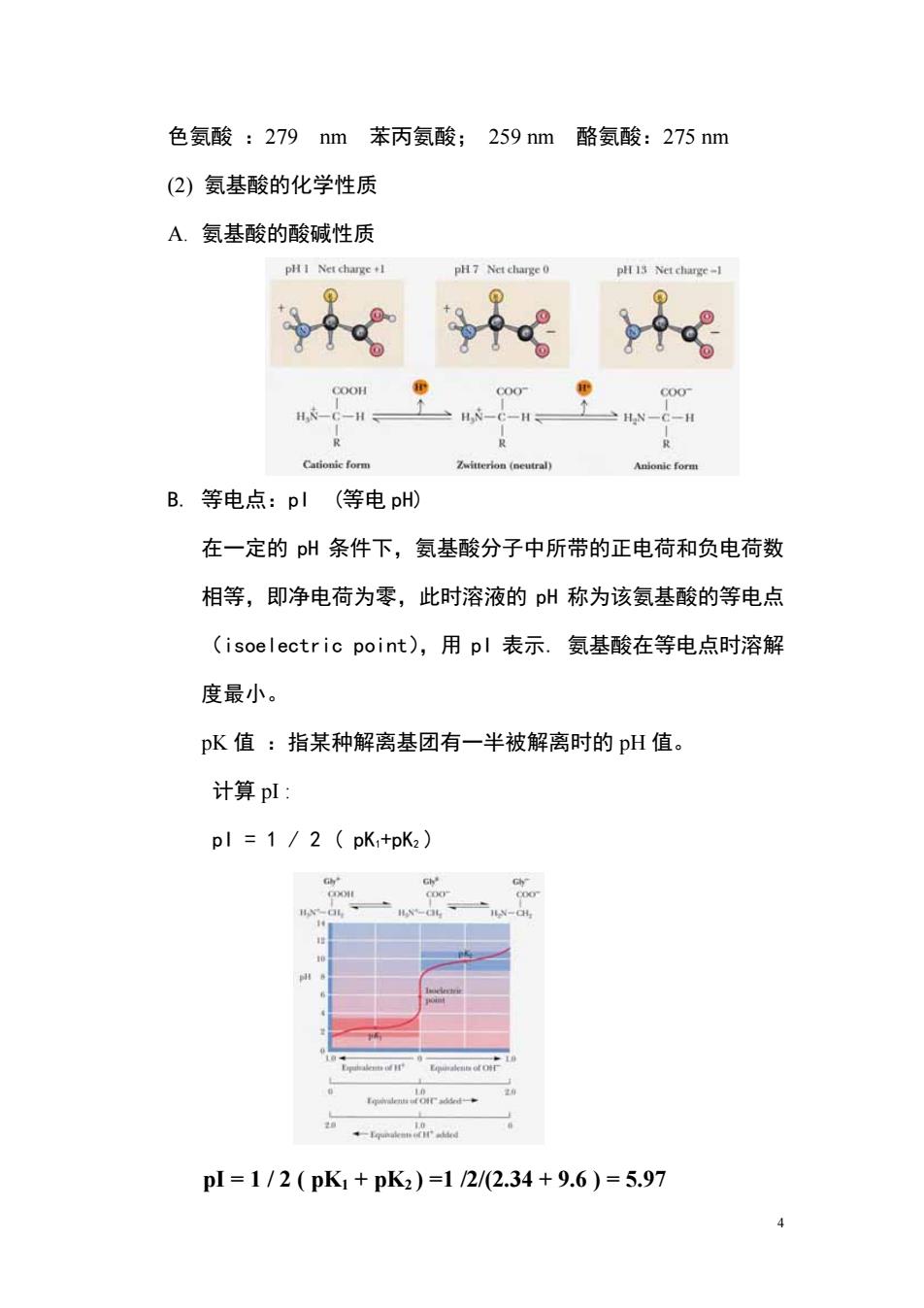
色氨酸 :279 nm 苯丙氨酸; 259 nm 酪氨酸:275 nm (2) 氨基酸的化学性质 A. 氨基酸的酸碱性质 B. 等电点:pI (等电 pH) 在一定的 pH 条件下,氨基酸分子中所带的正电荷和负电荷数 相等,即净电荷为零,此时溶液的 pH 称为该氨基酸的等电点 (isoelectric point),用 pI 表示. 氨基酸在等电点时溶解 度最小。 pK 值 :指某种解离基团有一半被解离时的 pH 值。 计算 pI : pI = 1 / 2 ( pK1+pK2 ) pI = 1 / 2 ( pK1 + pK2 ) =1 /2/(2.34 + 9.6 ) = 5.97 4

6.氨基酸的化学反应 (1)茚三酮反应 (2) 亚硝酸反应 (3) 2.4一二硝基氟苯反应(FDNB) (4) 甲醛的反应 (5) 二甲基氨基萘磺酰氯反应(DNS.CI) (6) 氨基酸与酰化剂(苄氧羰酰氯)的反应 (7) ā-羧基的成酯反应 (8) 侧链基团参加的反应 7.氨基酸的分离和分析鉴定 (1)蛋白质的水解 A.酸水解:6mol/LHC1,110-120℃,24h B.碱水解:5mol/L NaOH110c,24h
6.氨基酸的化学反应 (1) 茚三酮反应 (2) 亚硝酸反应 (3) 2.4—二硝基氟苯反应(FDNB) (4) 甲醛的反应 (5) 二甲基氨基萘磺酰氯反应(DNS - Cl) (6) 氨基酸与酰化剂(苄氧羰酰氯)的反应 (7) α-羧基的成酯反应 (8) 侧链基团参加的反应 7.氨基酸的分离和分析鉴定 (1)蛋白质的水解 A. 酸水解:6 mol/L HCl, 110 –120 0 C , 24 h B. 碱水解:5 mol/L NaOH 110 0 C , 24 h 5