
该理论认为反应物分子间相互作用的势能是分子间相对位置的函数,在反应物转变为产物的过程中,系统的势能不断变化。因此,画出反应过程中是势能变化的势能面图,可以从中找到最佳的反应途径该理论认为反应物分子间相互作用的势能是分子间相对位置的函数E, = E, (r)莫尔斯(Morse)公式是对双原子分子最常用的计算势能E,的经验公式:E,(r)= D.[expi-2a(r -r))-2exp/-a(r -r))]式中ro是分子中双原子分子间的平衡核间距,D.是势能21曲线的并深,α为与分子结构有关的常数物理化学(B)I
21 物理化学(B)II 该理论认为反应物分子间相互作用的势能是分子间相对位置的函 数,在反应物转变为产物的过程中,系统的势能不断变化。因此,画 出反应过程中是势能变化的势能面图,可以从中找到最佳的反应途径 。 该理论认为反应物分子间相互作用的势能是分子间 相对位置的函数 E E r p p = ( ) 莫尔斯(Morse)公式是对双原子分子最常用的计算势能 Ep的经验公式: p e 0 0 E r D a r r a r r ( ) [exp{ 2 ( )} 2exp{ ( )}] = − − − − − 式中r0是分子中双原子分子间的平衡核间距,De是势能 曲线的井深,a为与分子结构有关的常数
ODoDV=0双原子分子的莫尔斯势能曲线物理化学(B)II2025/4/
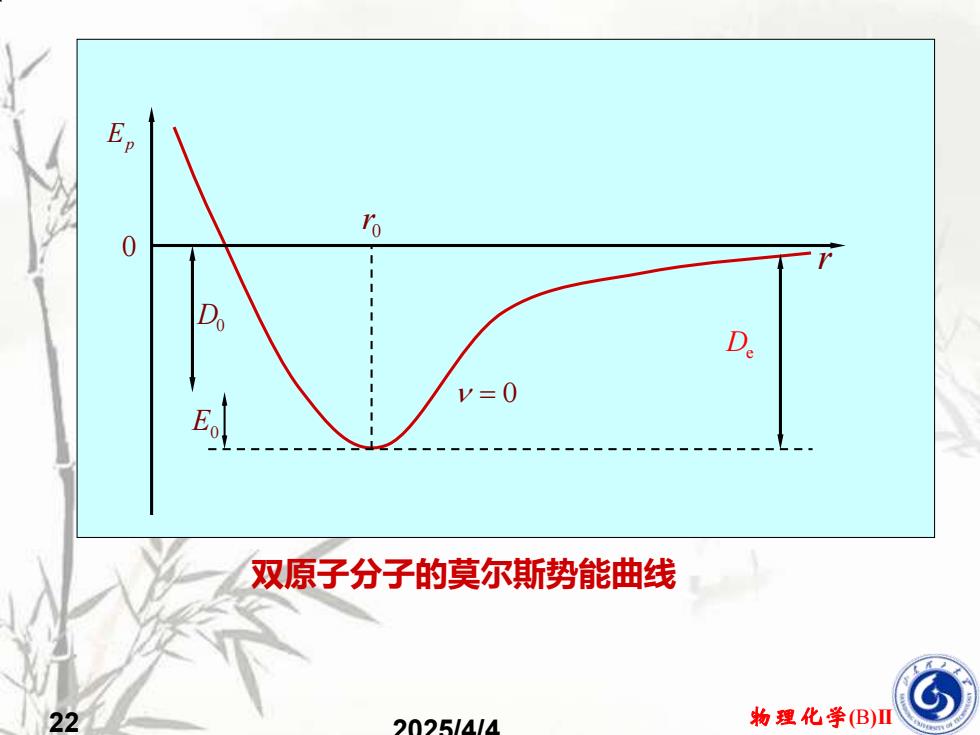
22 物理化学(B)II 2025/4/4 双原子分子的莫尔斯势能曲线 Ep 0 r = 0 De E0 D0 0 r
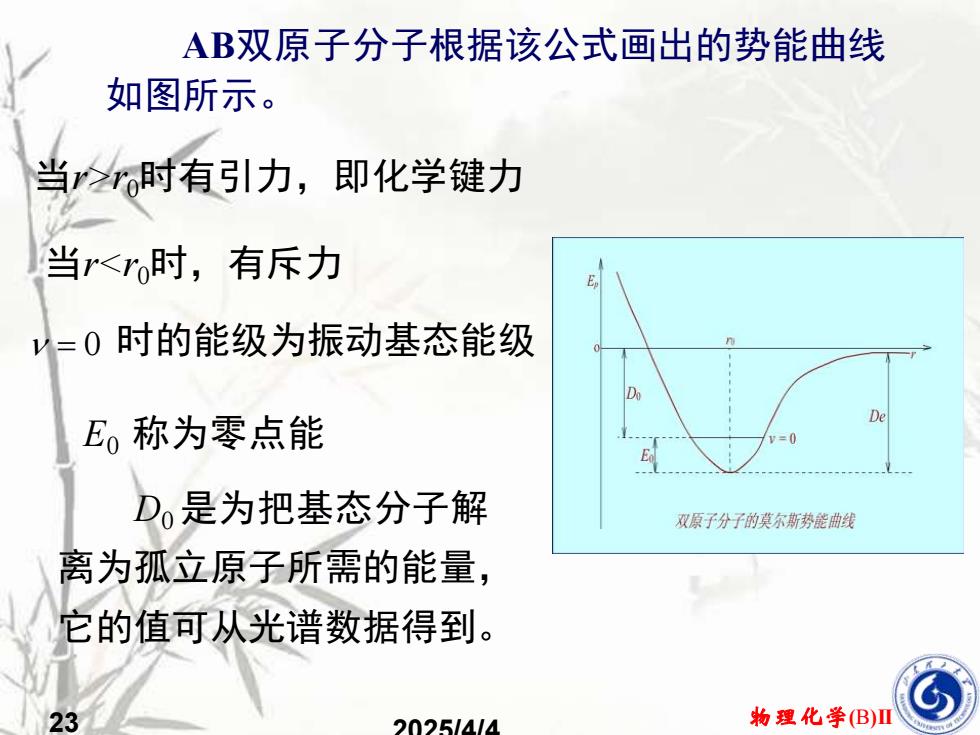
AB双原子分子根据该公式画出的势能曲线如图所示,当r>r时有引力,即化学键力当r<ro时,有斥力V=0时的能级为振动基态能级DeE。称为零点能Do是为把基态分子解双原子分子的莫尔斯势能曲线离为孤立原子所需的能量它的值可从光谱数据得到。物理化学(B)II232025/4/4
23 物理化学(B)II 2025/4/4 当r>r0时有引力,即化学键力 = 0 时的能级为振动基态能级 AB双原子分子根据该公式画出的势能曲线 如图所示。 当r<r0时,有斥力 D0 是为把基态分子解 离为孤立原子所需的能量, 它的值可从光谱数据得到。 E0 称为零点能

以三原子反应为例:A+B-C -[A-..B...C →A-B+C当A原子与双原子分子BC反应时,首先形成三原子分子的活化络合物,该络合物的势能是3个内坐标的函数Ep = Ep(rAB,rBc,r或Ep = Ep(rAB,rBC,ABC,这要用四维图表示物理化学(B)I242025/4/4
24 物理化学(B)II 2025/4/4 以三原子反应为例: 当A原子与双原子分子BC反应时,首先形成三 原子分子的活化络合物,该络合物的势能是3个内 坐标的函数 P P AB BC CA E E r r r = ( , , ) 这要用四维图表示 P P AB BC ABC 或 ( , , ) E E r r =
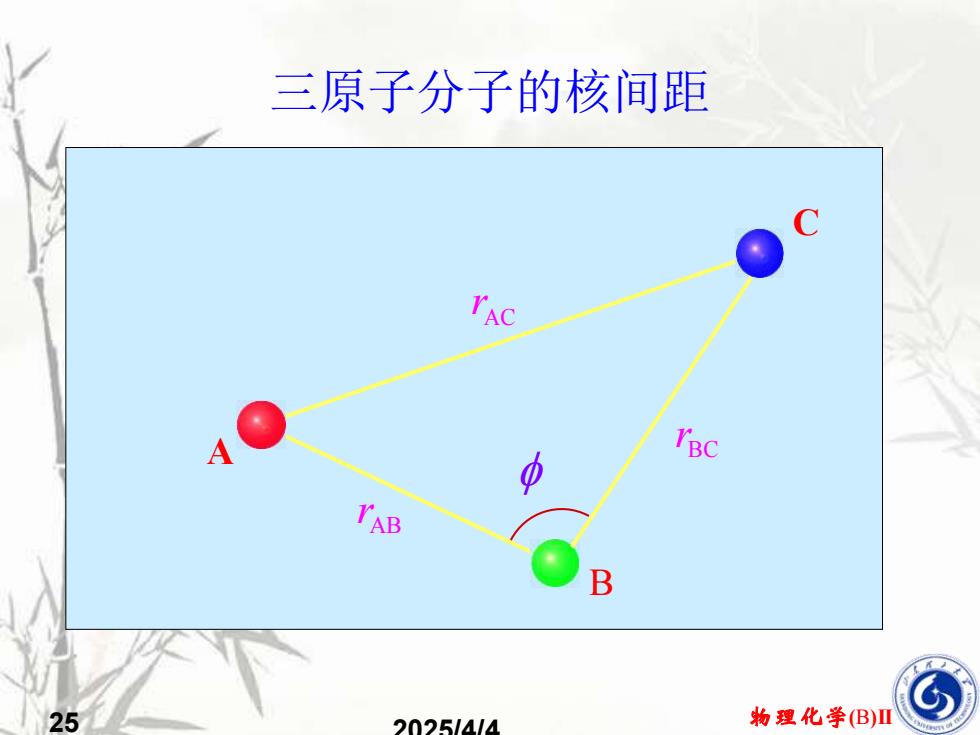
三原子分子的核间距BCYABB物理化学(B)II252025/4/4
25 物理化学(B)II 2025/4/4 三原子分子的核间距 AB r AC r A B C BC r