
(一)滴定前(Vb=0) [H+ ]=ca=0.1000mol·L-1 ,pH=1.00 (二)滴定开始至计量点前(Va>Vb) [H+ ]=( Va -Vb )/( Va+Vb )·ca 若 Vb=19.98ml (-0.1%相对误差) [H+ ]=5.00×10-5mol·L-1 , pH=4.30 (三)计量点时(Va=Vb) [H+ ]=1.0×10-7mol·L-1 , pH=7.00 (四)计量点后(Vb>Va) 计量点之后,NaOH再继续摘入便过量了,溶液的 酸度决定于过量的NaOH的浓度。 [OH- ]=( Vb -Va )/( Va+Vb )·cb 若 Vb=20.02ml (+0.1%相对误差) [OH- ]=5.00×10-5mol·L-1 pH=9.70
(一)滴定前(Vb=0) [H+ ]=ca=0.1000mol·L-1 ,pH=1.00 (二)滴定开始至计量点前(Va>Vb) [H+ ]=( Va -Vb )/( Va+Vb )·ca 若 Vb=19.98ml (-0.1%相对误差) [H+ ]=5.00×10-5mol·L-1 , pH=4.30 (三)计量点时(Va=Vb) [H+ ]=1.0×10-7mol·L-1 , pH=7.00 (四)计量点后(Vb>Va) 计量点之后,NaOH再继续摘入便过量了,溶液的 酸度决定于过量的NaOH的浓度。 [OH- ]=( Vb -Va )/( Va+Vb )·cb 若 Vb=20.02ml (+0.1%相对误差) [OH- ]=5.00×10-5mol·L-1 pH=9.70
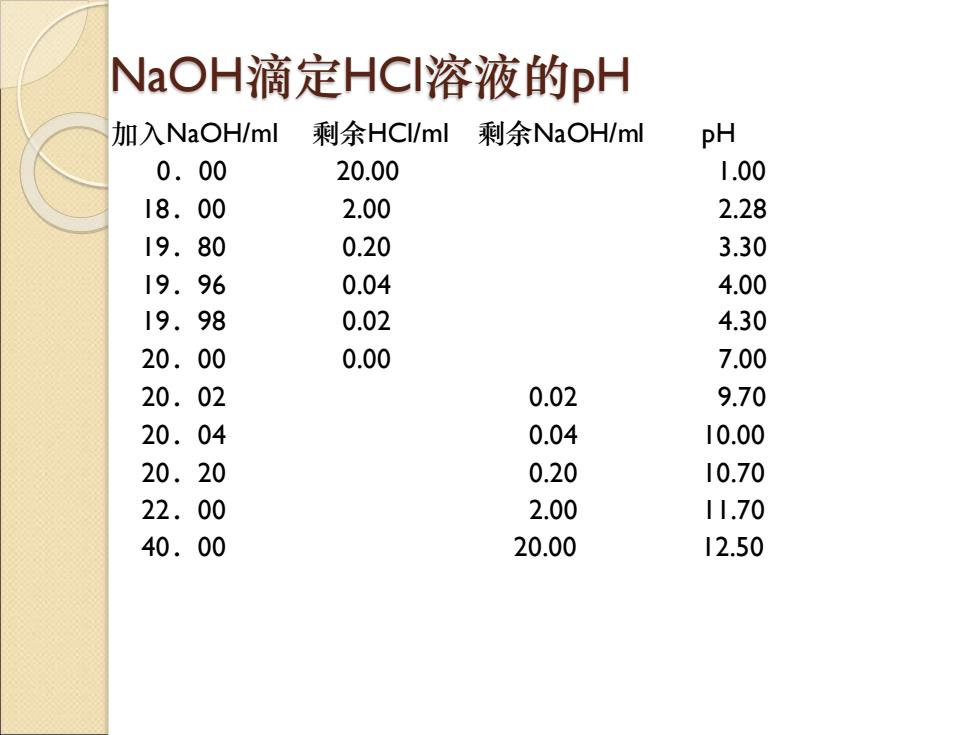
NaOH滴定HCl溶液的pH 加入NaOH/ml 剩余HCl/ml 剩余NaOH/ml pH 0.00 20.00 1.00 18.00 2.00 2.28 19.80 0.20 3.30 19.96 0.04 4.00 19.98 0.02 4.30 20.00 0.00 7.00 20.02 0.02 9.70 20.04 0.04 10.00 20.20 0.20 10.70 22.00 2.00 11.70 40.00 20.00 12.50
NaOH滴定HCl溶液的pH 加入NaOH/ml 剩余HCl/ml 剩余NaOH/ml pH 0.00 20.00 1.00 18.00 2.00 2.28 19.80 0.20 3.30 19.96 0.04 4.00 19.98 0.02 4.30 20.00 0.00 7.00 20.02 0.02 9.70 20.04 0.04 10.00 20.20 0.20 10.70 22.00 2.00 11.70 40.00 20.00 12.50
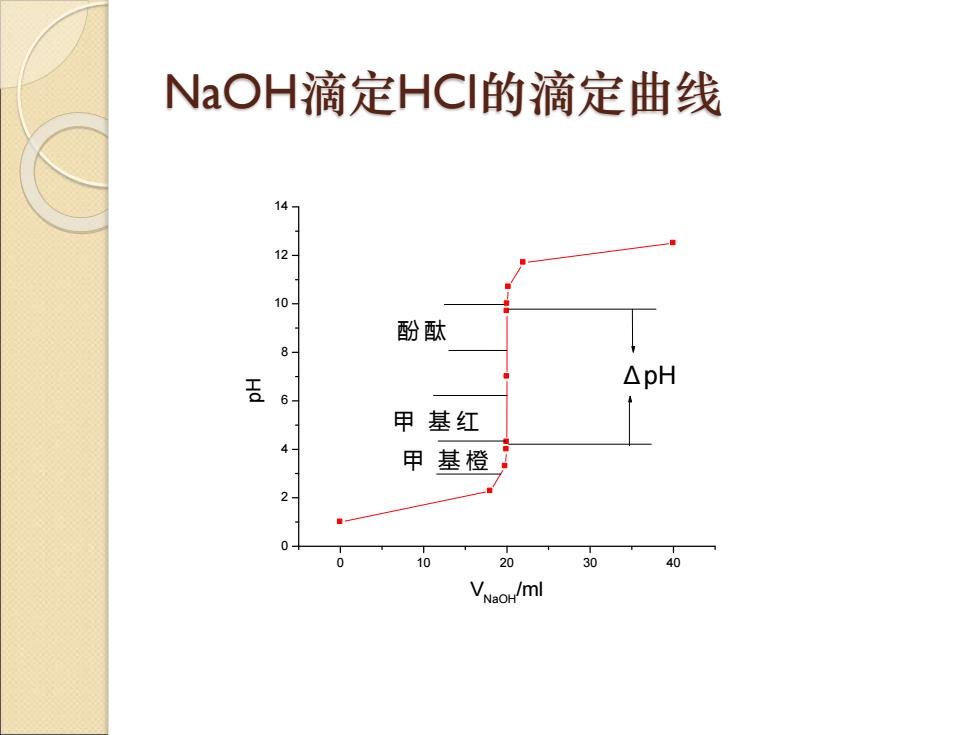
NaOH滴定HCl的滴定曲线 0 10 20 30 40 0 2 4 6 8 10 12 14 甲 基 橙 甲 基 红 酚 酞 Δ pH pH VNaOH/ml
NaOH滴定HCl的滴定曲线 0 10 20 30 40 0 2 4 6 8 10 12 14 甲 基 橙 甲 基 红 酚 酞 Δ pH pH VNaOH/ml

2.pH值的突跃范围 计量点前后± 0.1%相对误差范围内溶液pH值之变化, 在分析化学中称为滴定的pH突跃范围,简称突跃范 围。 3.指示剂的选择 滴定的突跃范围是选择指示剂的依据。选择在滴定 突跃范围内发生变化的指示剂,即凡变色点的pH值 处于滴定突跃范围内的指示剂均适用,都能使滴定 保证足够的准确度(相对误差在0.1%以内)。对本 例来说,如图pH值的突跃范围为4.30-9.70,由表4- 1可知能用的指示剂较多,如酚酞、甲基红、甲基橙。 4.浓度的影响 溶液浓度越大,突跃范围越大,可供选择的指示 就越多;反之,溶液越稀,突跃范围越小,可供选 择的指示剂就越少。因此,常用的标准溶液的浓度 一般采用0.1-1mol·L-1。否则太浓,试剂取量太多; 太稀,则突跃又不明显,指示剂的选择也比较困难
2.pH值的突跃范围 计量点前后± 0.1%相对误差范围内溶液pH值之变化, 在分析化学中称为滴定的pH突跃范围,简称突跃范 围。 3.指示剂的选择 滴定的突跃范围是选择指示剂的依据。选择在滴定 突跃范围内发生变化的指示剂,即凡变色点的pH值 处于滴定突跃范围内的指示剂均适用,都能使滴定 保证足够的准确度(相对误差在0.1%以内)。对本 例来说,如图pH值的突跃范围为4.30-9.70,由表4- 1可知能用的指示剂较多,如酚酞、甲基红、甲基橙。 4.浓度的影响 溶液浓度越大,突跃范围越大,可供选择的指示 就越多;反之,溶液越稀,突跃范围越小,可供选 择的指示剂就越少。因此,常用的标准溶液的浓度 一般采用0.1-1mol·L-1。否则太浓,试剂取量太多; 太稀,则突跃又不明显,指示剂的选择也比较困难

反之,若用HCl滴定NaOH(条件与前相同), 滴定曲线正好相反。滴定的突跃范围是从pH= 9.70-4.30,可选择酚酞和甲基红作指示剂。如 果用甲基橙作指示剂,只应滴至橙色(pH=4.0), 若滴至红色(pH=3.1),将产生+0.2%以上的误 差。为消除这种误差,可进行指示剂校正,即 取40毫升0.05 mol·L- NaCl溶液,加入与滴定时 相同量的甲基橙,再以0.1000 mol·L- HCl溶液 滴定至溶液的颜色恰好与被滴定的溶液颜色相 同为止,记下HCl的用量(称为校正值)。滴定 NaOH所消耗的HCl用量减去此校正值即HCl真 正的用量。 滴定的突跃范围,随滴定剂和被滴定物浓 度的改变而改变,指示剂的选择也应视具体情 况而定
反之,若用HCl滴定NaOH(条件与前相同), 滴定曲线正好相反。滴定的突跃范围是从pH= 9.70-4.30,可选择酚酞和甲基红作指示剂。如 果用甲基橙作指示剂,只应滴至橙色(pH=4.0), 若滴至红色(pH=3.1),将产生+0.2%以上的误 差。为消除这种误差,可进行指示剂校正,即 取40毫升0.05 mol·L- NaCl溶液,加入与滴定时 相同量的甲基橙,再以0.1000 mol·L- HCl溶液 滴定至溶液的颜色恰好与被滴定的溶液颜色相 同为止,记下HCl的用量(称为校正值)。滴定 NaOH所消耗的HCl用量减去此校正值即HCl真 正的用量。 滴定的突跃范围,随滴定剂和被滴定物浓 度的改变而改变,指示剂的选择也应视具体情 况而定