
3)有效温差:△=N△"=0.668+18.0=18.7℃■△t=100-41.6=58.4℃△t=△t-△=58.4-18.7=39.7℃(4)溶液的沸点:t=△+ T=18.7+41.6=60.3℃
◼ (3)有效温差: ◼ Δ= +Δ″=0.668+18.0=18.7 ℃ ◼ Δt0 =100-41.6=58.4 ℃ ◼ Δt=Δt0-Δ=58.4-18.7=39.7 ℃ ◼ (4)溶液的沸点: ◼ t=Δ+ =18.7+41.6=60.3℃ ' ' T

2.2 单效蒸发的计算
2.2 单效蒸发的计算
2.2.1蒸发器的物料衡算单效蒸发如图所示,作溶质的衡WT.H算,有:Fx=(F-W)x1整理得:W=F(1-xo/x或蒸发室FxoXi=F-WFxalaho式中:F-进料量,kg/s;DTHTovW-水分蒸发量,kg/s;加热室X-原料液中溶质的质量分数(F-W).)小hXi-完成液(即浓缩液)中溶质的质量分数D.Tahw
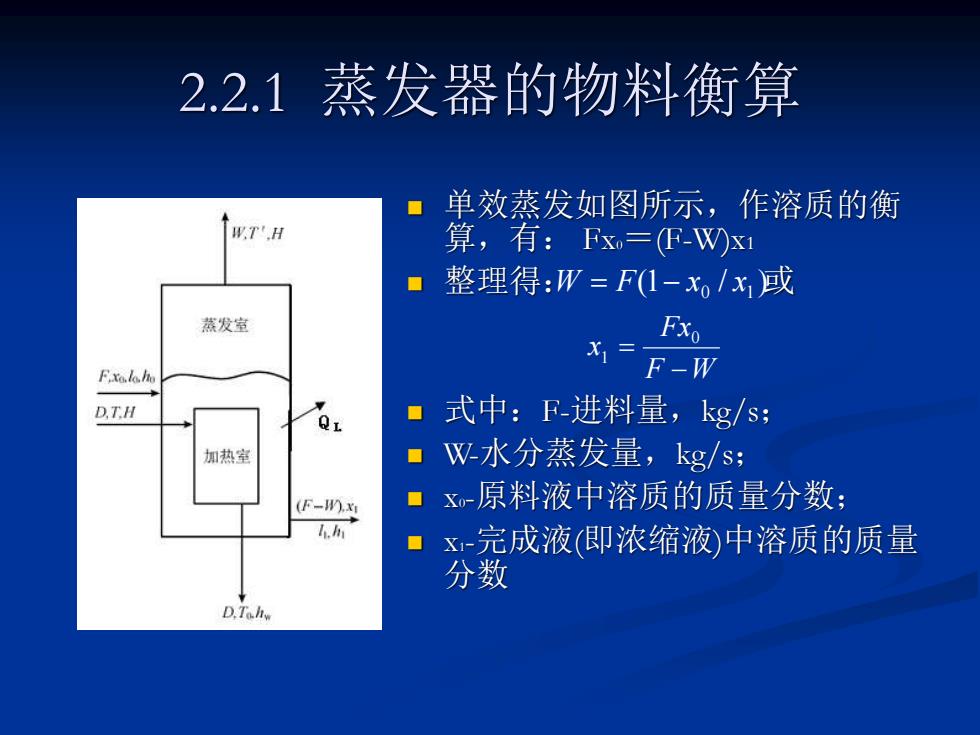
2.2.1 蒸发器的物料衡算 ◼ 单效蒸发如图所示,作溶质的衡 算,有: Fx0=(F-W)x1 ◼ 整理得: 或 ◼ 式中:F-进料量,kg/s; ◼ W-水分蒸发量,kg/s; ◼ x0-原料液中溶质的质量分数; ◼ x1-完成液(即浓缩液)中溶质的质量 分数 (1 / ) 0 1 W = F − x x F W Fx x − = 0 1

2.2.2 蒸发器的热量衡算对蒸发器作饸衡算,有:DH+Fh=WH'+(F-W)h.+Dhw+Q.或Q=D(H-hw)=WH+(F-W)hi-Fho+Q由于食品生产中的溶液大多为有机溶液,稀释热很小,可略去不计,则溶液的烩可用比热容计算,取0℃的液体的恰值为零,则有:hw=CpwTO;ho=Cpoto;hi=CpitiD(H-CpwT)=WH+(F-W)Cpti-FCmt+Q溶液的比热容由下面经验公式求取:Cp=Cpw(1-x)+CpBX式中:Cpw和CpB分别为水和溶质的比热容,J/(kgK)。当x<0.2时,上式可简化为Cp=Cpw (1-x)
2.2.2 蒸发器的热量衡算 ◼ 对蒸发器作焓衡算,有:DH+Fh0=WH′+(F-W) h1+DhW+QL或 Q=D(H-hW)=WH′+(F-W)h1-Fh0+QL ◼ 由于食品生产中的溶液大多为有机溶液,稀释热很小,可 略去不计,则溶液的焓可用比热容计算,取0℃的液体的 焓值为零,则有: hW=CPWT0; h0=CP0t0;h1=CP1t1 ◼ D(H- CPWT0)=WH′+(F-W) CP1t1-FCP0t0+QL ◼ 溶液的比热容由下面经验公式求取:Cp = CPW (1-x)+ CPB x ◼ 式中:CPW和CPB分别为水和溶质的比热容,J/(kg·K)。 ◼ 当x<0.2时,上式可简化为 ◼ CP=CPW (1-x)

据此可推得:(F-W)CpiFCpo-WCplw设加热蒸汽的冷凝液在饱和温度下排出,则:H-CpwT=r及H-Cpwti-r,代入上式整理得:Q=Dr=Wi+FCpo(ti-to)+Qt或Q=Dr=(1+a%)[W'+FCpo (ti-to)]式中:Q-蒸发器的热负荷,J/s或WD-加热蒸汽的消耗量,kg/s;r-加热蒸汽的汽化潜热,J/kg;r-二次蒸汽的汽化潜热,J/kg;
◼ 据此可推得:(F-W) CP1=FCP0-WCPW ◼ 设加热蒸汽的冷凝液在饱和温度下排出,则: H-CPWT=r及H′-CPWt1≈r′,代入上式整理得:Q =Dr =Wr′+FCP0 (t1-t0) +QL或 Q=Dr=(1+a%) [Wr′+FCP0 (t1-t0)] ◼ 式中:Q-蒸发器的热负荷,J/s或W; ◼ D-加热蒸汽的消耗量,kg/s; ◼ r-加热蒸汽的汽化潜热,J/kg; ◼ r′-二次蒸汽的汽化潜热,J/kg;