Ag20 ②在艾林罕姆图上, +250 Cuo 一个氧化物的生成自由 能负值越大,则金属一 C0→c0, 氧化物的线在图中的位 置就越靠下。相反,氧 FeO C→C02 化物生成自由能值负值 00 越小。则其金属一氧化 物线在图上的位置就越 SiO2 靠上。这就是说。根据 Al203 Mgo Cao 图上各种线的位置的高 -1000 低就可判断出这些氧化 物稳定性的相对大小。 500 10001500 2000 2500 温度 显然,金属一氧化物的 图氧化物的Ellingham图 线位置越低,意味着该 氧化物就越稳定
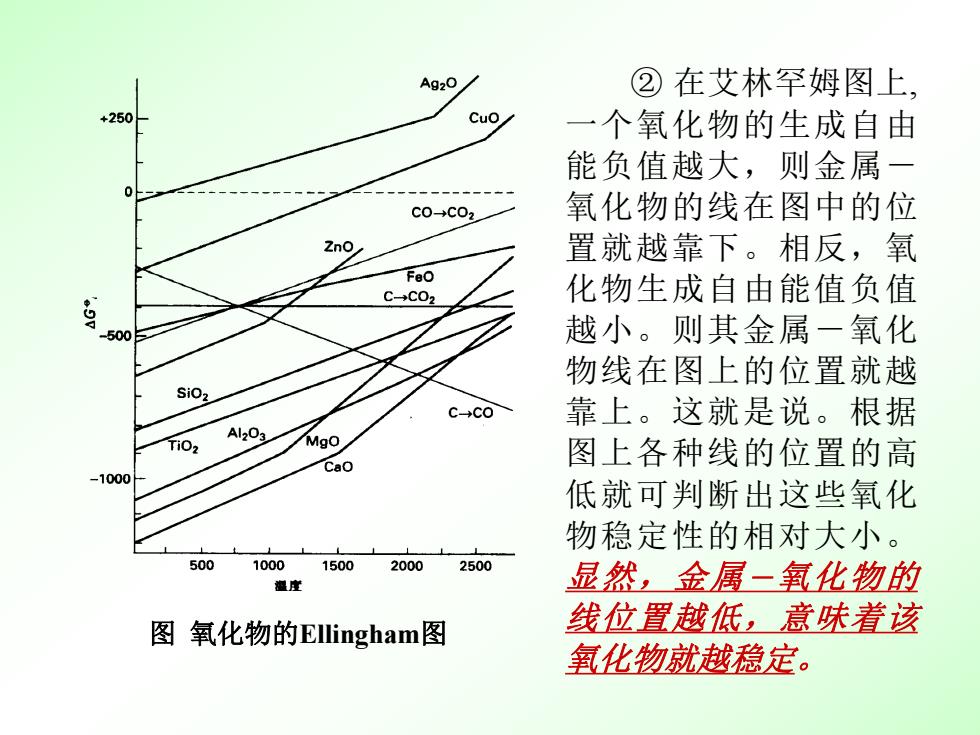
② 在艾林罕姆图上, 一个氧化物的生成自由 能负值越大,则金属- 氧化物的线在图中的位 置就越靠下。相反,氧 化物生成自由能值负值 越小。则其金属-氧化 物线在图上的位置就越 靠上。这就是说。根据 图上各种线的位置的高 低就可判断出这些氧化 物稳定性的相对大小。 显然,金属-氧化物的 线位置越低,意味着该 氧化物就越稳定。 图 氧化物的Ellingham图
Ag20 +250 Cuo ③如若一个还原反应能够 发生,必须是艾林罕姆图上位 c0-→C02 于下面的金属与位于上面的金 属氧化物之间相互作用的结果 C-C02 。反之,位于上面的金属与位 -500 于下面的金属氧化物之间的反 SiO2 应将不发生。 C→C0 A03 Mgo 表明位于下面的金属还原 Cao 100( 性强。 根据这个原则,从艾林罕 500 100015002000 2500 姆图可以排列出常见还原剂如 图氧化物的Ellingham图 在1073K时的相对强弱次序: Ca>Mg>Al>Ti>Si>Zn>Fe.(左图) 同理,常见氧化剂在1073K的强弱次序: Ag20>Cu0>Fe0>ZnO>Si02>TiO2.(左图)
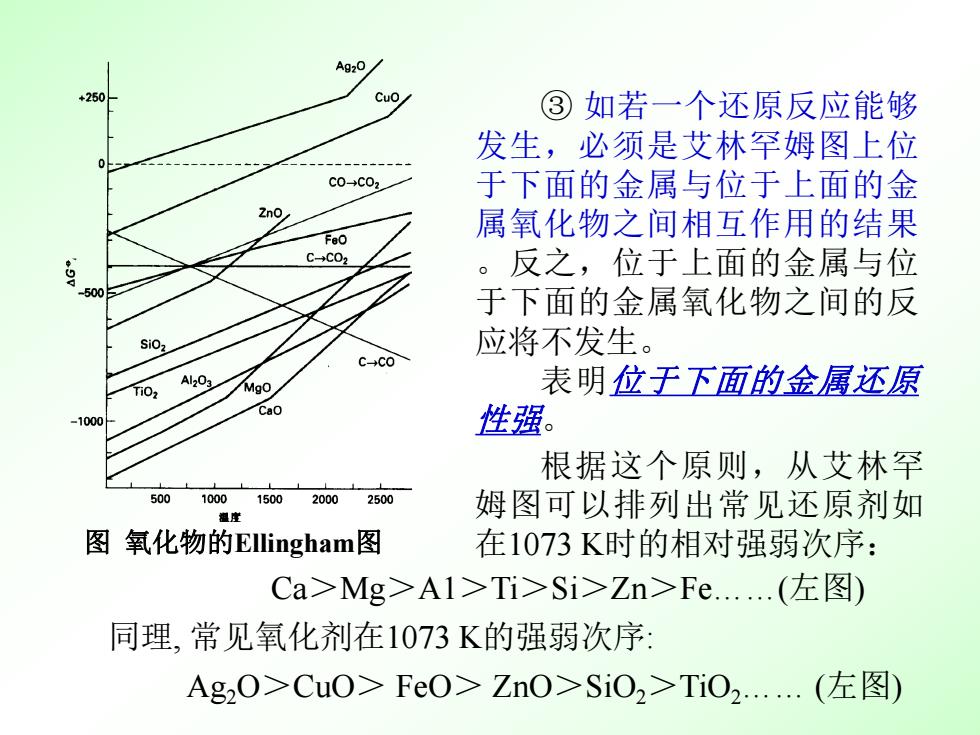
Ca>Mg>A1>Ti>Si>Zn>Fe.(左图) 同理, 常见氧化剂在1073 K的强弱次序: Ag2O>CuO> FeO> ZnO>SiO2>TiO2. (左图) 根据这个原则,从艾林罕 姆图可以排列出常见还原剂如 在1073 K时的相对强弱次序: ③ 如若一个还原反应能够 发生,必须是艾林罕姆图上位 于下面的金属与位于上面的金 属氧化物之间相互作用的结果 。反之,位于上面的金属与位 于下面的金属氧化物之间的反 应将不发生。 表明位于下面的金属还原 性强。 图 氧化物的Ellingham图
④对大多数金属氧化物的生 +250 Cuo 成来说,如2M(s)+O2(g)2MO ($),由于消耗氧气的反应是熵减 少的反应,因而直线有正的斜率 C0→C02 ,但对反应2C(s)+O2(g)一→2C0(g) Zn0 来说,气体分子数增加,是熵增的 C→C02 反应,故C→CO线有负的斜率。 500 这样,C→CO线将与许多金属一 SiOz 金属氧化物线会在某一温度时相 Al203 交。 TiO2 Mgo Cao 这意味着在低于该温度时, -1000 C0不如金属氧化物稳定;但在高 于该温度时,CO的稳定性大于该 500 10001500 2000 2500 金属氧化物,因而在高于该温度时, 图氧化物的Ellingham图 C可以将该金属从其氧化物中还原 出来
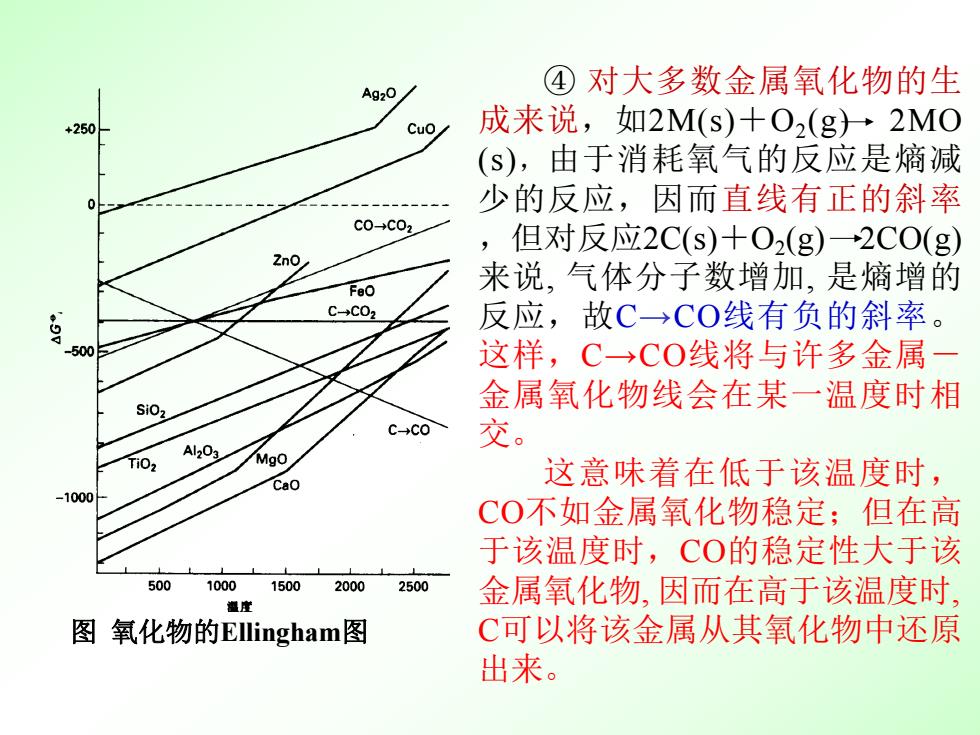
图 氧化物的Ellingham图 ④ 对大多数金属氧化物的生 成来说,如2M(s)+O2(g) 2MO (s),由于消耗氧气的反应是熵减 少的反应,因而直线有正的斜率 ,但对反应2C(s)+O2(g) 2CO(g) 来说, 气体分子数增加, 是熵增的 反应,故C→CO线有负的斜率。 这样,C→CO线将与许多金属- 金属氧化物线会在某一温度时相 交。 这意味着在低于该温度时, CO不如金属氧化物稳定;但在高 于该温度时,CO的稳定性大于该 金属氧化物, 因而在高于该温度时, C可以将该金属从其氧化物中还原 出来
举C还原A12O3为例:从左图可以 Cuo 发现,在低于2100K温度时,C→CO 线位于A1→AlO3线之上,表明AlO? 的生成自由能比CO要负,所以在低 c0→C02 于2100K时,C不能用作A12O3的还原 剂。但当温度超过2100K时CO的生 成自由能比A1,O,的要负,即C在大于 C→C02 9 2100K时能从A12O,中夺取氧而使 500 A1203还原。 SiOz 再看C还原SiO,的温度范围。在 C→C0 Al203 低温,如273K时,CO的生成自由能 TiO2 MgO 大于SO,的生成自由能,所以在此温 -1000 度下,C不能还原SO2;但当温度约 在1673K时两线相交,超过此温度时 500 10001500 2000 2500 CO的生成自由能低于SiO,的生成自 温度 图氧化物的Cllingham图 由能,故在T>1673K时,C还原SiO, 的反应可以发生
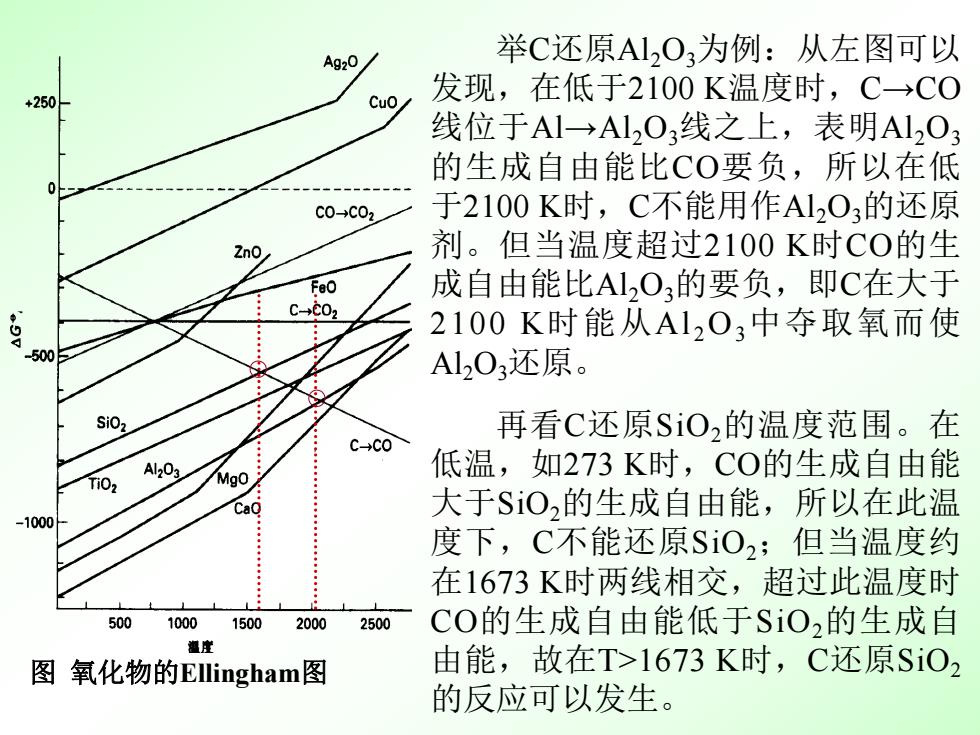
举C还原Al2O3为例:从左图可以 发现,在低于2100 K温度时,C→CO 线位于Al→Al2O3线之上,表明Al2O3 的生成自由能比CO要负,所以在低 于2100 K时,C不能用作Al2O3的还原 剂。但当温度超过2100 K时CO的生 成自由能比Al2O3的要负,即C在大于 2100 K时能从Al 2O3中夺取氧而使 Al2O3还原。 再看C还原SiO2的温度范围。在 低温,如273 K时,CO的生成自由能 大于SiO2的生成自由能,所以在此温 度下,C不能还原SiO2;但当温度约 在1673 K时两线相交,超过此温度时 CO的生成自由能低于SiO2的生成自 由能,故在T>1673 K时,C还原SiO2 的反应可以发生。 图 氧化物的Ellingham图

根据艾林罕姆图可以选择金属氧化物的还原方法,亦即金属 提取的一般方法的依据。 ①氧化物热分解法 Ag2O 位于艾林罕姆图上端的Ag 25 Cuo →Ag2O和Hg→Hg0(图上未示出) 线,在273K时位于△G=0线的 C0→C02 下方,即在273K时,这些氧化物 Zn0 的标准生成自由能是负值。但温 C→C02 度升高,如升到673K以上,这时 500 两条线均越过△G=0的线,即在 SiO2 C-CO 673K时,△G>0。这一变化意味 Ti024,03 Mgo 着Ag2O、HgO在温度升高时会自 -1000 Cao 动分解。所以对这些不活泼的金 属氧化物就可以采用氧化物的热 500 1000150020002500 分解法来获得金属。 图氧化物的Ellingham图
根据艾林罕姆图可以选择金属氧化物的还原方法,亦即金属 提取的一般方法的依据。 ① 氧化物热分解法 位于艾林罕姆图上端的Ag →Ag2O和Hg→HgO(图上未示出) 线, 在273 K时位于△Gθ=0线的 下方, 即在273 K时, 这些氧化物 的标准生成自由能是负值。但温 度升高, 如升到673 K以上, 这时 两条线均越过△Gθ=0的线, 即在 673 K时, △Gθ>0。这一变化意味 着Ag2O、HgO在温度升高时会自 动分解。所以对这些不活泼的金 属氧化物就可以采用氧化物的热 分解法来获得金属。 图 氧化物的Ellingham图