
第五章 化学平衡 Chemical equilibrium 范霍夫平衡箱 dD+eE。=+gG P'D PE P'F P'G
第五章 化学平衡 Chemical equilibrium

5.1化学平衡的条件和反应的亲和势 5.1.1化学反应的方向和限度 在600℃和100kPa下: C.HsC2Hs(g)C.H5C2H3(g)+H2(g) 乙苯的最大转换率不会超过72.8。 5.1.2化学反应的摩尔吉布斯函数变] 设有一任意的封闭系统,无非体积功, dG=-SdT+Vdp+ΣB LB dnB 在定温定压下, dG=∑B UB dnB
5.1 化学平衡的条件和反应的亲和势 5.1.1 化学反应的方向和限度 在600℃和100kPa下: C6H5C2H5 (g) C6H5C2H3 (g)+H2 (g) 乙苯的最大转换率不会超过72.8。 5.1.2 化学反应的摩尔吉布斯函数[变] 设有一任意的封闭系统,无非体积功, dG=-SdT+Vdp+∑B mB dnB 在定温定压下, dG=∑B mB dnB

aA+bByY+zZ 0=yY+zZ-aA-bB 0=∑BBB dξ= dnB 或者 dnB=veds VB dG=∑BBBd5 (yy十4z-a4A-b4B)dξ G def =∑e4=A,Cn亿,p.) T.P 称为化学反应的摩尔吉布斯函数!变引△Gm(molar Gibbs function of chemical reaction) △Gm的SI单位为Jmol-1
aA+bB yY+zZ 0=yY+zZ-aA-bB 0=∑B nB B B d B d n x n = 或者 dnB =nBdx dG=∑B nBmBdx =(ymY+zmZ-amA-bmB)dx n m ( x ) x G T , p, G T ,p B B B r m def = = D ÷ ÷ ø ö ç ç è æ ¶ ¶ å 称为化学反应的摩尔吉布斯函数[变] △rGm (molar Gibbs function of chemical reaction) △rGm的SI单位为J·mol-1

△Gm的物理意义是: 在T、p、时(即在一定的温度、压力和组成的 条件下),把发生d飞的微量反应进度折合成发生单 位反应进度时所引起的系统吉布斯函数变化: 或者在T、p、飞时,含物质的量很大的反应系 统中发生单位反应进度时系统吉布斯函数的变化
△rGm的物理意义是: • 在T、p、x时(即在一定的温度、压力和组成的 条件下),把发生dx 的微量反应进度折合成发生单 位反应进度时所引起的系统吉布斯函数变化; • 或者在T、p、x 时,含物质的量很大的反应系 统中发生单位反应进度时系统吉布斯函数的变化
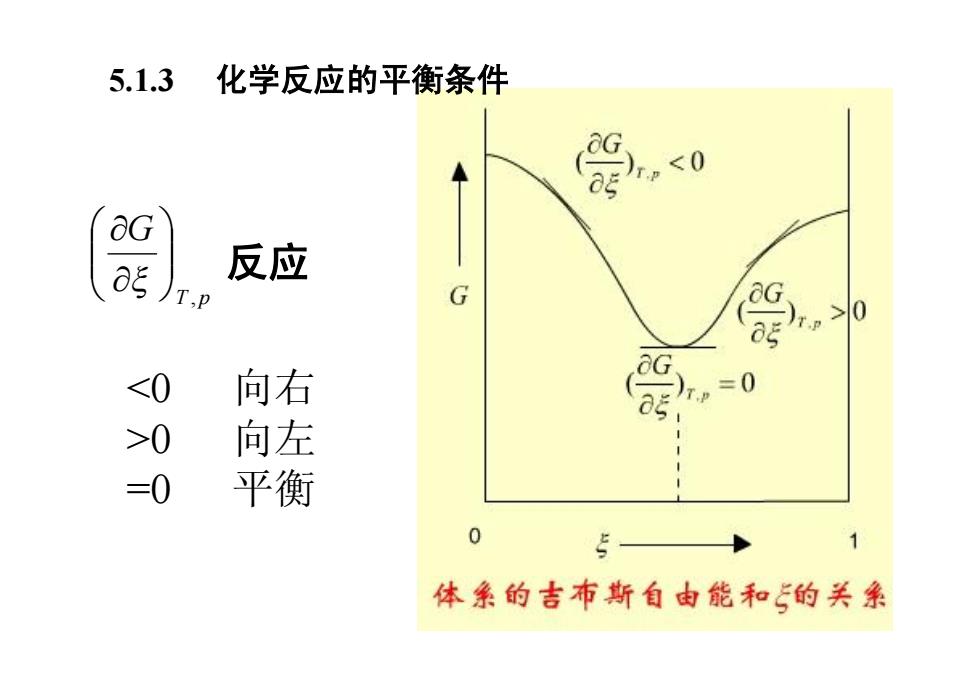
5.1.3 化学反应的平衡条件 OG 5 反应 G .0 <0 向右 >0 向左 =0 平衡 0 5 体系的吉布斯自由能和的关系
5.1.3 化学反应的平衡条件 T p G , ÷ ÷ ø ö ç ç è æ ¶ ¶ x 反应 <0 向右 >0 向左 =0 平衡