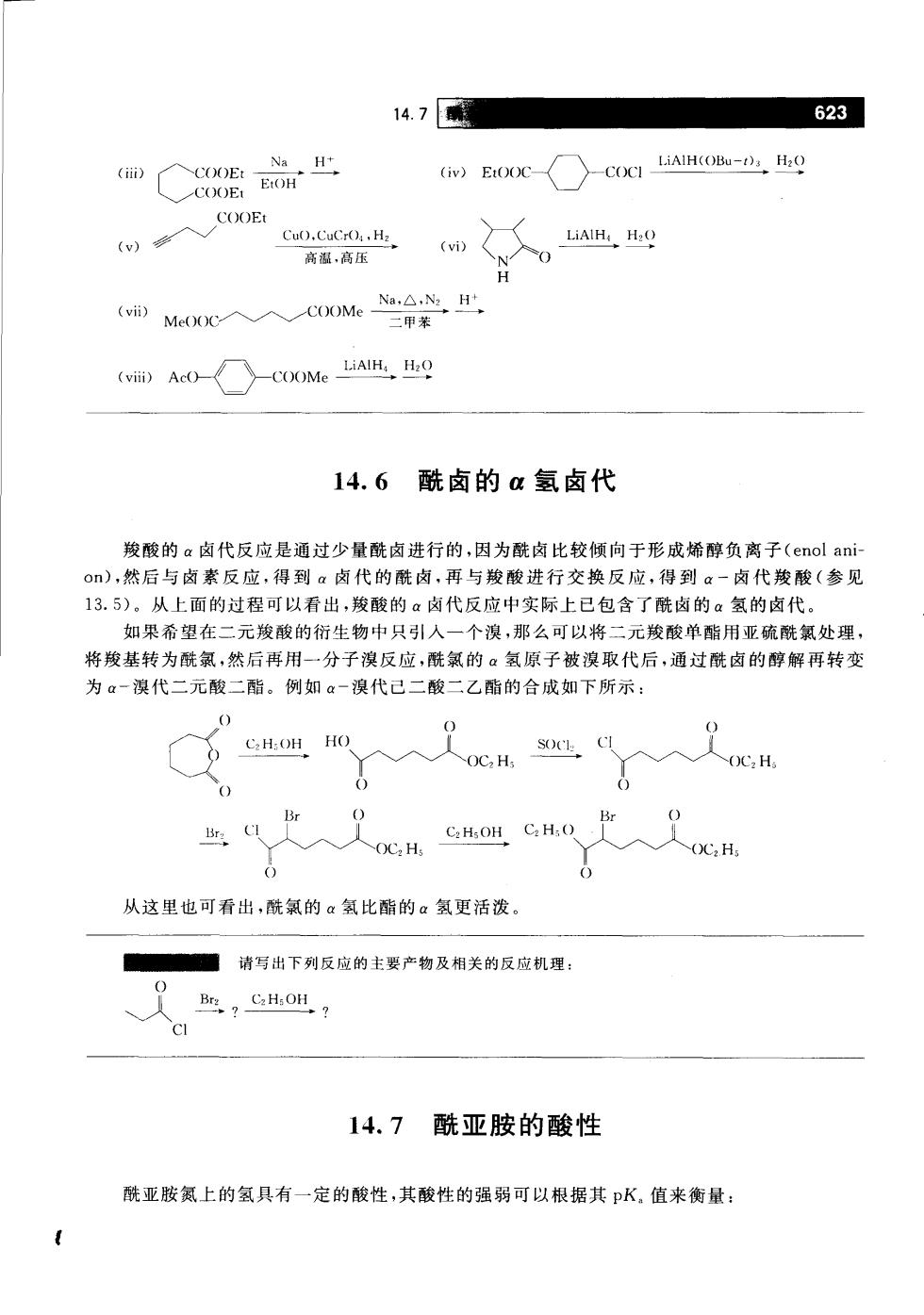
14.7利 623 (i) (v)LAOB-)HO Cu0.CuCrO.Hz 高滋,高压 m之人 LiAlH:H:O 。 二甲苯 (vii)AcO-《 〉-COMeANQ 14.6酰卤的a氢卤代 羧酸的a卤代反应是通过少量酰卤进行的,因为酰卤比较倾向于形成烯醇负离子(enol ani- o),然后与卤素反应,得到卤代的酰卤,再与羧酸进行交换反应,得到。一卤代羧酸(参见 13.5)。从上面的过程可以看出,羧酸的a卤代反应中实际上已包含了酰卤的a氢的卤代。 如果希望在二元羧酸的衍生物中只引入一个溴,那么可以将二元羧酸单酯用亚硫酰氯处理 将羧基转为酰氯,然后再用一分子溴反应,酰氯的α氢原子被溴取代后,通过酰卤的醇解再转变 为α一溴代二元酸二酯。例如a一溴代己二酸二乙酯的合成如下所示 人oC,Hg 0 () 人(CH 从这里也可看出,酰氯的a氢比酯的a氢更活泼 ■请写出下列反应的主要产物及相关的反应机理: c 14.7酰亚胺的酸性 酰亚胺氮上的氢具有一定的酸性,其酸性的强弱可以根据其PK,值来衡量:
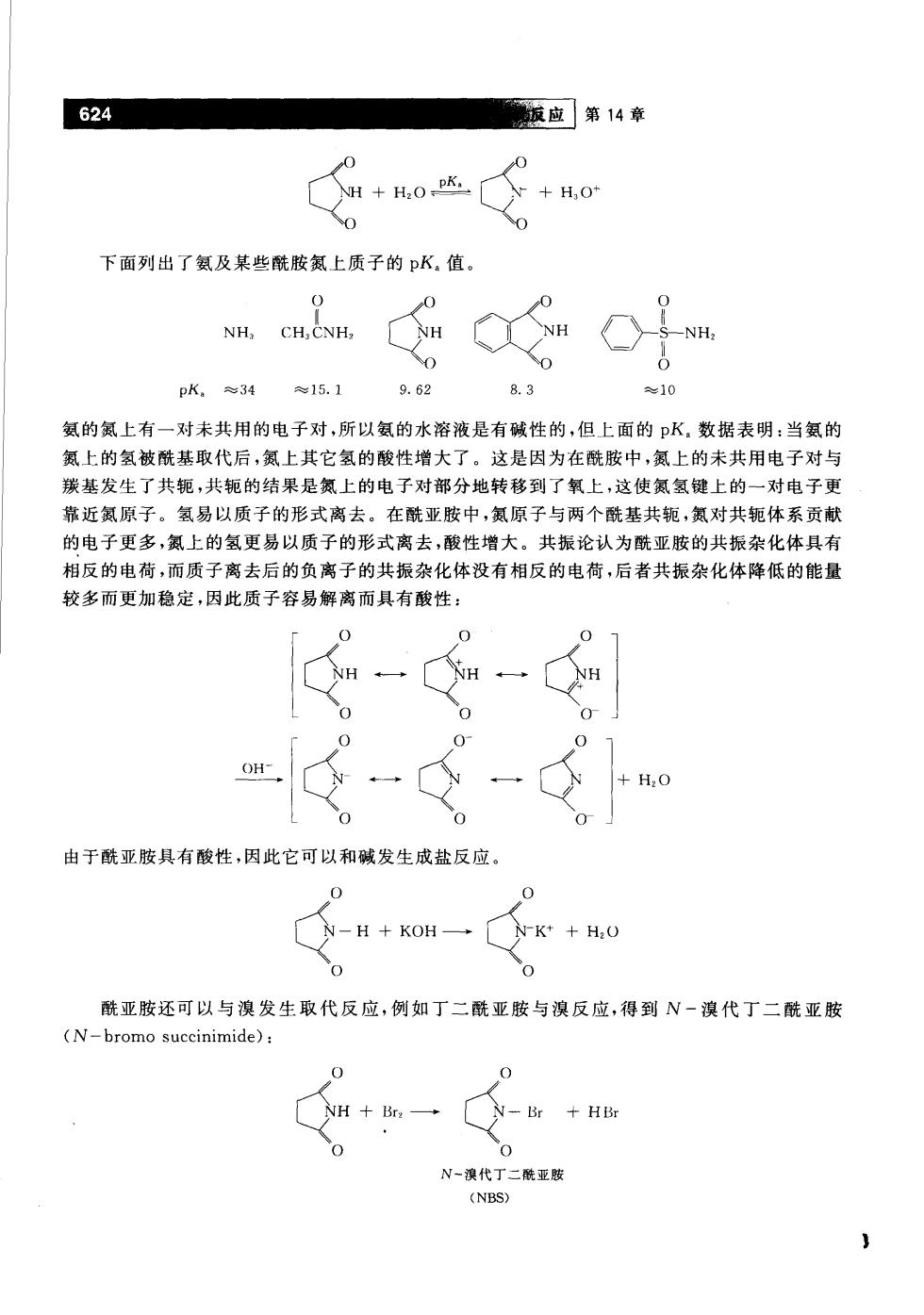
624 版应]第14章 +H,0+H,o 下面列出了氨及某些酰胺氮上质子的pK,值 NH, pK,≈34 15.1 9.62 8.3 氨的氯上有一对未共用的电子对,所以氨的水溶液是有碱性的,但上面的pK。数据表明:当氨的 氮上的氢被酰基取代后,氮上其它氢的酸性增大了。这是因为在酰胺中,氮上的未共用电子对与 羰基发生了共轭,共轭的结果是氮上的电子对部分地转移到了氧上,这使氮氢键上的一对电子更 靠近氮原子。氢易以质子的形式离去。在酰亚胺中,氨原子与两个酰基共轭,氮对共轭体系贡献 的电子更多,氯上的氢更易以质子的形式离去,酸性增大。共振论认为酰亚胺的共振杂化体具有 相反的电荷,而质子离去后的负离子的共振杂化体没有相反的电荷,后者共振杂化体降低的能量 较多而更加稳定,因此质子容易解离而具有酸性; 由于酰亚胺具有酸性,因此它可以和碱发生成盐反应。 0 N-H+KOH一 N-K*+HaO 酰亚胺还可以与溴发生取代反应,例如丁二酰亚胺与溴反应,得到N一溴代丁二酰亚胺 (N-bromo succinimide): 0 Br HBr 0 N一溴代丁二酰亚蔽 (NBS)

14.8 625 N-溴代丁二酰亚胺是一个重要的漠化试剂,可用于烯类化合物的α位溴代(参看8.10)。 鞭请用共振式表示下列各结构 00 (D CH,CNH, CH,CNH GHD)CH.CNHCCH, 00 00 (iv)CH.CNCCH CH.CNCCH, COCH, 14.8烯酮的反应 含有C一C一O结构的化合物称为烯嘲(olefine ketone),它可以看作是羧酸发生分子内 失水(失去羧羟基和。氢)形成的,因此也可以看作是分子内的酸酐: -c-om 4u00-0 最简单的烯酮是乙烯酮(CH:一C一O)。它是一个有毒的气体,沸点一48℃。 烯酮由于含有聚积的双键,化学性质十分活泼。现以乙烯酮为例,简单介绍它的反应 1.碳基的加成 烯酮的两个π键成正交形式,特别易于打开。它的羰基可和多种含“活泼”氢的化合物如水 卤化氢、羧酸、醇、氨等发生加成反应。加成时,总是氢加在氧上,另一部分加在碳上,生成的烯醇 经互变异构就得羧酸、酰卤、酸酐、酯、酰胺等: OH H-OH一CH.-COHJ互变异格CH.c0OH发酸 CC-0+H0-C一R二CHCR]互变CHC0R限F 0 00 Hm一【o"Rl5 CILOR。 H一cu5cmhn 0 酰胺 在以上各反应中,分子中的氢都被一个乙酰基取代,因此烯酮是一个很理想的乙酰基化试剂

626 瘦第14章 (acetylating agent),工业上制备乙酸酐就是利用这个反应。 烯酮也可以和格氏试剂发生反应,生成酮: OMgX OH CH-C-O+RMgX→CH-C CH,-C R 2.与甲醛反应烯酮二聚 烯酮与甲醛反应可形成B-丙内酯(B-propanolactone) 0 点-33.4℃,沸点162℃ 乙烯酮在合适的条件下二聚生成二乙烯酮,二乙烯酮是取代的日-丙内酯。加热又重新分解 为乙烯酮,因此二乙烯酮也是烯酮的一种保存形式。 CH,-C-O CH:-G-0 二乙烯酮 B-丙内酯可与一系列试剂发生反应,一般在中性、弱酸性介质中,经S、2反应,发生烷氧键断裂, 生成取代羧酸。例如: N.SH.H:O HS 入C00H CHOH 烷氧键断裂 ·CH,0入C00H HC,NaC,He0C入 COOH 在碱性或强酸性介质中,经加成-消除机理,发生酰氧键断裂开环,生成日取代的羧酸衍生物, 例如: Q名 CH,CH,OH.HO入-COOCH 酰氧健断 二乙烯酮由于B碳用双键与亚甲基相连,使亲核试剂难于进攻B碳,主要发生酰氧键断裂 例如: OC.Hs
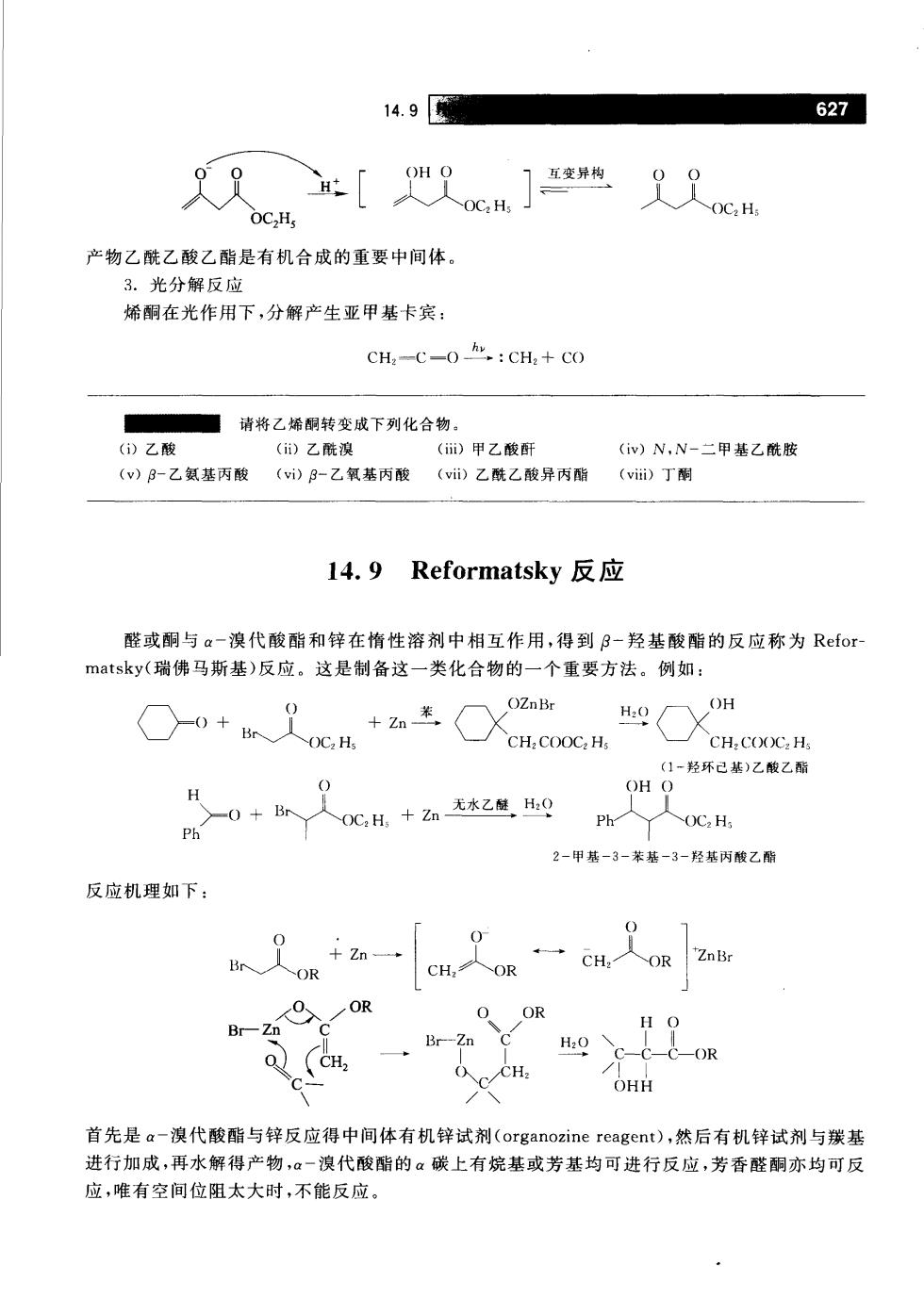
14.9 627 OC,H 产物乙酰乙酸乙酯是有机合成的重要中间体。 3.光分解反应 烯酮在光作用下,分解产生亚甲基卡宾: CH2-C-0:CH。+Co ■请将乙烯酮转变成下列化合物, (乙酸 (i)乙酰澳 ()甲乙酸酐 (iv)N,N-二甲基乙酰胺 (v)-乙氨基丙酸 (i)B-乙氧基丙酸(i)乙酰乙酸异丙酯(vi丁酮 l4.9 Reformatsky反应 醛或酮与a-溴代酸酯和锌在惰性溶剂中相互作用,得到B-羟基酸酯的反应称为Refor matsky(瑞佛马斯基)反应。这是制备这一类化合物的一个重要方法。例如: OZnBr ()H ○0+ +zn苯〈X OC:Hs CH:COOC:H. 门一羟环己基)乙酸乙酯 H OH C -0+Br OCH+Za无水2壁品0 Ph 2-甲基-3-装基-3-羟基丙酸乙酯 反应机理如下: CH,OR OR OR OHH 首先是a-溴代酸酯与锌反应得中间体有机锌试剂(organozine reagent)),然后有机锌试剂与羰基 进行加成,再水解得产物,一溴代酸酯的α碳上有烷基或芳基均可进行反应,芳香醛酮亦均可反 应,唯有空间位阻太大时,不能反应