
第八章羧酸、羧酸衍生物、取代酸讲课学时:6(7)教学目的:通过课堂教学使学生掌握羧酸、羧酸衍生物、取代酸的结构特征、系统命名法、物理性质与主要的化学性质。教学难点:羧酸、羧酸衍生物、取代酸的各类化学性质。教学方式:课堂讲授、多媒体、模型、课堂讨论教学内容:(一)羧酸(1)羧基的结构(2)羧酸的系统命名法和俗名(3)羧酸的物理性质(4)羧酸的化学性质:酸性、生成各类羧酸衍生物、0-取代反应、还原、二元羧酸的反应(5)自然界常见的羧酸类物质(二)羧酸衍生物(1)四类羧酸衍生物的结构和命名(2)四类羧酸衍生物的化学性质:水解、醇解、氨解、酯缩合反应(3)伯酰胺的降解(Hofmann降解)(三)碳酸衍生物(1)碳酸酰氯(光气):结构与性质(2)碳酸酰胺(尿素):结构与性质(3)碳酸酯与氨基甲酸酯:结构与性质(四)取代酸(1)醇酸(羟基酸):结构与性质(2)酚酸(羟基酸):结构与性质(3)羰基酸:结构与性质(4)乙酰乙酸乙酯(羰基酸酯):结构与性质
1 第八章 羧酸、羧酸衍生物、取代酸 讲课学时:6(7) 教学目的:通过课堂教学使学生掌握羧酸、羧酸衍生物、取代酸的结构 特征、系统命名法、物理性质与主要的化学性质。 教学难点:羧酸、羧酸衍生物、取代酸的各类化学性质。 教学方式:课堂讲授、多媒体、模型、课堂讨论 教学内容:(一) 羧酸 (1)羧基的结构 (2)羧酸的系统命名法和俗名 (3)羧酸的物理性质 (4)羧酸的化学性质:酸性、生成各类羧酸衍生物、α-取代反 应、还原、 二元羧酸的反应 (5)自然界常见的羧酸类物质 (二)羧酸衍生物 (1)四类羧酸衍生物的结构和命名 (2)四类羧酸衍生物的化学性质:水解、醇解、氨解、酯缩合 反应 (3)伯酰胺的降解(Hofmann 降解) (三)碳酸衍生物 (1)碳酸酰氯(光气):结构与性质 (2)碳酸酰胺(尿素):结构与性质 (3)碳酸酯与氨基甲酸酯:结构与性质 (四)取代酸 (1)醇酸(羟基酸):结构与性质 (2)酚酸(羟基酸):结构与性质 (3)羰基酸:结构与性质 (4)乙酰乙酸乙酯(羰基酸酯):结构与性质
课程进程「课程题目丨形式时间详细内容备注或讨论\min辅助手段(-)羧酸羧酸的结 讲授(1)羧酸的官能团是羧基多媒体辅助15梦教学;-0H-COOH 羧基中碳和氧都是SP2杂化,羧基中所有的原子在同一个平面上,羧基中的羰基和羟基形成P-元共轭(2)羟基上的氢解离后,两个C-0键键长完全平均化,负电荷均与分布在两个C-O键上,结构更稳定,所以羧基显示酸性,但仍属弱酸。羧酸的系讲授25羧酸类化合物在自然界大量存在,多媒体辅助统命名法因此很多羧酸化合物都有俗名。教学:和俗名例如:甲酸也叫蚁酸;乙酸也课堂练习;醋酸羧酸的系统命名法与醛相同,取含有羧基的最长碳链作为主链,编号由羧基开始。羧基连在脂肪环或芳香环上,要以甲酸为母体,例如环已烷甲酸、苯甲酸。[羧酸的物讲授10羧酸类化合物的沸点较高。例如乙多媒体辅助理性质酸的沸点117.9℃,分子量相当的教学;丙醛沸点才48.8℃。课堂讨论;分子量较低的羧酸类化合物水溶性较好,碳链增长,水溶性下降。例如四个碳以下的羧酸可以与水
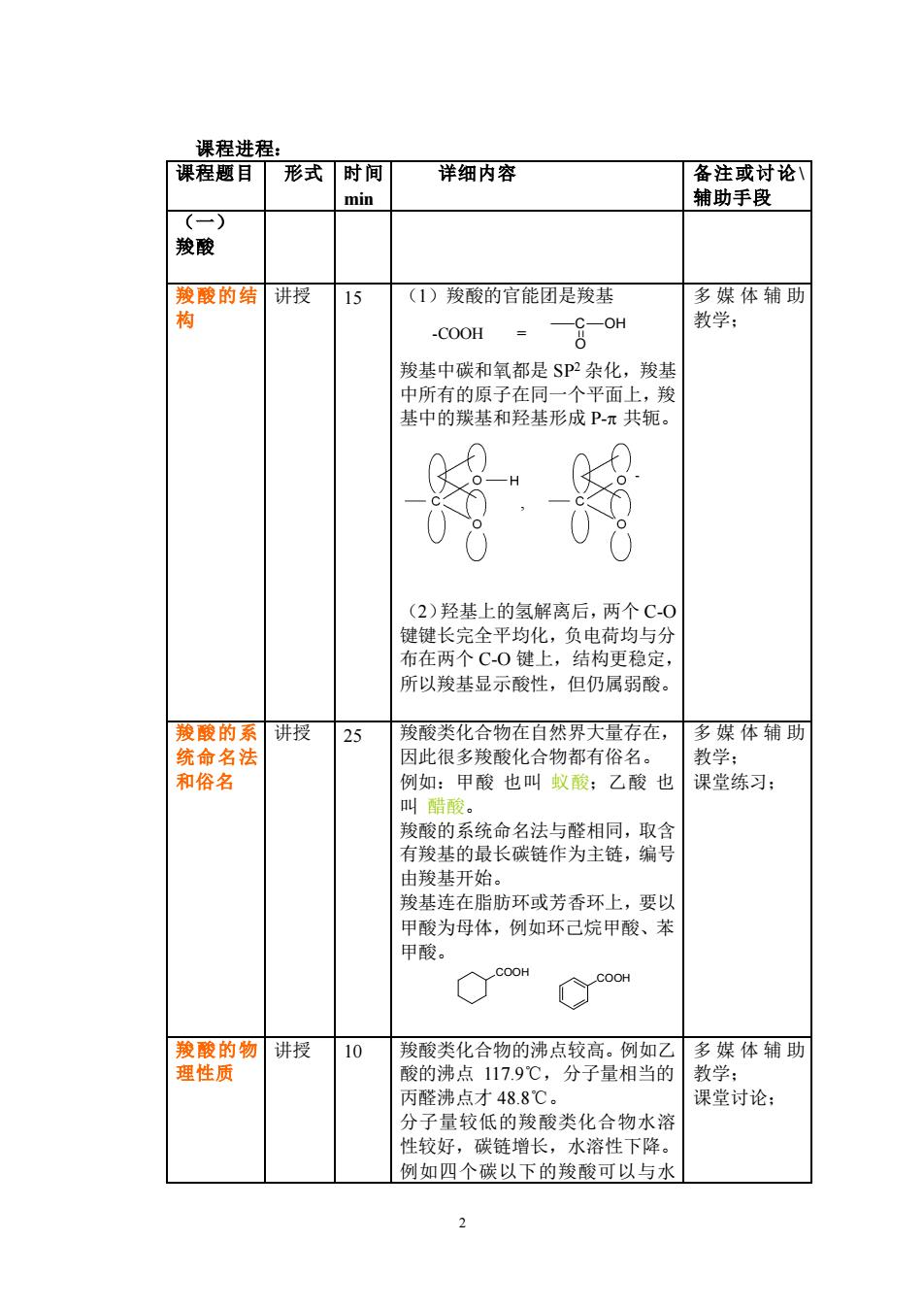
2 课程进程: 课程题目 形式 时间 min 详细内容 备注或讨论 \ 辅助手段 (一) 羧酸 羧酸的结 构 讲授 15 (1)羧酸的官能团是羧基 -COOH = C OH O 羧基中碳和氧都是 SP2 杂化,羧基 中所有的原子在同一个平面上,羧 基中的羰基和羟基形成 P- 共轭。 , (2)羟基上的氢解离后,两个 C-O 键键长完全平均化,负电荷均与分 布在两个 C-O 键上,结构更稳定, 所以羧基显示酸性,但仍属弱酸。 多媒体辅助 教学; 羧酸的系 统命名法 和俗名 讲授 25 羧酸类化合物在自然界大量存在, 因此很多羧酸化合物都有俗名。 例如:甲酸 也叫 蚁酸;乙酸 也 叫 醋酸。 羧酸的系统命名法与醛相同,取含 有羧基的最长碳链作为主链,编号 由羧基开始。 羧基连在脂肪环或芳香环上,要以 甲酸为母体,例如环己烷甲酸、苯 甲酸。 COOH COOH 多媒体辅助 教学; 课堂练习; 羧酸的物 理性质 讲授 10 羧酸类化合物的沸点较高。例如乙 酸的沸点 117.9℃,分子量相当的 丙醛沸点才 48.8℃。 分子量较低的羧酸类化合物水溶 性较好,碳链增长,水溶性下降。 例如四个碳以下的羧酸可以与水 多媒体辅助 教学; 课堂讨论;

以任何比例互溶。小分子的羧酸化合物有刺激性的气味和酸臭味。羧酸的化(1) 酸性多媒体辅助讲授50学性质羧酸的酸性比水和碳酸强,比大多教学;数酚强,但它仍属于弱酸。它可以课堂练习;和金属氧化物和氢氧化物形成盐。」课堂讨论R-COOH + NaOHR-O0ONa + H,O-COO).MgOH羧酸可以分解一般的酚盐:ONaR-COC羧酸可以分解碳酸盐,生二氧化R-COOH + NONa+ CONaHoR-COoH + Na,CO,-COoONa + CO,羧酸盐可以被更强的酸分解:COONaCOOHNaoHC利用羧酸的酸性,可以对混合物进做混合物分行分离纯化。离练习;(2)羧基上羟基的取代反应羧基上的羟基可以被一系列的原子和原子团所取代,生成的产物是羧酸衍生物:A-0-NH(3)还原催化氢化不能还原羧基,只有四氢铝锂(LiAIH4)可以把羧基直接还例题、课堂练原到醇:习;
3 以任何比例互溶。 小分子的羧酸化合物有刺激性的 气味和酸臭味。 羧酸的化 学性质 讲授 50 (1)酸性 羧酸的酸性比水和碳酸强,比大多 数酚强,但它仍属于弱酸。它可以 和金属氧化物和氢氧化物形成盐。 羧酸可以分解一般的酚盐: 羧酸可以分解碳酸盐,产生二氧化 碳 羧酸盐可以被更强的酸分解: 利用羧酸的酸性,可以对混合物进 行分离纯化。 (2)羧基上羟基的取代反应 羧基上的羟基可以被一系列的原 子和原子团所取代,生成的产物是 羧酸衍生物: R C O OR' R C O NH2 R C O X R C O O C R R C O O OH (3)还原 催化氢化不能还原羧基,只有四氢 铝锂(LiAlH4)可以把羧基直接还 原到醇: 多媒体辅助 教学; 课堂练习; 课堂讨论 做混合物分 离练习; 例题、课堂练 习;

(4)α-卤代反应羧基的拉电子作用使α-氢活泼,在日光或红磷的催化下,含有α-氢的例题、课堂做羧酸和卤素反应,生成α-卤代羧「合成练习;酸CH2COOHCHgCOOH + CI2 —OCHCOOHCIC—COOH(5)二元羧酸的性质a草酸(乙二酸)加热分解COOHHCOOH+CO2COOH二酸加热脱羧反应CH3COOHorCH2COCCHaCCH2COOCH2CO己二酸、戊二酸在氢氧化钡作用下加热失水与失羧CH.CHCOOH0+H,0+cO2做合成练习;CHCH.COC<0 + H2O + CO2CH2CH2COO(6)草酸与甲酸的还原性草酸和甲酸都具有还原性,都能使高锰酸钾褪色。甲酸还可以还原Fehling 溶液和 Tolln 试剂。草酸和甲酸的还原性可用于鉴别。自然界常列举部分自然界存在的羧酸类化
4 (4)-卤代反应 羧基的拉电子作用使 -氢活泼,在 日光或红磷的催化下,含有 -氢的 羧酸和卤素反应,生成 -卤代羧 酸: CH3COOH + Cl2 CH2COOH Cl C Cl CHCOOH Cl Cl COOH Cl Cl (5)二元羧酸的性质 a.草酸(乙二酸)加热分解 b.丙二酸加热脱羧反应 H2C COOH COOH CH3COOH + CO2 c. 丁二酸、戊二酸加热失水 CH2COOH CH2COOH O + H2O O O H2C CH2COOH CH2COOH O + H2O O O d. 己二酸、戊二酸在氢氧化钡作用下, 加热失水与失羧 CH2CH2COOH CH2CH2COOH Ba(OH)2 O + H2O + CO2 H2C CH2CH2COOH CH2CH2COOH Ba(OH)2 O + H2O + CO2 (6)草酸与甲酸的还原性 草酸和甲酸都具有还原性,都能使 高锰酸钾褪色。甲酸还可以还原 Fehling 溶液和 Tollen 试剂。 草酸和甲酸的还原性可用于鉴别。 例题、课堂做 合成练习; 做合成练习; 自然界常 列举部分自然界存在的羧酸类化
见的羧酸合物。类物质(三) 羧酸衍生物四类羧酸讲授通过具体化合物学习四类羧酸衍多媒体辅助120衍生物的生物酰卤、酸酐、酯、酰胺的命名:」教学;结构和命名aengaOchgogoanonCH,COOCH,CONH四类羧酸讲授(1)水解多媒体辅助35衍生物的教学:课堂讨论;化学性质10课堂练习;110RNH(2)醇解I做酯交换练目-C-OH习题,(3)氨解o.-1-0H(4)酯缩合反应CH3COOCH2CH3+CH3COOCH2CH做酯缩合练NaOC2H5OC2H5习题,+ CHaCH2OH产物称为乙酰乙酸乙酯(三乙)(4)伯酰胺的降解(Hofmann降解):在Br2和氢氧化钠存在下,伯酰胺发生脱羰反应,生成伯胺
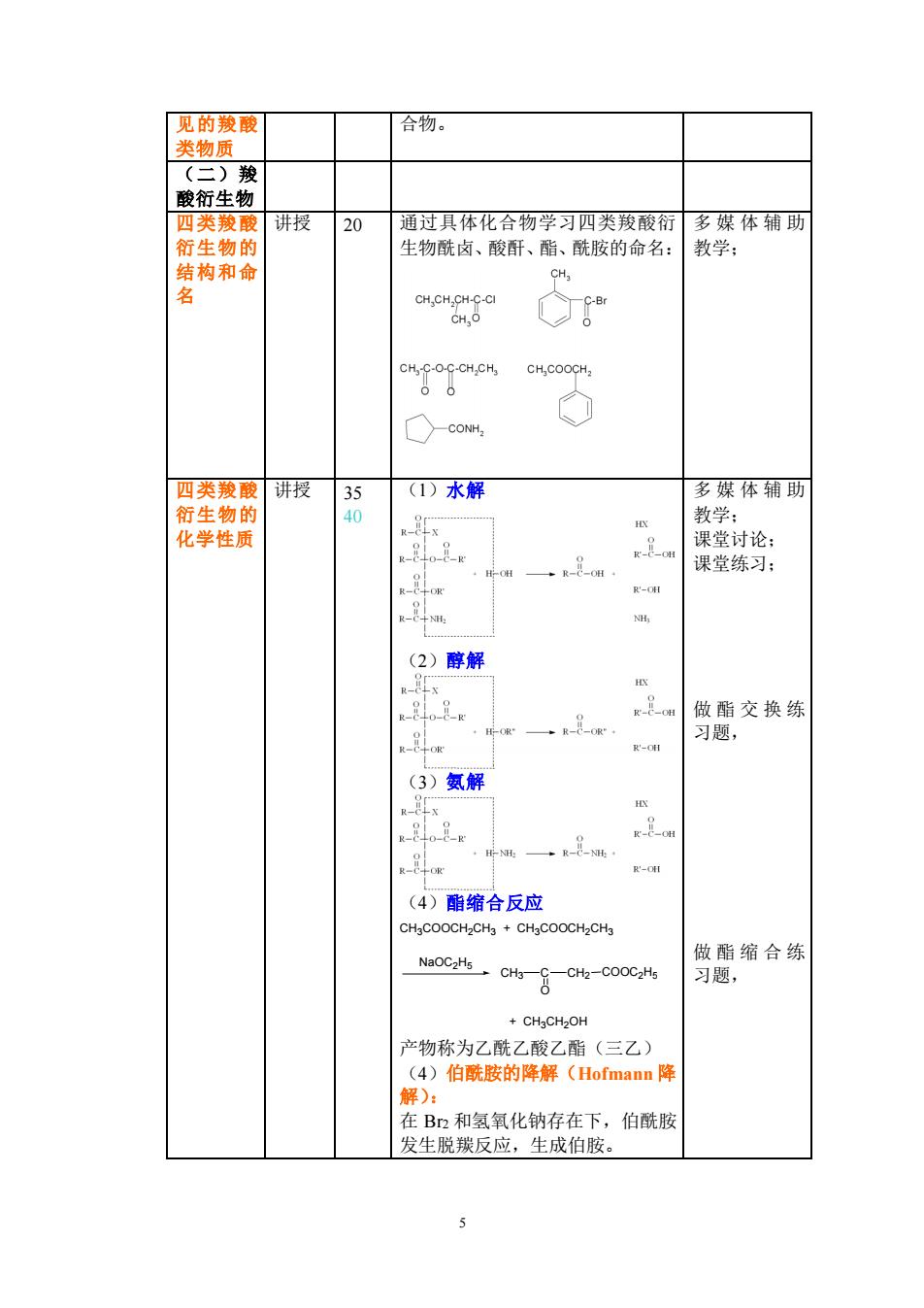
5 见的羧酸 类物质 合物。 (二)羧 酸衍生物 四类羧酸 衍生物的 结构和命 名 讲授 20 通过具体化合物学习四类羧酸衍 生物酰卤、酸酐、酯、酰胺的命名: 多媒体辅助 教学; 四类羧酸 衍生物的 化学性质 讲授 35 40 (1)水解 (2)醇解 (3)氨解 (4)酯缩合反应 CH3COOCH2CH3 + CH3COOCH2CH3 NaOC2H5 CH3 C CH2 COOC2H5 O + CH3CH2OH 产物称为乙酰乙酸乙酯(三乙) (4)伯酰胺的降解(Hofmann 降 解): 在 Br2 和氢氧化钠存在下,伯酰胺 发生脱羰反应,生成伯胺。 多媒体辅助 教学; 课堂讨论; 课堂练习; 做酯交换练 习题, 做酯缩合练 习题