
km和k的关系: p=KxXB ● =kxng/(nA+nB) ● ≈kng/n4 当Xg→0时 ● =k MAnB/(nAMA) ● -(k MA)nE/(nAMA) =(k MA)ng/WA ● =(KMA)mB ● =kmmB ·令 km=KxMA (4)
km和kx的关系: • p=kxxB • =kxnB /(nA+nB ) • ≈ kxnB /nA 当xB→0时 • =kxMAnB /(nAMA) • =(kxMA)nB /(nAMA) • = (kxMA)nB /WA • = (kxMA)mB • =kmmB • 令 km=kxMA (4)
·若用物质的量浓度贝则亨利定律为: ● PB=kcCB 5 ·k:物质的量浓度为单位的亨利系数 ·可以证明,对于稀溶液,不同浓度表示 法的亨利系数k与k的关系为: KC=KXMAPA (6)
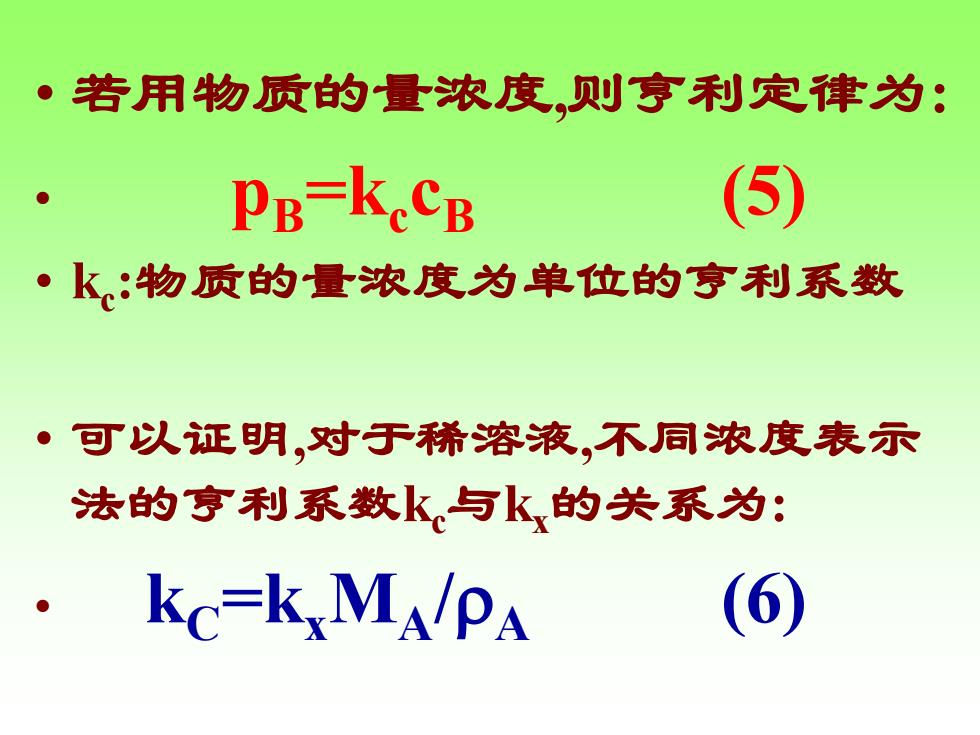
• 若用物质的量浓度,则亨利定律为: • pB=kc cB (5) • kc :物质的量浓度为单位的亨利系数 • 可以证明,对于稀溶液,不同浓度表示 法的亨利系数kc与kx的关系为: • kC=kxMA/A (6)

。亨利定律的适用范围: ·1。适用于稀溶液,浓度大时偏差较大; ·。溶质在气相和液湘中的分子形态应一 致,若两相中分子的形态不一致,则 不适用. ·如: ·HC在气相中以HC分子的形式存在,当 其溶于水溶液中后,HC将电离成H+离子 和C离子,故HC在水溶液中和气湘中的 粒子形态不相同,故亨利定律不能用于盐 酸溶液
• 亨利定律的适用范围: • 1. 适用于稀溶液, 浓度大时偏差较大; • 2. 溶质在气相和液相中的分子形态应一 致, 若两相中分子的形态不一致,则 不适用. • 如: • HCl在气相中以HCl分子的形式存在, 当 其溶于水溶液中后, HCl将电离成H+离子 和Cl-离子,故HCl在水溶液中和气相中的 粒子形态不相同, 故亨利定律不能用于盐 酸溶液

·三。理想溶液(ideal solution) ·热力学定义: 若溶液中任一组分在全部浓度范围内 (0≤x≤1)均服从拉乌尔定律,则其为 理想溶液. ·理想溶液的理论模型:满足以下条件的体系为 理想溶液以二元溶液为例): ·1.A、B分子的大小相同,形状相似: ·2.A-A:A-B:B-B分子对之间具有相 同的势能函数
• 三. 理想溶液(ideal solution) • 热力学定义: 若溶液中任一组分在全部浓度范围内 (0≦xi≦1)均服从拉乌尔定律,则其为 理想溶液. • 理想溶液的理论模型: 满足以下条件的体系为 理想溶液(以二元溶液为例): • 1. A、B分子的大小相同,形状相似; • 2. A-A;A-B;B-B分子对之间具有相 同的势能函数