
二、价键理论的基本要点 1·成键两原子接近时,只有各自提供自旋方向相反 的单电子才能彼此配对,形成稳定的共价键。 2.自旋方向相反的单电子配对成键后,就不能再和其 它原子的单电子配对。所以,每个原子所能形成的 共价键数目取决于该原子中的单电子数目。这就是 共价键的饱和性。 3.成键电子的原子轨道重叠愈多,两核间的电子云密 集愈多,形成的共价键愈牢固。这称为原子轨道最 大重叠原理。因此,原子间总是尽可能地沿着原子 轨道重叠最大的方向成键。 所以共价键具有方向性
1.成键两原子接近时,只有各自提供自旋方向相反 的单电子才能彼此配对,形成稳定的共价键。 二、价键理论的基本要点 2.自旋方向相反的单电子配对成键后,就不能再和其 它原子的单电子配对。所以,每个原子所能形成的 共价键数目取决于该原子中的单电子数目。这就是 共价键的饱和性。 3.成键电子的原子轨道重叠愈多,两核间的电子云密 集愈多,形成的共价键愈牢固。这称为原子轨道最 大重叠原理。因此,原子间总是尽可能地沿着原子 轨道重叠最大的方向成键。 所以共价键具有方向性

三、共价键的类型 ■ 若原子轨道沿键轴方 向以“头碰头”方式 重叠,如S一$,S一 Px,Px一Px重叠, 所形成的共价键称为 σ键,这种键的电子 森券形沿键牺对
三、共价键的类型 若原子轨道沿键轴方 向以“头碰头”方式 重叠,如S-S,S- Px,Px-Px重叠, 所形成的共价键称为 键,这种键的电子 云以圆柱形沿键轴对 称分布
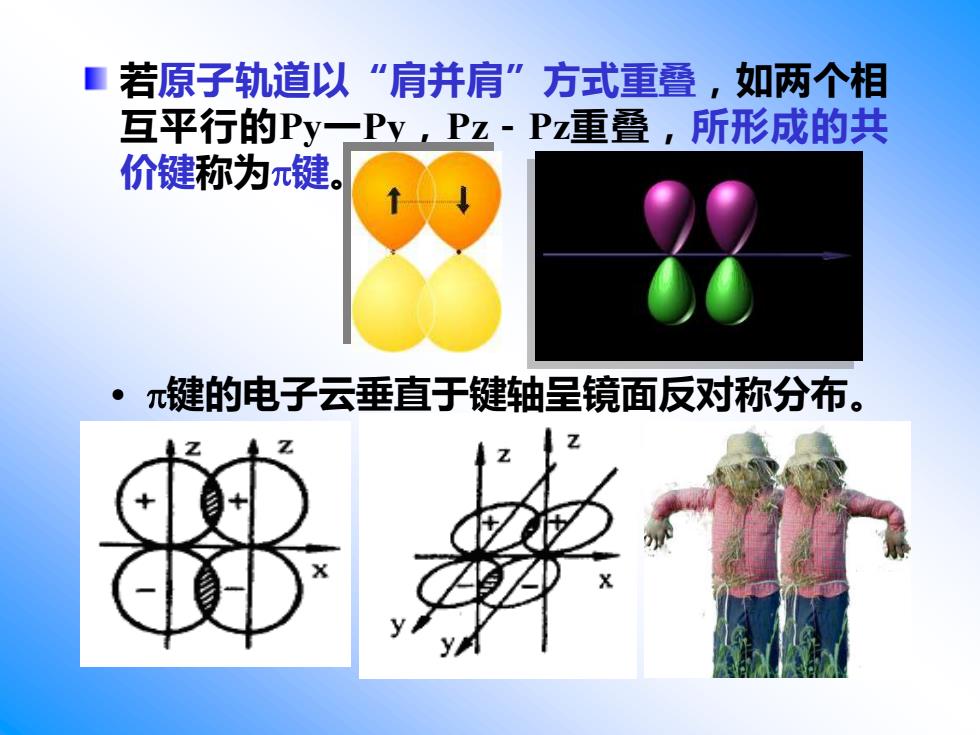
■若原子轨道以“肩并肩”方式重叠,如两个相 互平行的Py一Py,Pz-Pz重叠,所形成的共 价键称为π键。 ·π键的电子云垂直于键轴呈镜面反对称分布
若原子轨道以“肩并肩”方式重叠,如两个相 互平行的Py一Py,Pz-Pz重叠,所形成的共 价键称为键。 • 键的电子云垂直于键轴呈镜面反对称分布

o键与π键的差异 σ键的轨道重叠程度较π键大,故σ键的键能 大,稳定性高;π键的稳定性低,元电子的活 泼性较大,是化学反应的积极参与者。 一般,共价单键是σ键,双键中有一个σ键和 一个π键,三键中有一个σ键和两个π键。 N2的生成
键与键的差异 键的轨道重叠程度较键大,故键的键能 大,稳定性高; 键的稳定性低, 电子的活 泼性较大,是化学反应的积极参与者。 一般,共价单键是键,双键中有一个键和 一个键,三键中有一个键和两个键。 N2的生成
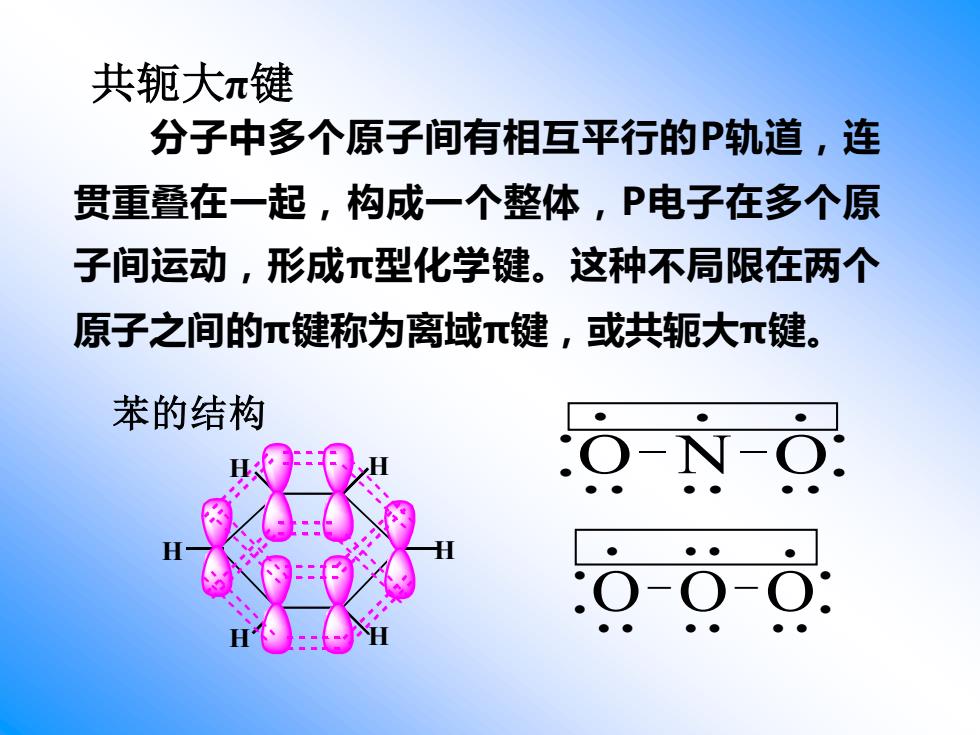
共轭大π键 分子中多个原子间有相互平行的P轨道,连 贯重叠在一起,构成一个整体,P电子在多个原 子间运动,形成π型化学键。这种不局限在两个 原子之间的π键称为离域π键,或共轭大π键。 苯的结构 δ-N-ò
共轭大π键 分子中多个原子间有相互平行的P轨道,连 贯重叠在一起,构成一个整体,P电子在多个原 子间运动,形成π型化学键。这种不局限在两个 原子之间的π键称为离域π键,或共轭大π键。 H H H H H H 苯的结构 • • • • • • • • • • • • • O−N−O • • • • • • • • • • • • • • O−O−O