
三、化学反应的平衡常数和等温方程假设有理想气体化学反应aA+bB3二gG+hH当反应达到平衡(A,Gm)r,p =VBμg = 0gu+huH=aua+buB混合理想气体的化学势表达式为:Ppμp(T,p)= μ(T)+ RTInDo则上式可写为PGDgue+gRTIn+hμ +hRTInDaμ% +aRT In+bug+bRT In6
6 三、化学反应的平衡常数和等温方程 假设有理想气体化学反应 aA + bB gG + hH 当反应达到平衡 G H A B g h a b + = +B B B ( , ) ( ) ln p T p T RT p = + 混合理想气体的化学势表达式为: 则上式可写为 ln ln ln ln G H G H A B A B p p g gRT h hRT p p p p a aRT b bRT p p + + + = + + + , ( ) 0 = = r m T p B B G

即DIn(gue+hun-aua-bug)RT(分)()式中,PB为B物质在平衡时的分压。=常数=K0()标准平衡常数,一定温度时为一定值,量纲为1
7 即 1 ln ( ) g h G H a b G H A B A B p p p p g h a b p p RT p p = − + − − 式中,pB为B物质在平衡时的分压。 g h G H a b A B p p p p p p p p = 常数 = Kθ 标准平衡常数,一定温度 时为一定值,量纲为1

D0(gue+hun-aua-bug)InRT()()如果令gu+hu-au%-bug=A,Gm则反应的标准吉布斯函数变化,指反应物和产物均处于标准态时,产物△,G =-RTlnK6的吉布斯函数与反应物的吉布斯函数总之差8
8 如果令 1 ln ( ) g h G H a b G H A B A B p p p p g h a b p p RT p p = − + − − G H A B r m g h a b G + − − = 则 ln r m G RT K = − 反应的标准吉布斯函数 变化,指反应物和产物 均处于标准态时,产物 的吉布斯函数与反应物 的吉布斯函数总之差
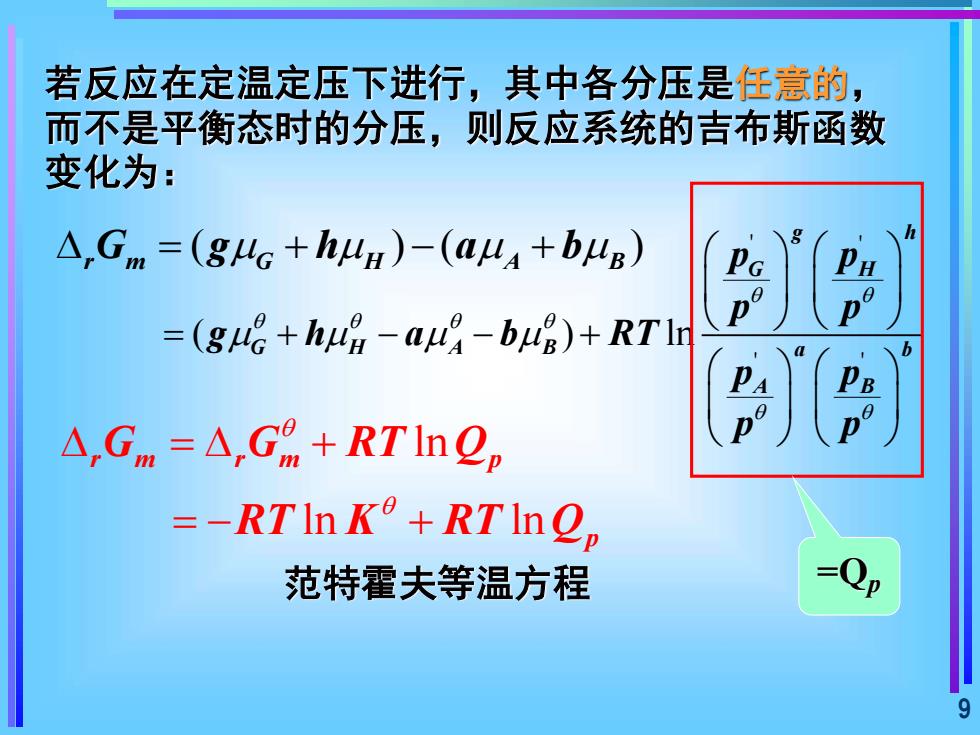
若反应在定温定压下进行,其中各分压是任意的而不是平衡态时的分压,则反应系统的吉布斯函数变化为:A,Gm=(guG+hu)-(au+buB)=(gu+hug-au-bu)+RTlrA,Gm=△,Gm + RT lnQ,=-RTIn K'+RTInQ=Qp范特霍夫等温方程07
9 若反应在定温定压下进行,其中各分压是任意的, 而不是平衡态时的分压,则反应系统的吉布斯函数 变化为: ( ) ( ) = + − + r m G H A B G g h a b ' ' ' ' ( ) ln g h G H G H A B a b A B p p p p g h a b RT p p p p = + − − + ln ln ln r m r m p p G G RT Q RT K RT Q = + = − + 范特霍夫等温方程 =Qp

说明:(1)式中p指平衡分压,P指任意状态时的分压K是标准平衡常数,Q,不是平衡常数,称为“分压商”。(2)推广到任意化学反应,只需用aB代替pB/poA,G. =△,G" +RTInQ.活度商=K0II(ab),IIasD:=Q(aa)e,(ag )enBB理想气体,a表示比值p/po高压实际气体,aB表示比值fB/p0理想液态混合物,B表示浓度xB10
10 说明:(1)式中pB指平衡分压,pB ’指任意状态时的分压; Kθ是标准平衡常数,Qp不是平衡常数,称为“分压商”。 (2)推广到任意化学反应,只需用aB代替pB /pθ ln r m r m a G G RT Q = + 活度商 ( ) B B eq B a K = ( ) ( ) ( ) ( ) b B eq a A eq h H eq g G eq a a a a = B B a B a Q = ☞理想气体, aB表示比值pB/pθ ☞高压实际气体, aB表示比值fB/pθ ☞理想液态混合物, aB表示浓度xB