
导航、 化学式 Fe(OH)2 Fe(OH)3 受热分解 隔绝空气加热,分解 稳定性 △ 2Fe(OH)3 Fe(OHDz二一Fe0+H2O Fe203+3H20 Fe(OH)2+2H Fe(OH)3+3H Fe2++2H20 Fe3++3H2O 与盐酸反应 固体溶解,溶液变成浅绿 固体溶解,溶液变成棕黄 色 色
导航 化学式 Fe(OH)2 Fe(OH)3 稳定性 隔绝空气加热,分解 Fe(OH)2 FeO+H2O 受热分解 2Fe(OH)3 Fe2O3+3H2O 与盐酸反应 Fe(OH)2+2H+ Fe2++2H2O 固体溶解,溶液变成浅绿 色 Fe(OH)3+3H+ Fe3++3H2O 固体溶解,溶液变成棕黄 色

导航 化学式 Fe(OH)2 Fe(OH)3 空气中,Fe(OHD2能迅速被氧气氧化成Fe(OHD3,现 两者的关系 象是白色沉淀迅速变成灰绿色,最后变成红褐色,化 学方程式为4Fe(OHD2+02+2H20一4Fe(OHD)3
导航 化学式 Fe(OH)2 Fe(OH)3 两者的关系 空气中,Fe(OH)2能迅速被氧气氧化成 Fe(OH)3,现 象是白色沉淀迅速变成灰绿色,最后变成红褐色,化 学方程式为 4Fe(OH)2+O2+2H2O 4Fe(OH)3
导 肯思考发现 氢氧化亚铁可用来制颜料、药物、催化剂、吸收剂和砷解 毒剂等。 下面是某同学用现配制的FSO,溶液与煮沸过冷却后的 NaOH溶液反应制备Fe(OHD2白色沉淀的实验。 NaOH 溶液 FeSO4 溶液
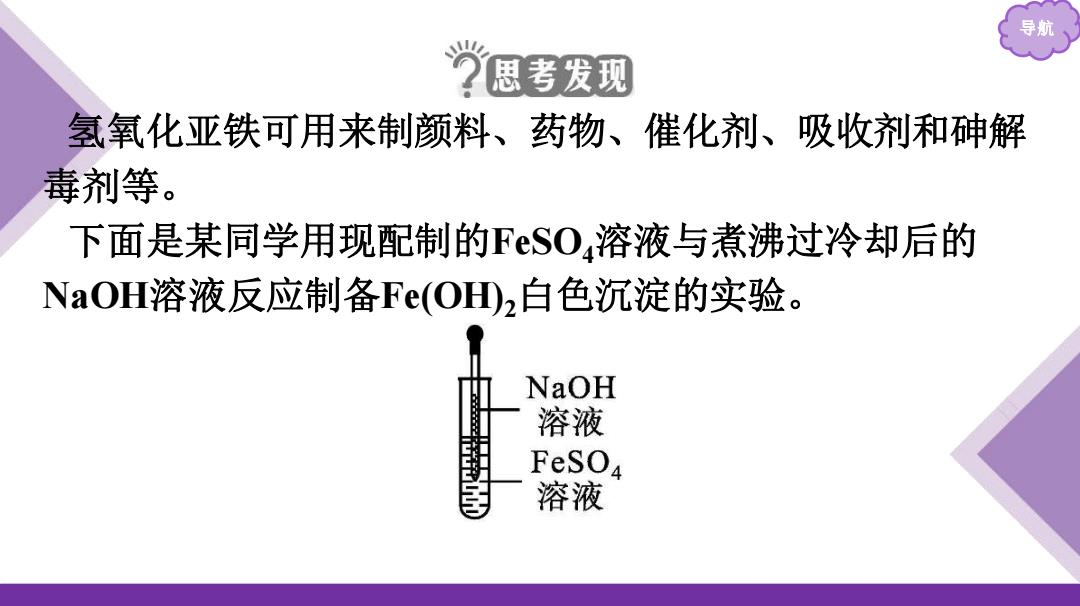
导航 氢氧化亚铁可用来制颜料、药物、催化剂、吸收剂和砷解 毒剂等。 下面是某同学用现配制的FeSO4溶液与煮沸过冷却后的 NaOH溶液反应制备Fe(OH)2白色沉淀的实验

(1)硫酸亚铁、氢氧化亚铁易被氧化的原因是什么? (2)采用FeSO4晶体配制上述FeSO,溶液时,还需要加入某种 固体,该固体可能是什么?为什么要加入该固体? (3)除去蒸馏水中溶解的O,常采用什么方法? (4)生成白色Fε(OH2沉淀的操作是用长胶头滴管吸取煮沸 过冷却后的NaOH溶液,插入FeSO,溶液液面下,再挤出NaOH 溶液。为什么这样操作? (⑤)根据该同学的实验,请你总结一下在实验室里用FS0溶 液和NaOH溶液制备Fe(OHD2时,采取哪些措施可以较长时间 观察到白色的Fe(OHD2沉淀?
导航 (1)硫酸亚铁、氢氧化亚铁易被氧化的原因是什么? (2)采用FeSO4晶体配制上述FeSO4溶液时,还需要加入某种 固体,该固体可能是什么?为什么要加入该固体? (3)除去蒸馏水中溶解的O2 ,常采用什么方法? (4)生成白色Fe(OH)2沉淀的操作是用长胶头滴管吸取煮沸 过冷却后的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH 溶液。为什么这样操作? (5)根据该同学的实验,请你总结一下在实验室里用FeSO4溶 液和NaOH溶液制备Fe(OH)2时,采取哪些措施可以较长时间 观察到白色的Fe(OH)2沉淀?

导航 提示:1)硫酸亚铁、氢氧化亚铁中铁元素为+2价,可以升高 到+3价,具有还原性,易被氧化。 (2)可以加入铁粉,以防止+2价铁被氧化。 3)可以加热煮沸。 (4)避免生成的Fε(OHD2沉淀接触02而被氧化
导航 提示:(1)硫酸亚铁、氢氧化亚铁中铁元素为+2价,可以升高 到+3价,具有还原性,易被氧化。 (2)可以加入铁粉,以防止+2价铁被氧化。 (3)可以加热煮沸。 (4)避免生成的Fe(OH)2沉淀接触O2而被氧化