D 1958 胺的结构 0 -CH3 H106H3C 089 CH3 氨的结构 甲胺的结构 三甲胺的结构 氨和胺分子具有四面体棱锥形结构: N原子是不等性的sp杂化。三个杂化轨道用于成键,一个杂 化轨道中含有孤对电子。 若N原子上连有三个不同基团,是手性分子,理论上应存在 对映体。 实际分离不出,因为: R' R CH3 iH3C C2H5 C2H5 △E=6千卡/mol Organic Chemistry
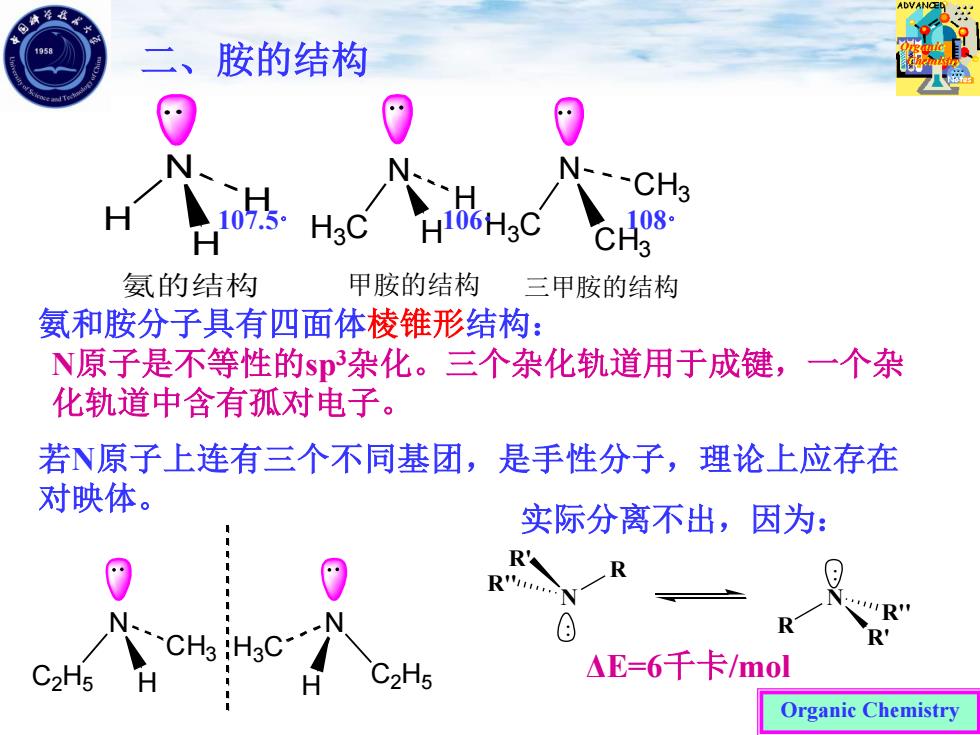
Organic Chemistry N H3 C H H 甲胺的结构 二、胺的结构 N H H H 氨的结构 N H3 C CH3 CH3 三甲胺的结构 氨和胺分子具有四面体棱锥形结构: N原子是不等性的sp3杂化。三个杂化轨道用于成键,一个杂 化轨道中含有孤对电子。 若N原子上连有三个不同基团,是手性分子,理论上应存在 对映体。 N C2 H5 H CH3 N H C2 H5 H3 C 实际分离不出,因为: N R R' R'' N R R' R'' . . ΔE=6千卡/mol 107.5。 106。 108
但有些被环状结构固定的三级胺,由于不能翻转, 也可以分离出对映异构体,如: CH3 Trogert碱 四级铵盐的对映体已经分离出来,N上四个sp轨道都用于成键, 氮的翻转难发生: CH; CH; Ph Ph C2H5 CH,=CH-CH2 H2C-CH=CH2 Organic Chemistry
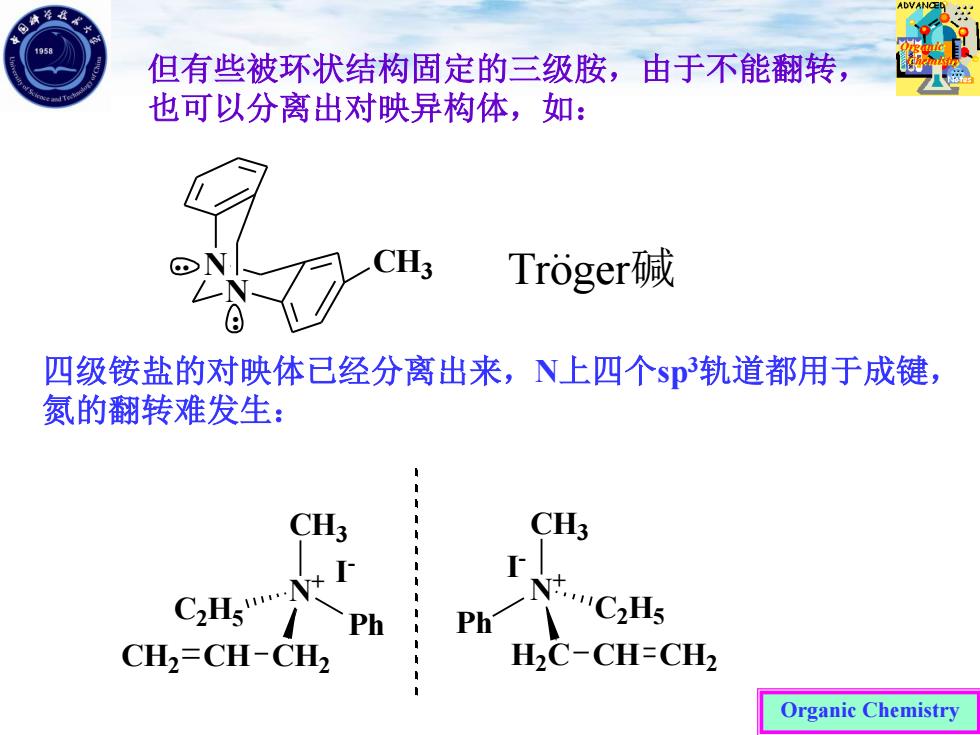
Organic Chemistry 但有些被环状结构固定的三级胺,由于不能翻转, 也可以分离出对映异构体,如: 四级铵盐的对映体已经分离出来,N上四个sp3轨道都用于成键, 氮的翻转难发生: N N CH3 . . Troger碱 . N + CH3 N + CH3 Ph Ph C2 H5 CH2 H2 C C2 H5 CH2 CH CH CH2 I - I -

1958 芳胺和脂肪胺的结构比较 1.47A ”具有较多p成份 CH 105.9 1.40A 13.9。 N介于sp2~sp3杂化之间 p一π共轭 电子云向 环上共轭转移 脂肪胺R一NH, 芳胺Ar一NH2 NH2 是吸电基() 是供电基(+C) 反应中心 在N原子的孤对电子上 不在N原子而在苯环上 碱性 较大 较小 三、胺的物理性质 低级胺(C6以下)一般易溶于水,溶解度随相对分子质量的增加而降低 伯胺和仲胺的沸点介入相对分子质量相近的醇与烷烃之间,这是由于伯胺和 仲胺能形成分子间氢键(但较醇分子间的氢键弱,N的电负性小于0,N不太易 作为氢键受体)的缘故。叔胺分子中没有N-H键,水溶性及沸点均比伯胺、仲 胺低。 Organic Chemistry
Organic Chemistry 芳胺和脂肪胺的结构比较 脂肪胺R—NH2 芳胺 Ar—NH2 —NH2 是吸电基(-I) 是供电基(+C) 反应中心 在N原子的孤对电子上 不在N原子而在苯环上 碱 性 较 大 较 小 三、 胺的物理性质 低级胺(C6以下)一般易溶于水,溶解度随相对分子质量的增加而降低 伯胺和仲胺的沸点介入相对分子质量相近的醇与烷烃之间,这是由于伯胺和 仲胺能形成分子间氢键(但较醇分子间的氢键弱,N的电负性小于O,N不太易 作为氢键受体)的缘故。叔胺分子中没有N-H键,水溶性及沸点均比伯胺、仲 胺低。 p—π共轭 电子云向 环上共轭转移 113.9。 105.9
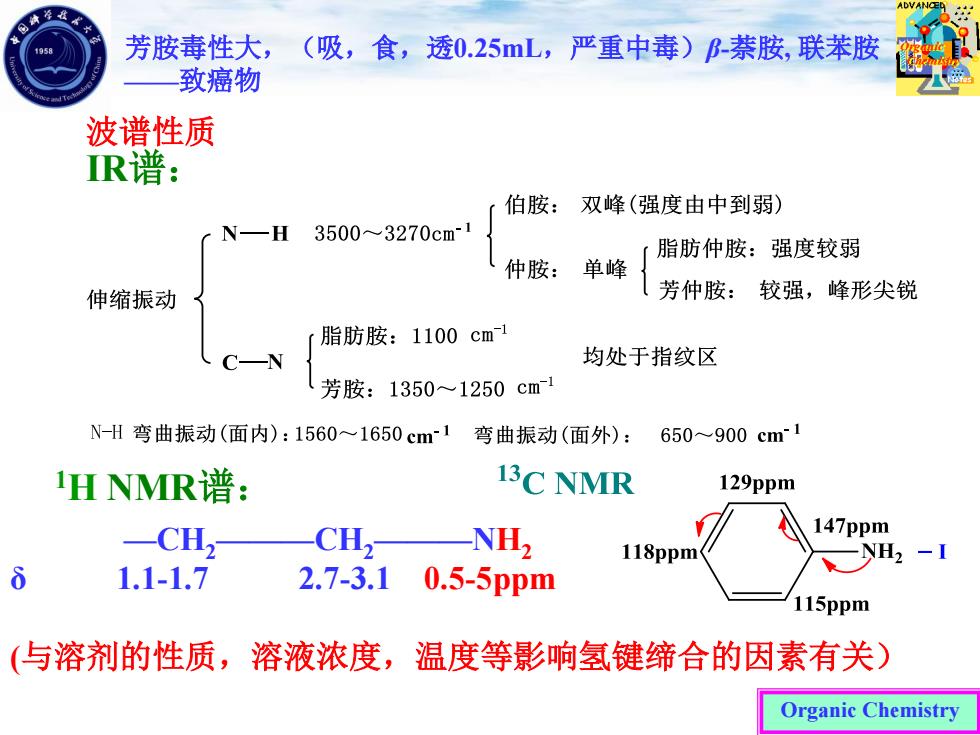
芳胺毒性大, (吸,食,透0.25mL,严重中毒)B-萘胺,联苯胺 致癌物 波谱性质 IR谱: 伯胺: 双峰(强度由中到弱) N一H 3500~3270cm1 脂肪仲胺:强度较弱 仲胺: 单峰 伸缩振动 芳仲胺: 较强,峰形尖锐 脂肪胺:1100cm -N 均处于指纹区 芳胺:1350~1250cm N-H弯曲振动(面内):1560~1650cm1弯曲振动(面外): 650~900cm1 HNMR谱: 13C NMR 129ppm CH NH2 147ppm 118ppm 6 1.1-1.7 2.7-3.1 0.5-5ppm 115ppm (与溶剂的性质,溶液浓度,温度等影响氢键缔合的因素有关) Organic Chemistry
Organic Chemistry 波谱性质 IR谱: 1H NMR谱: 芳胺毒性大,(吸,食,透0.25mL,严重中毒)β-萘胺, 联苯胺 ——致癌物 —CH2———CH2———NH2 δ 1.1-1.7 2.7-3.1 0.5-5ppm (与溶剂的性质,溶液浓度,温度等影响氢键缔合的因素有关)

1958 四、胺的化学性质 1.胺的碱性(basicity) N上的未共用电子对能接受一个质子,与大多数的无机酸反应 呈碱性 R-NH2 +HCI R一tNH3CI 胺的碱性强弱可用其离解常数K或离解常数的负对数pK来表 示。当胺溶于水时存在下列的平衡: RNH,+HO Kb=RNH *OH- K越大(或pK越小) Kb= [RNH ][OH pKb=-IgKb 碱性越强 [RNH,] 碱性强弱顺序:脂肪胺>NH,>芳香胺 pKp 3-4.54.75 910 在脂肪胺中: RNH,R,NH RN 级 二级 三级 Organic Chemistry
Organic Chemistry 四、胺的化学性质 1. 胺的碱性(basicity) N上的未共用电子对能接受一个质子,与大多数的无机酸反应 ——呈碱性 R NH2 + HCl R + NH3 Cl 胺的碱性强弱可用其离解常数Kb或离解常数的负对数pKb来表 示。当胺溶于水时存在下列的平衡: RNH2 H2 O RNH3 OH Kb Kb [RNH3 ] [OH ] [RNH2 ] pKb lgKb + + + - = + - =- 碱性强弱顺序:脂肪胺 > NH3 > 芳香胺 pKb 3—4.5 4.75 9—10 在脂肪胺中: RNH2 < R2NH > R3N 一级 二级 三级 Kb越大(或pKb越小) 碱性越强