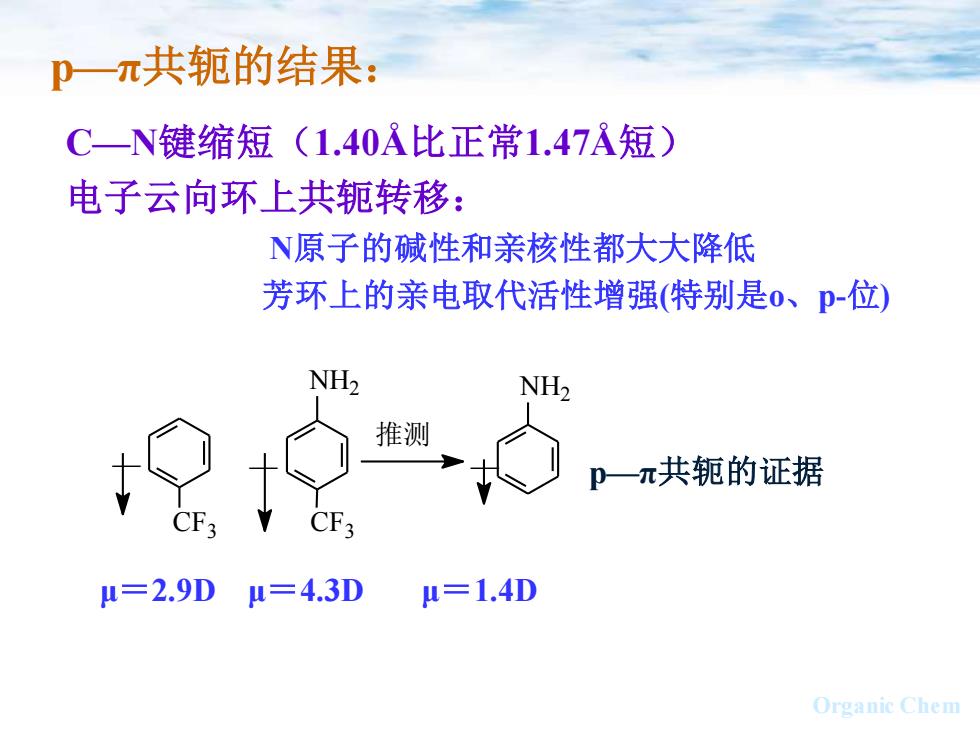
p一π共轭的结果: C一N键缩短(1.40A比正常1.47A短) 电子云向环上共轭转移: N原子的碱性和亲核性都大大降低 芳环上的亲电取代活性增强(特别是o、p-位) NH2 NH 推测 p一π共轭的证据 CF CF3 u=2.9D=4.3D u=1.4D Organic Chem
Organic Chem C—N键缩短(1.40Å比正常1.47Å短) 电子云向环上共轭转移: N原子的碱性和亲核性都大大降低 芳环上的亲电取代活性增强(特别是o、p-位) CF3 CF3 NH2 NH2 — — — 推测 p—π共轭的证据 μ=2.9D μ=4.3D μ=1.4D p—π共轭的结果:

a.胺的碱性与酸性 i,碱性 N上的未共用电子对能接受一个质子, 与大多数的无机酸成盐一 呈碱性 R-NH2 HCI R一+NH3CI 碱性强弱顺序:脂肪胺>NH,>芳香胺 pKb 3-4.54.75 9—10 在脂肪胺中:RNH2<R,NH>R,N 一级二级 .三级 Organic Chem
Organic Chem a. 胺的碱性与酸性 i. 碱性 N上的未共用电子对能接受一个质子, 与大多数的无机酸成盐——呈碱性 R NH2 + HCl R + NH3 Cl 碱性强弱顺序:脂肪胺 > NH3 > 芳香胺 pKb 3—4.5 4.75 9—10 在脂肪胺中:RNH2 < R2NH > R3N 一级 二级 三级

一 些常见的胺的pKb值: 化合物 pKb(25℃) 化合物 pKb(25℃) NH3 4.75 C2HsNH2 3.36 CH.NH2 3.38 (C2H3)NH 3.06 (CH3)NH 3.27 (C2Hs)3N 3.25 (CH3)N 4.21 (bN阳 13.8 NH2 9.4 CH3- NH28.0 14.3 Organic Chem
Organic Chem 一些常见的胺的pKb值: 化合物 pKb(25℃) 化合物 pKb(25℃) NH3 4.75 C2H5NH2 3.36 CH3NH2 3.38 (C2H5 ) 2NH 3.06 (CH3 ) 2NH 3.27 (C2H5 ) 3N 3.25 (CH3 ) 3N 4.21 NH 2 13.8 NH2 9.4 CH3 NH2 8.0 NO2 NH2 14.3

从电子效应看:R基给电子,使N上的电子云更集中, 孤对电子接受H的能力增强,碱性顺序应是:RN >R2NH>RNH2>NH3,(在气相中测定或非质子性溶 剂中(如CHCl3,CH3CN,Ph-CI等)测定确按此顺序) 。 从溶剂效应和空间位阻效应看:N上取代基多,与H,O 形成氢键少,与H+结合形成铵离子后,溶剂化稳定作 用弱,碱性减弱。 ·N上的取代基多了,空间障碍就不利于N接受H+一碱 性减弱。 ·具体的胺的碱性是这两种相反因素协同作用的结果, 一级胺与三级胺哪个碱性强,要看是什么烃基,不同 的烃基得出的次序可能不同。 芳胺的碱性较弱,主要是p-π共轭,N上电子云向苯环 转移,N原子与质子结合能力降低。 Organic Chem
Organic Chem • 从电子效应看:R基给电子,使N上的电子云更集中, 孤对电子接受H +的能力增强,碱性顺序应是:R3N >R2NH > RNH2> NH3,(在气相中测定或非质子性溶 剂中(如CHCl3,CH3CN,Ph-Cl等)测定确按此顺序) • 从溶剂效应和空间位阻效应看:N上取代基多,与H2O 形成氢键少,与H+结合形成铵离子后,溶剂化稳定作 用弱,碱性减弱。 • N上的取代基多了,空间障碍就不利于N接受H+——碱 性减弱。 • 具体的胺的碱性是这两种相反因素协同作用的结果, 一级胺与三级胺哪个碱性强,要看是什么烃基,不同 的烃基得出的次序可能不同。 • 芳胺的碱性较弱,主要是p-π共轭,N上电子云向苯环 转移,N原子与质子结合能力降低

ii.酸性 伯、仲胺中N-H键可电离, R2NHR2N+H 酸性很弱。例如(C2H)2NH,pKa=36 iPr2Ng+n-C4,iTH亚, (i-Pr)2NLi n-C4H10 pKa 40 LDA 50 Organic Chem
Organic Chem ii. 酸性 伯、仲胺中N-H键可电离, 酸性很弱。例如(C2H5)2NH,pKa=36 R2 NH R2 N - + H + (i-Pr) 2 NH + n-C4 H9 Li THF (i-Pr) 2 NLi + n-C4 H10 pKa ~40 LDA ~50