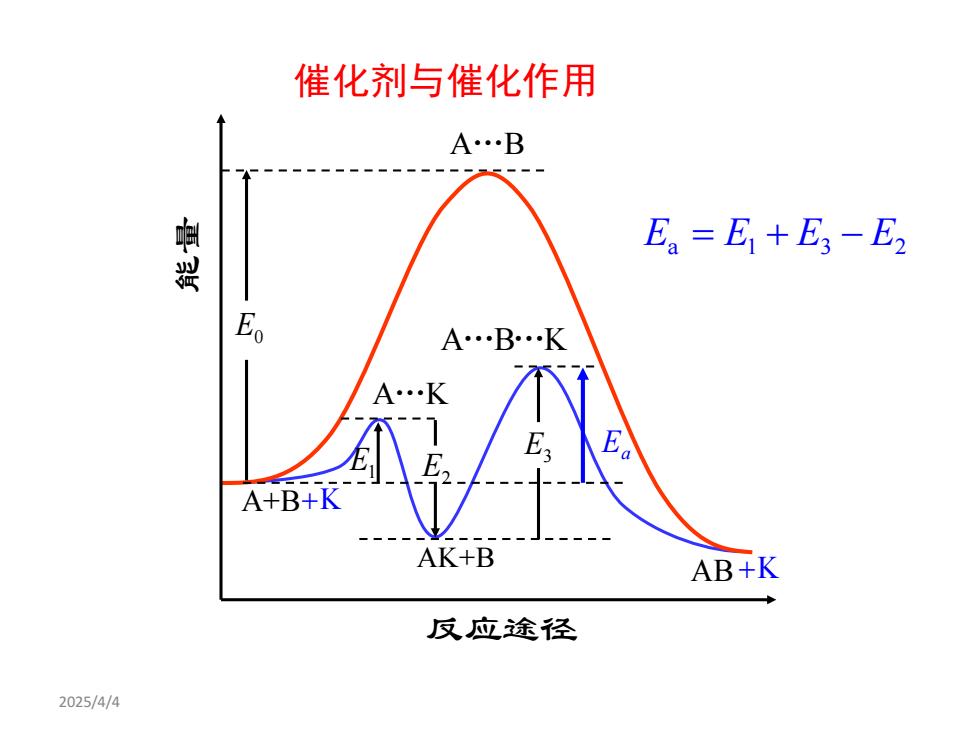
催化剂与催化作用A..B鲁骐E =E +E,-E,E.A...B...KA.KAEE,EE21A+B+KAK+BAB+K反应途径2025/4/4
2025/4/4 A B . A B K . . A K . A+B AK+B AB E1 反应途径 能量 E0 E2 E3 Ea +K +K E E E E a 1 3 2 = + − 催化剂与催化作用
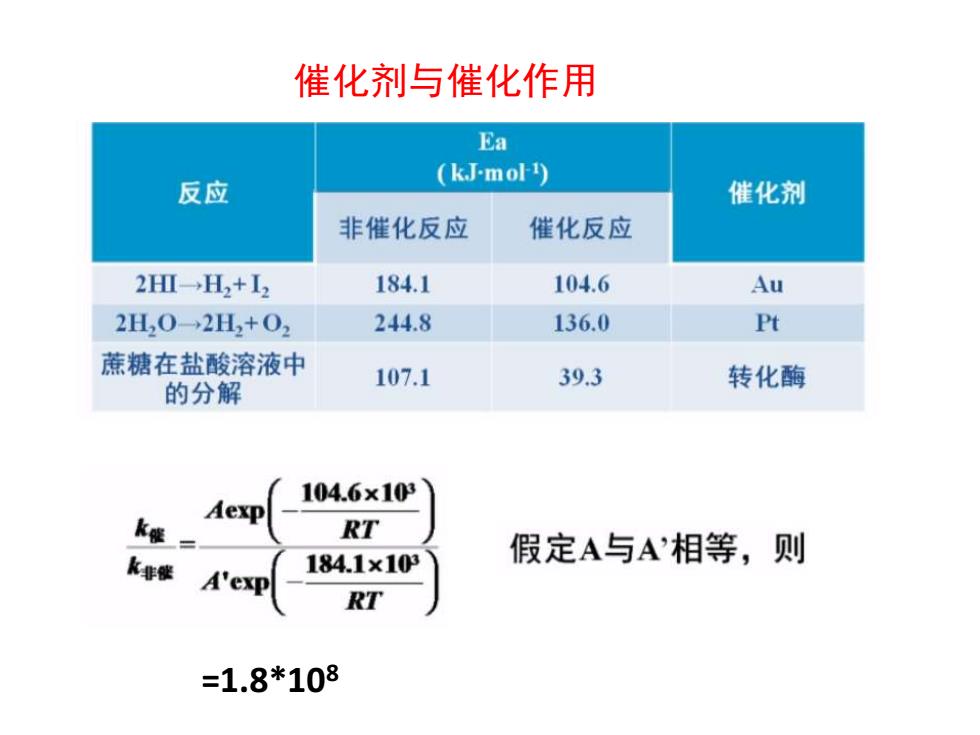
催化剂与催化作用Ea(kJ-mol)反应催化剂催化反应非催化反应184.1104.62HI-H+I2AuPt244.8136.02H0-2H+0蔗糖在盐酸溶液中转化酶107.139.3的分解104.6x103AexpRTKo假定A与A相等,则184.1x103k非俄A'expRT=1.8*108
催化剂与催化作用 =1.8*108

催化剂与催化作用也有某些催化反应,活化能降低得不多,而反应速率却改变很大。有时也发现同一反应在不同的催化剂上反应,其活化能相差不大,而反应速率相差很大,这种情况可由活化摘的改变来解释。4*seE△.Hk = (c0)"mmexpexpRRTE0= AexpRT如果活化改变很大,相当于指前因子改变很大,也可以明显地改变速率常数值。2025/4/4
2025/4/4 也有某些催化反应,活化能降低得不多,而反应速率却 改变很大。有时也发现同一反应在不同的催化剂上反应,其 活化能相差不大,而反应速率相差很大,这种情况可由活化 熵的改变来解释。 ( ) ( ) 1 B r m r m r exp exp k T S H n k c h R RT − = − a exp E A RT = − 如果活化熵改变很大,相当于指前因子改变很大,也 可以明显地改变速率常数值。 催化剂与催化作用

催化剂与催化作用催化反应的特点1.催化剂加速反应速率的本质是改变了反应的历程,降低了整个反应的表观活化能2.催化剂在反应前后,化学性质没有改变,但物理性质可能会发生改变,3.催化剂不影响化学平衡,不能改变反应的方向和限度,催化剂同时加速正向和逆向反应的速率,使平衡提前到达。即不能改变热力学函数 △,Gm,△,G的值2025/4/4
2025/4/4 催化反应的特点 2.催化剂在反应前后,化学性质没有改变,但物理性 质可能会发生改变。 即不能改变热力学函数 r m r m G G , 的值 1.催化剂加速反应速率的本质是改变了反应的历程, 降低了整个反应的表观活化能。 3.催化剂不影响化学平衡,不能改变反应的方向和 限度,催化剂同时加速正向和逆向反应的速率,使平 衡提前到达。 催化剂与催化作用
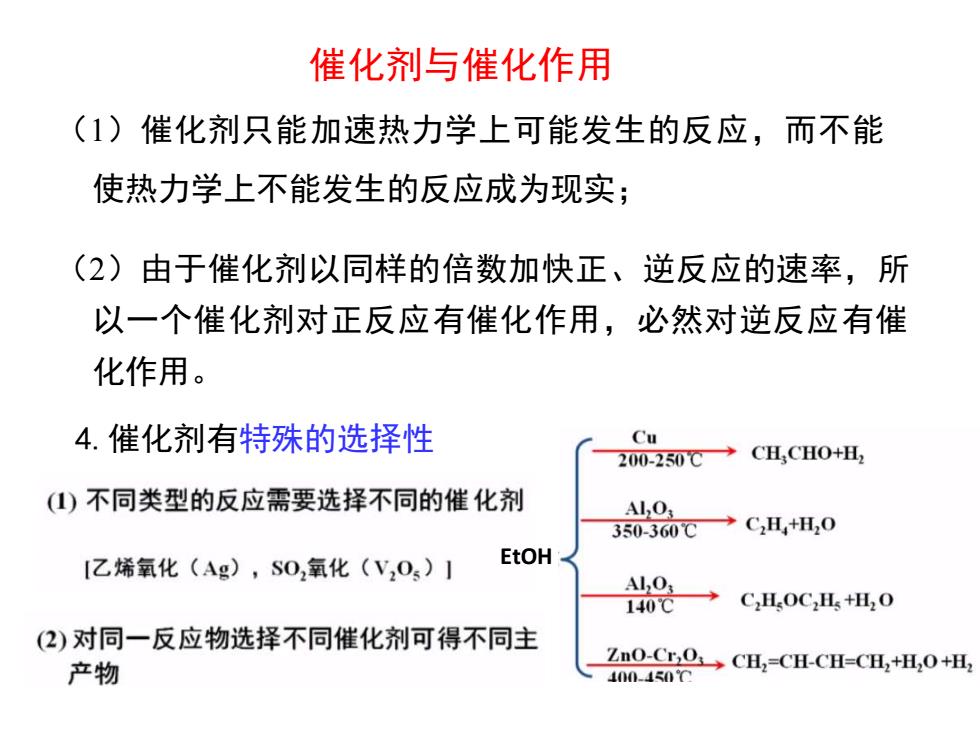
催化剂与催化作用(1)催化剂只能加速热力学上可能发生的反应,而不能使热力学上不能发生的反应成为现实:(2)由于催化剂以同样的倍数加快正、逆反应的速率,所以一个催化剂对正反应有催化作用,必然对逆反应有催化作用。Cu4.催化剂有特殊的选择性CH,CHO+H,200-250℃1)不同类型的反应需要选择不同的催化剂Al,OC,H,+H,0350-360℃EtOH[乙烯氧化(Ag),SO,氧化(VO,)】Al,OC,HoC,H+H,o140℃(2)对同一反应物选择不同催化剂可得不同主ZnO-Cr,OCH,=CH-CH=CH,+H,O+H产物100-450℃
(1)催化剂只能加速热力学上可能发生的反应,而不能 使热力学上不能发生的反应成为现实; (2)由于催化剂以同样的倍数加快正、逆反应的速率,所 以一个催化剂对正反应有催化作用,必然对逆反应有催 化作用。 催化剂与催化作用 4.催化剂有特殊的选择性 EtOH