
掌握配合物的组成和命名:配位平衡的基本概念和配位平衡移动的有关计算 熟悉配合物的价键理论、晶体场理论的基本要点和应用:整合物的结构和性质。 了解配合物的几何异构现象、配合物的分类、羟基配合物和配合物的应用。 3.教学重点难点 重点:配合物的组成和命名,配合物的价键理论,配合物的晶体场理论的基本要点和应 用,配位平衡的基本概念和配位平衡移动的有关计算。 难点:配合物的价键理论,配合物的品体场理论,配位平衡移动的有关计算。 4.数学建议:使用多媒体授课。 第十一章:s区元素 1.基本内容: 氢,碱金属和碱土金属,水的硬度与净化。 2.教学基本要求: 了解水的硬度和水质净化的几种方法,氢化物的类型及特点,s区元素在医学检验及医学 中的一些应用。 熟悉s区元素的电子构型与性质递变关系 掌握s区元素的重要化合物的结构、性质。 3.教学重点难点: 重点:氢化物,碱金属和碱土金属的通性及重要的化合物,硬度及其表示法,水质净化 的方法。 难点:重要化合物的性质递变规律。 4.教学建议:使用多媒体授课。 第十二章:p区元素 1.基本内容: P区元素概述,卤素,氧族元素,氮族元素,碳族元素,阴族元素,P区元素在医学检验 和药学中的一些应用 2.教学基本要求 了解p区元素的基本性质与其电子层结构的关系。 了解某些单质、常见氧化物、含氧酸及含氧酸根的结构。 了解惰性电子对效应、离域π键、氢桥键、RO州规则、等电子体和缺电子原子等基本概念。 熟悉P区元素重要化合物的主要化学性质及其变化规律。 16
16 掌握配合物的组成和命名;配位平衡的基本概念和配位平衡移动的有关计算。 熟悉配合物的价键理论、晶体场理论的基本要点和应用;螯合物的结构和性质。 了解配合物的几何异构现象、配合物的分类、羟基配合物和配合物的应用。 3. 教学重点难点: 重点:配合物的组成和命名,配合物的价键理论,配合物的晶体场理论的基本要点和应 用,配位平衡的基本概念和配位平衡移动的有关计算。 难点: 配合物的价键理论,配合物的晶体场理论,配位平衡移动的有关计算。 4. 教学建议:使用多媒体授课。 第十一章:s 区元素 1. 基本内容: 氢,碱金属和碱土金属,水的硬度与净化。 2. 教学基本要求: 了解水的硬度和水质净化的几种方法,氢化物的类型及特点,s 区元素在医学检验及医学 中的一些应用。 熟悉 s 区元素的电子构型与性质递变关系。 掌握 s 区元素的重要化合物的结构、性质。 3. 教学重点难点: 重点:氢化物,碱金属和碱土金属的通性及重要的化合物,硬度及其表示法,水质净化 的方法。 难点:重要化合物的性质递变规律。 4. 教学建议:使用多媒体授课。 第十二章:p 区元素 1. 基本内容: P 区元素概述,卤素,氧族元素,氮族元素,碳族元素,硼族元素,p 区元素在医学检验 和药学中的一些应用。 2. 教学基本要求: 了解 p 区元素的基本性质与其电子层结构的关系。 了解某些单质、常见氧化物、含氧酸及含氧酸根的结构。 了解惰性电子对效应、离域π键、氢桥键、ROH 规则、等电子体和缺电子原子等基本概念。 熟悉 p 区元素重要化合物的主要化学性质及其变化规律

熟悉p区元素各主要氧化态的氧化还原性。 3.教学重点难点: 重点:P区元素的卤化氢和卤化物、卤素的含氧酸及其盐、硫化物及硫的含氧酸、氮的氢 化物及氨的含氧化合物、碳的化合物、碳的氧化物、硼的化合物的性质及其变化规律 难点:含氧酸的结构特征,各种化合物性质之间的变化规律。 4.教学建议:使用多媒体授课。 第十三章:d区元素 1.基本内容: d区元素概述,铬、钼,锰,铁、钴、镍,铂系元素简介,铜、银、金,锌、镉、汞,d 区元素在医学检验及医药学中的一些应用。 2.教学基本要求: 掌握区元素原子的价电子结构特征及通性:铬、锰、铁、钻、镍、铜、银、锌、汞等 元素的主要性质及重要离子的鉴别与分离方法。 熟悉铬(Ⅲ)氧化物和氢氧化物的酸碱性,铬(Ⅲ)的还原性和铬(Ⅵ)的氧化性以及 貉酸盐和重铬酸盐的互变性:锰化合物的氧化还原性:铁系元素重要化合物的酸碱性、氧化还 原性及配位性:铜、银、锌、汞氧化物、氢氧化物及其重要盐类的性质:铜(【)和铜(Ⅱ)入 汞(I)和汞(Ⅱ)之间的相互转化规律。 了解d区元素在医学上的应用。 3.教学重点难点: 重点:铬、锰、铁、钴、镍、铜、银、锌、汞单质及其重要化合物的性质。 难点:过度元素性质的变化规律。 4.教学建议:使用多媒体授课。 第十四章:镧系、钢系、稀有气体 1.基本内容: 镧系元素,铜系元素,稀有气体 2.教学基本要求: 了解镧系、钢系元素的性质。 熟悉镧系收缩、钢系收缩及其影响。 了解稀有气体的性质和用途 3.教学重点难点: 17
17 熟悉 p 区元素各主要氧化态的氧化还原性。 3. 教学重点难点: 重点:p 区元素的卤化氢和卤化物、卤素的含氧酸及其盐、硫化物及硫的含氧酸、氮的氢 化物及氮的含氧化合物、磷的化合物、碳的氧化物、硼的化合物的性质及其变化规律。 难点: 含氧酸的结构特征,各种化合物性质之间的变化规律。 4. 教学建议:使用多媒体授课。 第十三章:d 区元素 1. 基本内容: d 区元素概述,铬、钼,锰,铁、钴、镍,铂系元素简介,铜、银、金,锌、镉、汞,d 区元素在医学检验及医药学中的一些应用。 2. 教学基本要求: 掌握 d 区元素原子的价电子结构特征及通性;铬、锰、铁、钴、镍、铜、银、锌、汞等 元素的主要性质及重要离子的鉴别与分离方法。 熟悉铬(Ⅲ)氧化物和氢氧化物的酸碱性,铬(Ⅲ)的还原性和铬(Ⅵ)的氧化性以及 铬酸盐和重铬酸盐的互变性;锰化合物的氧化还原性;铁系元素重要化合物的酸碱性、氧化还 原性及配位性;铜、银、锌、汞氧化物、氢氧化物及其重要盐类的性质;铜(Ⅰ)和铜(Ⅱ)、 汞(Ⅰ)和汞(Ⅱ)之间的相互转化规律。 了解 d 区元素在医学上的应用。 3. 教学重点难点: 重点:铬、锰、铁、钴、镍、铜、银、锌、汞单质及其重要化合物的性质。 难点: 过度元素性质的变化规律。 4. 教学建议:使用多媒体授课。 第十四章:镧系、锕系、稀有气体 1. 基本内容: 镧系元素,锕系元素,稀有气体。 2. 教学基本要求: 了解镧系、锕系元素的性质。 熟悉镧系收缩、锕系收缩及其影响。 了解稀有气体的性质和用途。 3. 教学重点难点:

重点:镧系、钢系元素的性质,稀有气体的性质和用途。 难点:铜系、铜系元素的性质的变化规律。 4.教学建议:使用多媒体授课 第十五章:生命元素及其在生物体内的作用 1.基本内容: 生命元素,生命元素的生理功能。 2.教学基本要求: 了解生命元素的分类和它们在周期表中的位置。 了解宏量元素和微量元素的生物功能以及生命元素过量时的危害。 3.教学重点难点: 重点:生命元素的分类及生理功能 难点:宏量元素和微量元素的生物功能 4.教学建议:使用多媒体授课 第十六章:环境中常见的无机化合物污染 1.基本内容 大气中主要无机污染物,地面水主要无机污染物,土壤中的无机污染物。 2.教学基本要求: 了解环境中常见的无机物污染。 了解无机物污染对环境、人类健康及生活的影响。 3.教学重点难点: 重点:大气、地面水和土壤中的无机污染物。 难点:无机物污染对环境、人类健康及生活的影响 4.教学建议:使用多媒体授课 四、教学环节与学时分配 序 总学 其 教学内容 课外辅导/备 号 时 讲课实验上机其他课外实践注 1论、溶液和胶体 2电解质溶液 3 3沉淀溶解平衡 3 4缓冲溶液 5 化学反应中的能量变化 5 6化学反应速率 3
18 重点:镧系、锕系元素的性质,稀有气体的性质和用途。 难点: 镧系、锕系元素的性质的变化规律。 4. 教学建议:使用多媒体授课 第十五章:生命元素及其在生物体内的作用 1. 基本内容: 生命元素,生命元素的生理功能。 2. 教学基本要求: 了解生命元素的分类和它们在周期表中的位置。 了解宏量元素和微量元素的生物功能以及生命元素过量时的危害。 3. 教学重点难点: 重点:生命元素的分类及生理功能。 难点: 宏量元素和微量元素的生物功能。 4. 教学建议:使用多媒体授课 第十六章:环境中常见的无机化合物污染 1. 基本内容: 大气中主要无机污染物,地面水主要无机污染物,土壤中的无机污染物。 2. 教学基本要求: 了解环境中常见的无机物污染。 了解无机物污染对环境、人类健康及生活的影响。 3. 教学重点难点: 重点:大气、地面水和土壤中的无机污染物。 难点: 无机物污染对环境、人类健康及生活的影响。 4. 教学建议:使用多媒体授课 四、教学环节与学时分配 序 号 教学内容 总学 时 其 中 课外辅导/ 课外实践 备 讲课 实验 上机 其他 注 1 绪论、溶液和胶体 4 4 2 电解质溶液 3 3 3 沉淀溶解平衡 3 3 4 缓冲溶液 2 2 5 化学反应中的能量变化 5 5 6 化学反应速率 3 3
7氨化还原与电极电势5 8原子结枸和元素周期律 5 9共价键和分子间作用力4 10s区元素 2 1p区元素 3 12配位化合物 5 13d区元素 3 14镧系、锕系、稀有气体1 15 生命元素及其在生物体 自学 内的作用 环境中常见的无机化合 16物污来 0 自学 五、教学中应注意的问题: 结合专业学生,理论联系实际 六、实验内容: 见《无机化学B》课程实践教学大纲 七、考核方式: 见《无机化学B》课程考试大纲 八、教材及主要参考书: 1、选用教材: 《无机化学》第二版,谢吉民主编,人民卫生出版社,2013年 2、主要参考书: 《基础化学》第三版,胡琴、祁嘉义主编,高等教育出版社,2014年 九、教改说明及其他: 执笔人:王晓娟系室审核人:肖锡林 19
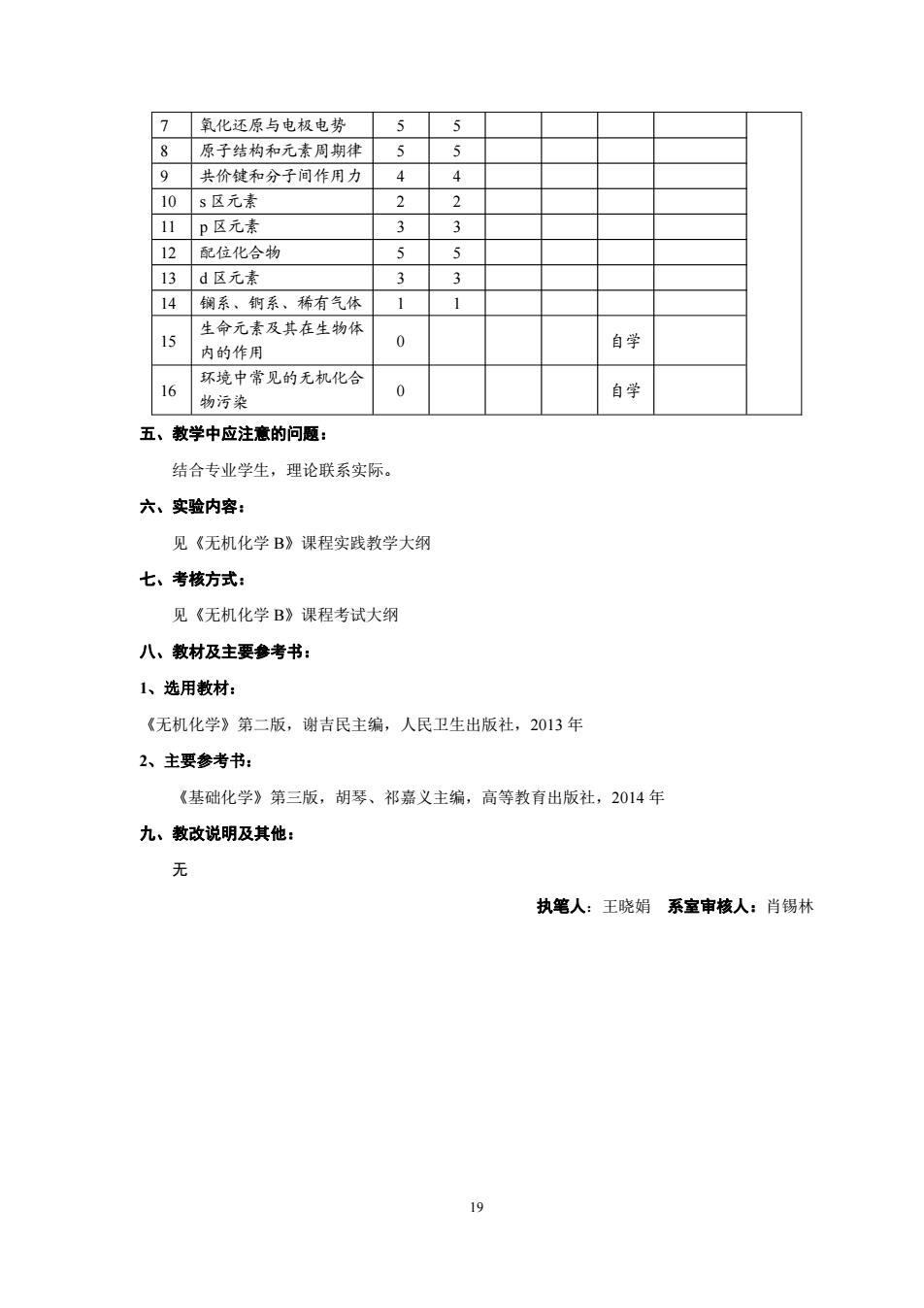
19 7 氧化还原与电极电势 5 5 8 原子结构和元素周期律 5 5 9 共价键和分子间作用力 4 4 10 s 区元素 2 2 11 p 区元素 3 3 12 配位化合物 5 5 13 d 区元素 3 3 14 镧系、锕系、稀有气体 1 1 15 生命元素及其在生物体 内的作用 0 自学 16 环境中常见的无机化合 物污染 0 自学 五、教学中应注意的问题: 结合专业学生,理论联系实际。 六、实验内容: 见《无机化学 B》课程实践教学大纲 七、考核方式: 见《无机化学 B》课程考试大纲 八、教材及主要参考书: 1、选用教材: 《无机化学》第二版,谢吉民主编,人民卫生出版社,2013 年 2、主要参考书: 《基础化学》第三版,胡琴、祁嘉义主编,高等教育出版社,2014 年 九、教改说明及其他: 无 执笔人:王晓娟 系室审核人:肖锡林

《无机化学B》课程考试大纲 Inorganic Chemistry 课程编号:130805024 总学时数:48 学分:3 一、考试对象: 修完本课程规定的各专业学生。 二、考试目的 本课程考试目的是使学生了解现代无机化学的基本理论,具备必要的化学基本知识和一定 的基本技能,为后续课程学习和掌握新的科学技术打下必要的基础。 三、考试要求 本课程是一门专业基础课,要求学生掌握物质结构的基础理论、化学反应的基本原理、溶 液的性质、化学平衡及元素化学的基本知识和实验的基本技能:培养学生具有独立思考、分析 和解决问题的能力。 四、考试内容与要求 第一章:绪论、溶液和胶体5-8分值 1.考试内容:物质的量浓度、质量浓度、质量分数、摩尔分数的概念及相互换算,稀溶液的 蒸气压下降、沸点上升、凝固点降低和渗透压力四个依数性和变化规律:溶胶的光学性质、动 力学性质和电学性质:影响溶胶聚沉的因素。 2,考试要求:能进行溶液各种组成标度之间的换算,稀溶液依数性的判断。 第二章:电解质溶液 8-10分值 1考试内容:水溶液中的质子转移平衡及有关计算,酸碱理论。 2.考试要求:能进行弱酸弱碱有关pH的计算:考察影响pH的因素。 第三章:沉淀溶解平衡 10-15分值 1考试内容:溶度积规则及有关计算:稀释效应、同离子效应、盐效应及对弱电解质的电离 平衡的影响:溶度积Kp·溶度积规则。 2.考试要求:能进行溶度积与溶解度相互运算,能进行沉淀反应的相关计算。 了解:分步沉淀及转化。 第四章:缓冲溶液 5-8分值 20
20 《无机化学 B》课程考试大纲 Inorganic Chemistry 课程编号:130805024 总学时数:48 学分:3 一、考试对象: 修完本课程规定的各专业学生。 二、考试目的 本课程考试目的是使学生了解现代无机化学的基本理论,具备必要的化学基本知识和一定 的基本技能,为后续课程学习和掌握新的科学技术打下必要的基础。 三、考试要求 本课程是一门专业基础课,要求学生掌握物质结构的基础理论、化学反应的基本原理、溶 液的性质、化学平衡及元素化学的基本知识和实验的基本技能;培养学生具有独立思考、分析 和解决问题的能力。 四、考试内容与要求 第一章:绪论、溶液和胶体 5-8 分值 1.考试内容:物质的量浓度、质量浓度、质量分数、摩尔分数的概念及相互换算,稀溶液的 蒸气压下降、沸点上升、凝固点降低和渗透压力四个依数性和变化规律;溶胶的光学性质、动 力学性质和电学性质;影响溶胶聚沉的因素。 2.考试要求:能进行溶液各种组成标度之间的换算,稀溶液依数性的判断。 第二章:电解质溶液 8-10 分值 1.考试内容:水溶液中的质子转移平衡及有关计算,酸碱理论。 2.考试要求:能进行弱酸弱碱有关 pH 的计算;考察影响 pH 的因素。 第三章:沉淀溶解平衡 10-15 分值 1.考试内容:溶度积规则及有关计算;稀释效应、同离子效应、盐效应及对弱电解质的电离 平衡的影响;溶度积 Ksp,溶度积规则。 2.考试要求:能进行溶度积与溶解度相互运算,能进行沉淀反应的相关计算。 了解:分步沉淀及转化。 第四章:缓冲溶液 5-8 分值