
§15-1原子核的基本性质 一、原子核的电荷和质量 1.原子核的电荷 原子核带有正电荷,原子核中的电荷由质子数Z 决定,质子数Z等于核外电子数,它决定了原子在周 期表中的位置与次序,因此Z又称为原子序数。 原子核所带电量是电子电量的整数倍:q=Z 让式不觉返司退
上页 下页 返回 退出 原子核带有正电荷,原子核中的电荷由质子数Z 决定,质子数Z等于核外电子数,它决定了原子在周 期表中的位置与次序,因此Z又称为原子序数。 原子核所带电量是电子电量的整数倍:q=Ze 1.原子核的电荷 §15-1 原子核的基本性质 一、原子核的电荷和质量

2.原子核的质量 原子核的质量等于原子的质量减去核外电子的 质量。由于核外电子的质量极小,原子核的质量与 原子的质量相差极小。 原子核的质量等于质子的质量加中子的质量。 原子质量单位(:选碳的同位素2原子质量 的1/12为一个原子质量单位(u: 1 12×10-3 lu 126.022×1023 =1.6606×1027kg 女意不贰通回退
上页 下页 返回 退出 原子质量单位(u):选碳的同位素 原子质量 的1/12为一个原子质量单位(u): 12 6 C 2.原子核的质量 3 27 23 1 12 10 1 1.6606 10 12 6.022 10 u kg − − = = 原子核的质量等于原子的质量减去核外电子的 质量。由于核外电子的质量极小,原子核的质量与 原子的质量相差极小。 原子核的质量等于质子的质量加中子的质量
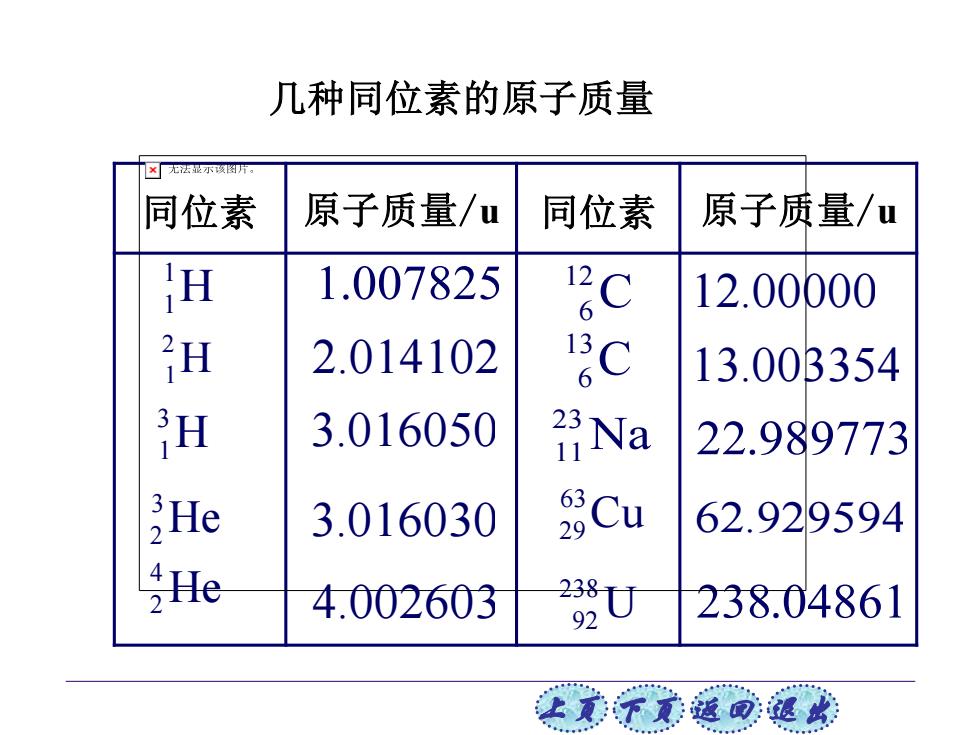
几种同位素的原子质量 同位素 原子质量/u 同位素 原子质量/u 1.007825 12.00000 3H 2.014102 6 13.003354 3H 3.016050 Na 22.989773 3He 3.016030 SCu 62.929594 He 4.002603 8U 9 238.04861 让元不觉返司退
上页 下页 返回 退出 同位素 原子质量/u 同位素 原子质量/u 238 92U 22.989773 62.929594 238.04861 12.00000 13.003354 23 11Na 63 29Cu 12 6 C 13 6 C 1 1 H 2 1 H 3 1 H 3 2 He 4 2 He 1.007825 2.014102 3.016050 3.016030 4.002603 几种同位素的原子质量

由表可见,以“原子质量单位”()计算原子的质 量时,原子质量都接近于一个整数,这个整数称为 原子核的质量数,或称核子数,以A表示。 原子核通常用质量数(4)和电荷数(☑)来表示.若某 化学元素符号用X来表示,则该原子核表示为:X 核素:Z和A都相同的原子核称为某种核素。 同位素:Z相同而A不同的原子核称为同位素。同 位素有稳定同位素和放射性同位素之分。 放射性同位素:自发地衰变为其他元素,同时放 出一高能粒子
上页 下页 返回 退出 原子核通常用质量数(A)和电荷数(Z)来表示.若某 化学元素符号用X来表示,则该原子核表示为: 由表可见,以“原子质量单位”(u)计算原子的质 量时,原子质量都接近于一个整数,这个整数称为 原子核的质量数,或称核子数,以A表示。 同位素:Z相同而A不同的原子核称为同位素。同 位素有稳定同位素和放射性同位素之分。 核素:Z和A都相同的原子核称为某种核素。 放射性同位素:自发地衰变为其他元素,同时放 出一高能粒子。 X A Z

二、原子核的大小和形状 1.原子核的大小 原子核的半径大约10-14-10-15m,是原子 半径的104_10-5倍。 实验指出,核的体积正比于质量数A。若把原 子核看作球体,则 4 号TR3oeA,R3cA,R0A3 3 fm为飞米,则上式可写为 R=R4 (R=1.2×10-15m=1.2fm) R=1.243fm 让元子觉道司退欢
上页 下页 返回 退出 1. 原子核的大小 原子核的半径大约 10-14—10-15 m , 是原子 半径的 10-4— 10-5倍。 实验指出,核的体积正比于质量数A。若把原 子核看作球体,则 fm为飞米,则上式可写为 二、原子核的大小和形状 4 3 3 πR A , 3 R A , 1 3 R A 1 3 R R A = 0 15 0 ( 1.2 10 1.2 R m fm) − = = 1 3 R A =1.2 fm