
§3.5稀溶液的依数性 稀溶液:溶质浓度很低,可略溶质一溶质间 的相互作用,溶质的外围被溶剂包围。 在等T,P下,溶质的蒸气压只与溶质在溶液 中的溶解度有关,而与溶质的性质无关 依数性:体系某些性质只与溶质的数量有关, 而与溶质的本性无关 前提:溶质是不挥发的,气相仅为溶剂, 不生成固溶体 1
1 §3.5 稀溶液的依数性 稀溶液:溶质浓度很低,可略溶质—溶质间 的相互作用,溶质的外围被溶剂包围。 依数性:体系某些性质只与溶质的数量有关, 而与溶质的本性无关 在等 T,P 下,溶质的蒸气压只与溶质在溶液 中的溶解度有关,而与溶质的性质无关 前提:溶质是不挥发的,气相仅为溶剂, 不生成固溶体

依数性质:1)蒸气压降低 2)冰点降低 3)沸点升高 4)渗透压 1.蒸汽压降低 溶剂:PA=PAX4 AP=PA-PA=PA-PAXA=PAXE 蒸气压降低,只与溶质的数量有关, 而与溶质的性质无关 2
2 依数性质:1)蒸气压降低 3)沸点升高 2)冰点降低 4)渗透压 1.蒸汽压降低 ΔP= P* A- PA 溶剂:PA =P* AXA = P* A- P* A XA = P* A XB 蒸气压降低,只与溶质的数量有关, 而与溶质的性质无关

2.凝固点降低 凝固点T:s-1平衡温度 A(s)→A(1,Xa) ==4转(T,P)+RTLnX Ln,= 4- ,Gm R T RT 1. △H RT2 3
3 2.凝固点降低 A(s)→A(l,XA) s A = l A = l B * , (T,P)+ RTLnXA 凝固点 Tf:s-l 平衡温度 RT G R T LnX m l s l A s A A = − − = * , 1 2 [ ( )] 1 ( ) RT H T G T R T LnX m m l s P l s P A = = −
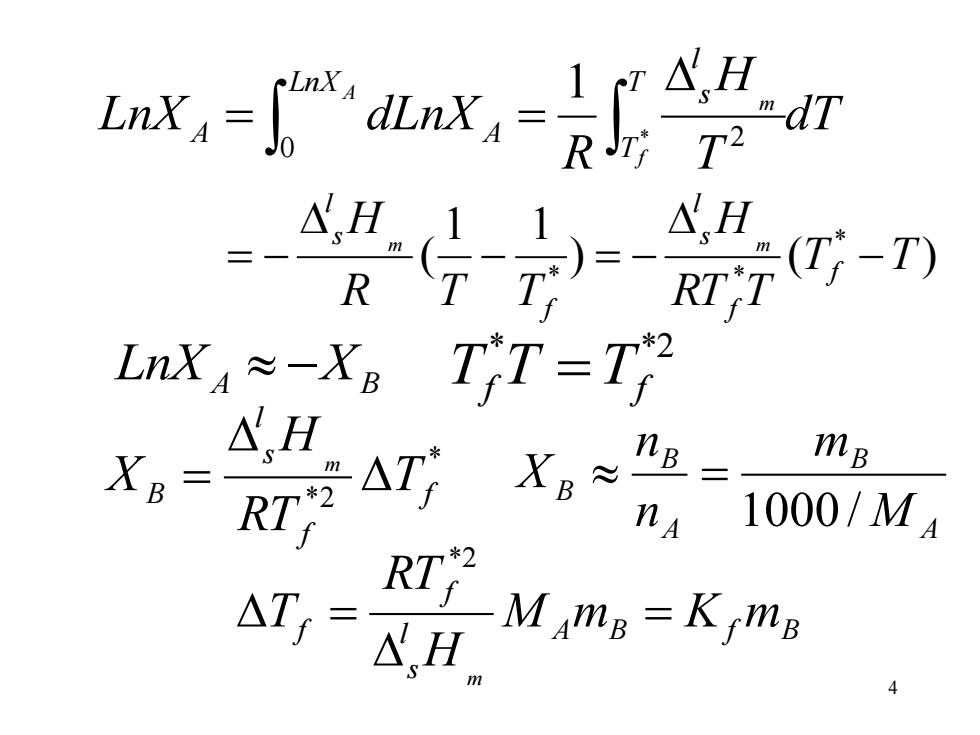
a式-了”ax, n dT △H R LnX4≈-XBTT=T △H XR= RT AT *2 XB≈ B mB 1000/MA BTM m-K ma △T=H
4 dT T H R LnX dLnX T T l s LnX A A f m A = = * 2 0 1 ) ( ) 1 1 ( * * * T T RT T H R T T H f f l s f l s m m − − = − = − * *2 A B Tf T =Tf LnX −X * *2 f f l s B T RT H X m = l A B f B s f f M m K m H RT T m = = *2 A B A B B M m n n X 1000 / =

△T=Kem Kf=△Hm M MA:Kgmol K:凝固点降低常数,只与溶剂A性质有关查表 m:为溶质B的质量摩尔浓度,mol/Kg △T=T*-TE>0 T*,T分别表示纯溶剂和稀溶液的凝固点 5
5 Kf :凝固点降低常数,只与溶剂 A 性质有关,查表 ΔTf = Tf * - Tf > 0 Tf * ,Tf分别表示纯溶剂和稀溶液的凝固点 mB:为溶质 B 的质量摩尔浓度,mol/Kg A fus m f f M H RT K = *2 MA:Kgmol-1 ΔTf =Kf mB