
导航 5.电解质的电离: ()电离:电解质 或 时,形成 的过程叫做电离。 (2)电离的表示方法一电离方程式。 用化学式和离子符号表示电离过程的式子叫做电离方程式。 ①强酸的电离(如NO3): ②强碱的电离(如NaOD: ③盐的电离(如CuSO4): ●
导航 5.电解质的电离: (1)电离:电解质 溶于水 或 受热熔化 时,形成 自由 移动的离子 的过程叫做电离。 (2)电离的表示方法——电离方程式。 用化学式和离子符号表示电离过程的式子叫做电离方程式。 ①强酸的电离(如 HNO3): HNO3 H+ +N𝐎𝟑 - 。 ②强碱的电离(如 NaOH): NaOH Na+ +OH- 。 ③盐的电离(如 CuSO4): CuSO4 Cu2++S𝐎𝟒 𝟐-

导 微判断2(1)Na2C03溶于水的电离方程式为Na2C03一 Na++C03。(×) (2)能电离的物质一定都能导电。(X) (3)水溶液中的氯化钠在电流的作用下电离出Na+和C。 (X) (4)NaHS04在水中能完全电离出Ht,所以它是一元强酸。 (X)
导航 微判断2(1)Na2CO3溶于水的电离方程式为Na2CO3══ ( ) (2)能电离的物质一定都能导电。( ) (3)水溶液中的氯化钠在电流的作用下电离出Na+和Cl-。 ( ) (4)NaHSO4在水中能完全电离出H+ ,所以它是一元强酸。 ( ) N𝐚𝟐 𝟐+ +C𝐎𝟑 𝟐- 。 × × × ×

导航 课堂·重难突破 电解质 重难归纳 1理解电解质的概念的“四个要点”。 四个要点 正确理解 误区警示 如铁丝、铜、石墨能导电,但不是 电解质是化合物, 电解质; 化合物 不是单质,也不是 盐酸、氯化钠溶液能导电,是混合 混合物 物,不是电解质
导航 一 电解质 重难归纳 1.理解电解质的概念的“四个要点” 。 四个要点 正确理解 误区警示 化合物 电解质是化合物, 不是单质,也不是 混合物 如铁丝、铜、石墨能导电,但不是 电解质; 盐酸、氯化钠溶液能导电,是混合 物,不是电解质 课堂·重难突破
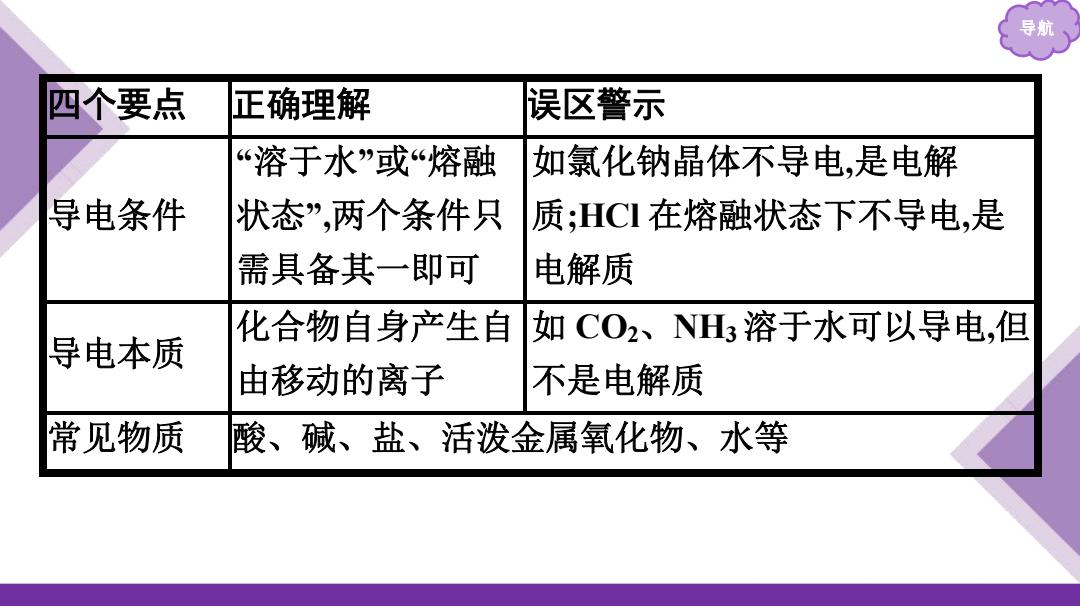
导航 四个要点 正确理解 误区警示 “溶于水”或“熔融 如氯化钠晶体不导电,是电解 导电条件 状态”,两个条件只 质;HCI在熔融状态下不导电,是 需具备其一即可 电解质 化合物自身产生自 如CO2、NL3溶于水可以导电,但 导电本质 由移动的离子 不是电解质 常见物质 酸、碱、盐、活泼金属氧化物、水等
导航 四个要点 正确理解 误区警示 导电条件 “溶于水”或“熔融 状态”,两个条件只 需具备其一即可 如氯化钠晶体不导电,是电解 质;HCl 在熔融状态下不导电,是 电解质 导电本质 化合物自身产生自 由移动的离子 如 CO2、NH3溶于水可以导电,但 不是电解质 常见物质 酸、碱、盐、活泼金属氧化物、水等
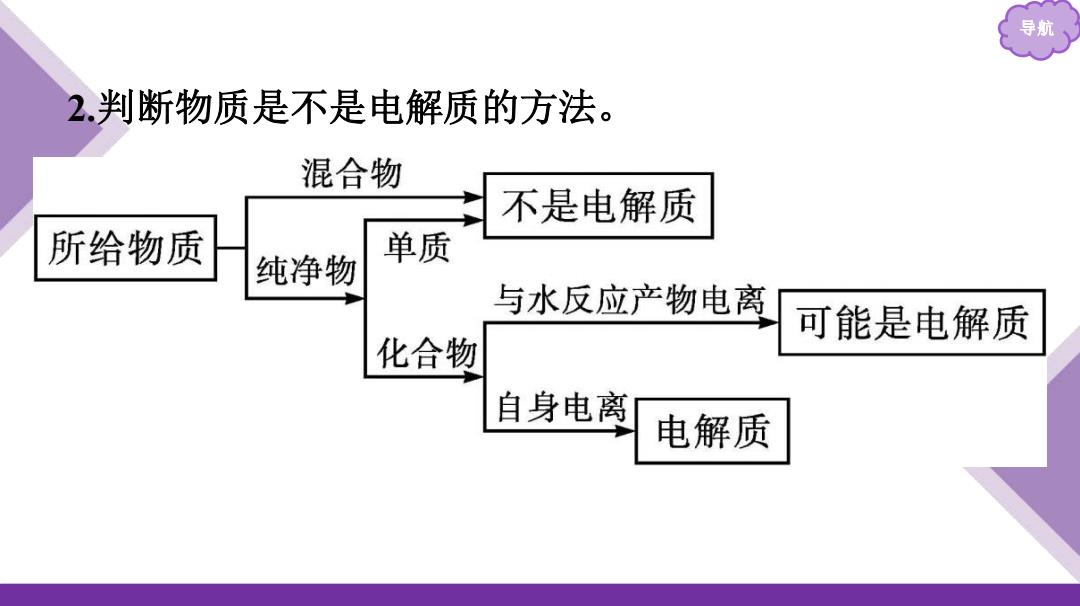
导航 2判断物质是不是电解质的方法。 混合物 不是电解质 所给物质 单质 纯净物 与水反应产物电离 可能是电解质 化合物 自身电离 电解质
导航 2.判断物质是不是电解质的方法