
3、酸碱反应由两个酸碱半反应构成例:HAc与NH,水中的反应半反应:+HHAc -Ac半反应:H++ NH, NH+H+总反应:HAc +NH,NHAc酸碱反应的实质一一酸碱间的质子授受过程质子的转移山东翟工大学11HANDONGUNIVTSTOTICINOLOGAnalytical Chemistry
Analytical Chemistry 11 3、酸碱反应 酸碱反应的实质——酸碱间的质子授受过程 质子的转移 ——由两个酸碱半反应构成 总反应: HAc + NH3 NH4Ac H+ 半反应: H+ + NH3 NH4 + 半反应: HAc Ac- + H+ 例: HAc与NH3 水中的反应

按质子理论,Na,HPO,是:A.中性物质B. 酸性物质C.碱性物质D.两性物质E.酸碱惰性物质答:D按质子理论,下列物质中何者具有两性?B. CO,2-C. HPO 2-A. HCO3D. NO3E. HS-E答:A、C、山东翟工大学12HANDOOUNVSRTOTTCINOLOAnalytical Chemistry
Analytical Chemistry 12 按质子理论,Na2HPO4是: A.中性物质 B. 酸性物质 C. 碱性物质 D. 两性物质 E. 酸碱惰性物质 按质子理论,下列物质中何者具有两性? A. HCO3 - B. CO3 2- C. HPO4 2- D. NO3 - E. HS- 答:D 答:A、 C、 E

酸碱反应类型与平衡常数二、1、溶剂分子之间的质子转移反应一质子自递反应H,O=H +OHH,O+H,O =H,O+OHK, =[H,O* [OH ] =[H ][OH ] = 1' 10- 14SH+SH = SH,++SK, =[SH, I[S" ]K一溶剂分子的质子自递常数山东翟工大学13HANDONGUNIVTSRTOTICINOLOGAnalytical Chemistry
Analytical Chemistry 13 1、溶剂分子之间的质子转移反应—质子自递反应 K—溶剂分子的质子自递常数 二、酸碱反应类型与平衡常数

2、酸碱溶质与溶剂分子间的反应一酸碱的解离HAc=Ac' +HHAc +H,O= Ac' +H,OK, =[Ac' I[H/HAc]K =[Ac lH,O+/[HAclK。一酸的解离常数NH,+H,O = NH +OHK一碱的解离常数K, =NHJIOH J/NH,酸碱的强弱取决于给出质子或接受质子的能力通常用解离常数的大小衡量。K,或(K.或K)-K,越大,酸碱强度越强。山东翟工大学14HANDONGUNIVTSTOTICINOLOGAnalytical Chemistry
Analytical Chemistry 14 2、酸碱溶质与溶剂分子间的反应—酸碱的解离 Ka—酸的解离常数 Kb—碱的解离常数 酸碱的强弱取决于给出质子或接受质子的能力, 通常用解离常数(Ka 或 Kb)的大小衡量。 Ka 或 Kb越大,酸碱强度越强
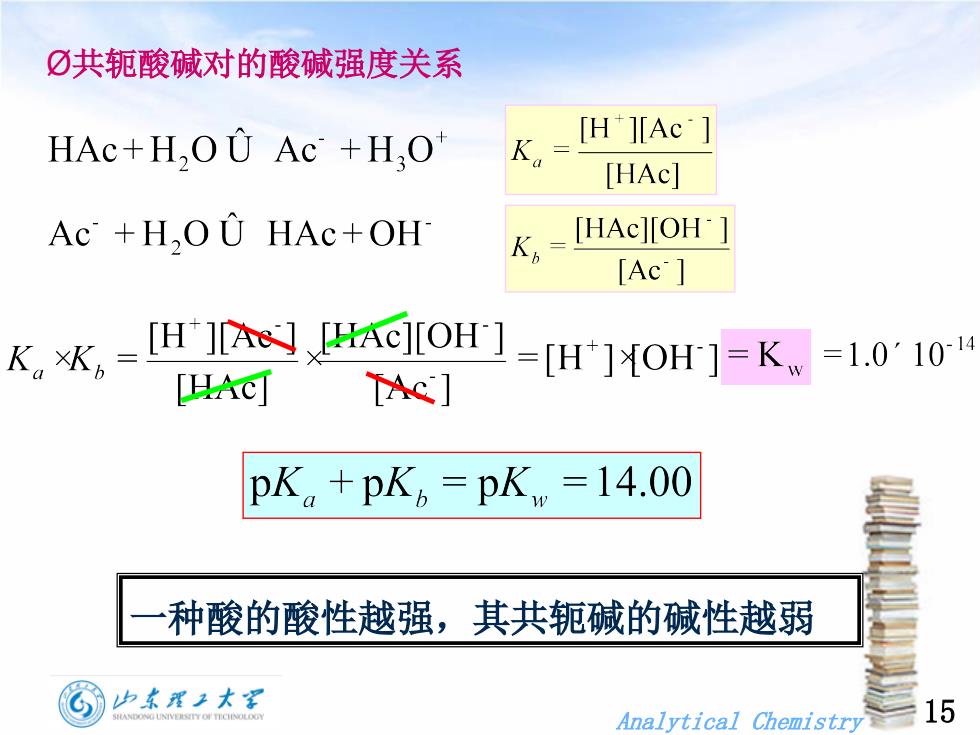
①共轭酸碱对的酸碱强度关系[H[AcHAc+H,U Ac +H,OK[HAc][HAc][OH'Ac' +H,OU HAc+OHK,[Ac ][H][A] [HAc][OH]=1.0°10-14K.xK.[H+]XOH] =K[Ac][HAC]pK.+pK, =pK=14.00一种酸的酸性越强,其共轭碱的碱性越弱山东翟工大学15HANDONGUNIVTSRTOTICINOLOGAnalytical Chemistry
Analytical Chemistry 15 Ø共轭酸碱对的酸碱强度关系 一种酸的酸性越强,其共轭碱的碱性越弱