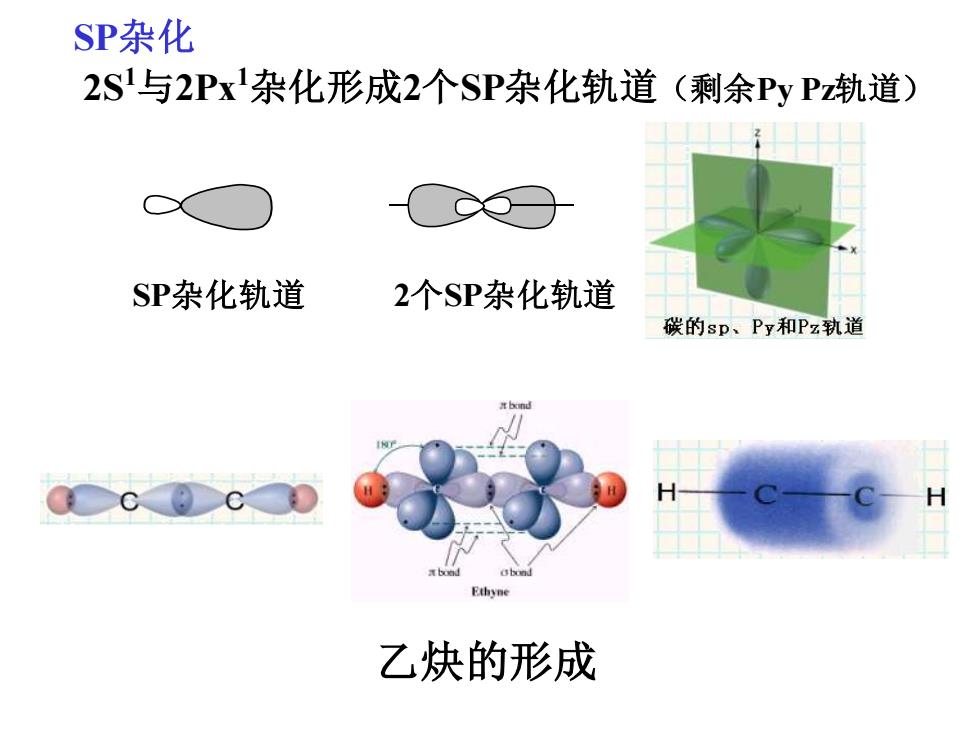
SP杂化2SI与2Pxl杂化形成2个SP杂化轨道(剩余PyPz轨道)SP杂化轨道2个SP杂化轨道碳的sp、Py和Pz轨道mHTEthyne乙炔的形成
SP杂化 2S1与2Px1杂化形成2个SP杂化轨道(剩余Py Pz轨道) SP杂化轨道 2个SP杂化轨道 乙炔的形成

共价键的种类极性键、非极性键按键的极性分:按共用电子对数分:单键、双键、三键按轨道重叠方式分:键、元键c键:成键轨道沿键轴重迭,“头碰头”元键:成键轨道平行重迭“肩并肩
共价键的种类 按键的极性分: 极性键、非极性键 按共用电子对数分:单键、双键、三键 按轨道重叠方式分:σ键、π键 σ键:成键轨道沿键轴重迭,“头碰头” π键:成键轨道平行重迭,“肩并肩

共价键一共价键的种类o键和T键的主要特点a键π键存在生成可单独存在,存在于任不能单独存在,只能与0何共价键中,键同时存在,成键轨道沿键轴重迭,成键轨道平行重迭,重迭程度较小.重迭程度大,性1.键能较大,较稳定,1.键能较小,较不稳定2.电子云受核约束大2.电子云受核约束小,易被极化.不易被极化质3.成键的两个原子间3.成键的两个原子不能沿键轴自由旋转可沿键轴自由旋转
σ键和π键的主要特点 共价键-共价键的种类 σ键 π键 存 在 可单独存在,存在于任 何共价键中. 不能单独存在,只能与σ 键同时存在. 生 成 成键轨道沿键轴重迭, 重迭程度大. 成键轨道平行重迭,重迭 程度较小. 性 质 1.键能较大,较稳定. 2.电子云受核约束大, 不 易被极化. 3.成键的两个原子间 可沿键轴自由旋转. 1.键能较小,较不稳定. 2.电子云受核约束小,易 被极化. 3.成键的两个原子不能 沿键轴自由旋转
有机化合物分子中的电子效应原子间的相互影响→电子效应:电子云密度分布对性质的影响分诱导效应和共轭效应两类空间效应:分子空间结构对性质的影响
有机化合物分子中的电子效应 原 子 间 的 相 互 影 响 分子空间结构对性质的影响 电子云密度分布对性质的影响 分诱导效应和共轭效应两类 电子效应: 空间效应:
吸电子诱导效应(-I)诱导效应斥电子诱导效应(+I)电子效应斥电子共轭效应(+C)共轭效应吸电子共轭效应(-C)
电子效应 诱导效应 吸电子诱导效应(-I) 斥电子诱导效应(+I) 共轭效应 斥电子共轭效应(+C) 吸电子共轭效应(-C)