·由物质的燃烧焓可直接求出化学反应的热效应: △,Hm0=∑(:△cHnm)反应物一∑(V:△cHm,i)产物 ·其理由可用下图表示.注意,相对有机化合物而言, 燃烧产物的能级一般比较低。 。设有反应: A+B=C+D A+B C+D △H反<0 △H>0 △H<0 C+D A+B △H产<0 △H产<0 △H反<0 燃烧产物C02等 燃烧产物C02等
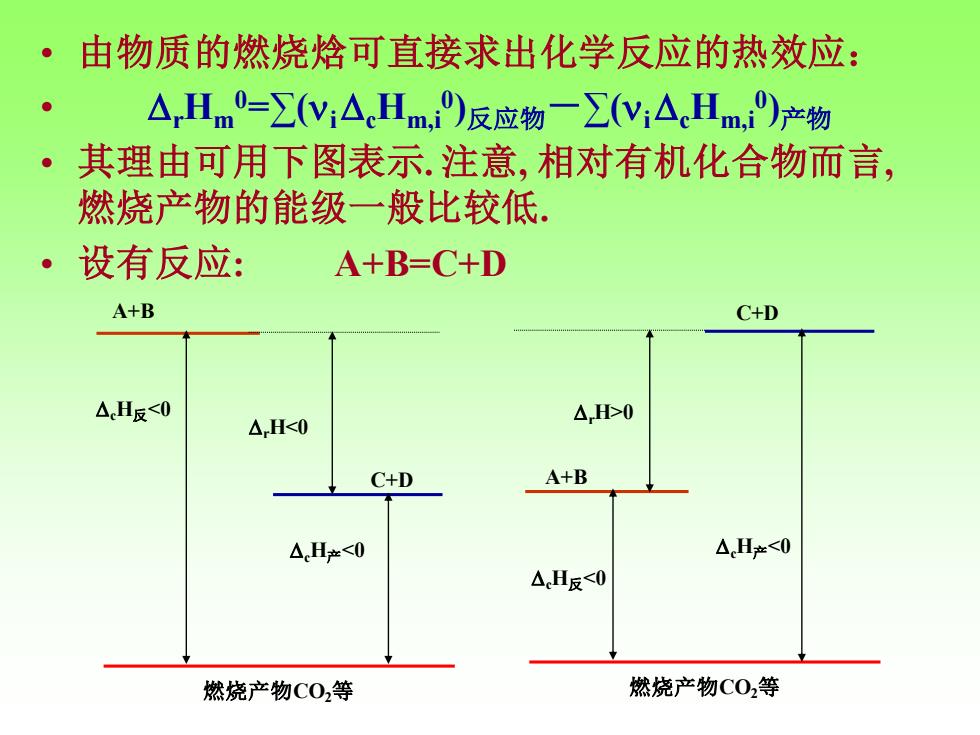
• 由物质的燃烧焓可直接求出化学反应的热效应: • rHm 0=∑(i cHm,i 0 )反应物-∑(i cHm,i 0 )产物 • 其理由可用下图表示. 注意, 相对有机化合物而言, 燃烧产物的能级一般比较低. • 设有反应: A+B=C+D 燃烧产物CO2等 A+B C+D cH反<0 cH产<0 rH<0 燃烧产物CO2等 A+B C+D cH反<0 cH产<0 rH>0

3。键焓 由化学键的键焓可以估算化学反应的热效应, 。 化学反应实质上是分子中的原子或原子团进行重新组合,一些 化学键断裂,一些化学键生成.反应的焓变就是这些键能的代 数和,所以由化学键能可以估算化学反应的焓变. 因为化学键键焓影响因素很多,故由键焓求出的反应焓变精度 不高,一般在无其它数据时,可用键焓对反应热进行估算 常见的化学键的键焓如下: H一H 435.9 kJ.mol-1 C-C 342 kJ.mol-1 C=C 613 kJ.mol-1 C≡C 845 kJ.mol-1 N-N 85 kJ.mol-1 0-0 139 kJ.mol-1 O一H 463 kJ.mol-1 N-H 354 kJ.mol-1
3. 键焓 • 由化学键的键焓可以估算化学反应的热效应. • 化学反应实质上是分子中的原子或原子团进行重新组合, 一些 化学键断裂, 一些化学键生成. 反应的焓变就是这些键能的代 数和, 所以由化学键能可以估算化学反应的焓变. • 因为化学键键焓影响因素很多, 故由键焓求出的反应焓变精度 不高, 一般在无其它数据时, 可用键焓对反应热进行估算. • 常见的化学键的键焓如下: • H-H 435.9 kJ.mol-1 • C-C 342 kJ.mol-1 • C=C 613 kJ.mol-1 • C≡C 845 kJ.mol-1 • N-N 85 kJ.mol-1 • O-O 139 kJ.mol-1 • O-H 463 kJ.mol-1 • N-H 354 kJ.mol-1