念,认识到持续自我完善的重要性,不断追求 进步。 (二)知识 系统全面地掌握本专业所必需的包括数学、物 2 指标点3.2 理学、化学、生物学、医学等学科的基础知识 第5-11章 和基本实践技能。并能用于指导未来的学习和 工作实践。 (三)能力 具有较强的创新和创业意识、人际沟通交流能 力、团队合作精神,以及初步的研发能力。掌 3 指标点33 握文献检索、相关专业信息获取的基本方法, 第5-11章 具有一定的科研能力。 指标点描述:同时化学是考研课程,掌握基本 化学知识达到研究生入学化学水平。 三、教学内容和学时分配 表2课程教学安排表 讲实实上 章节/单元 主要教学内容 课验贱机 主要教学方法 时 时学学 6 第五章化学分析 69 课堂教学 7 第六章酸碱平衡和酸碱滴定 128 课堂教学 8 第七章沉淀溶解平衡和沉淀滴定6 课堂教学 9 第八章配位平衡和配位滴定 94 课堂教学 10 第九章氧化还限平衡和氧化还原98 课堂教学 11 第十章吸光光度法 6 课堂教学与实验教学 合计 4833 第五章化学分析绪论 教学要求:了解本课程概况、学科分类、学习特点 教学内容:一、分析化学与农业科学的关系
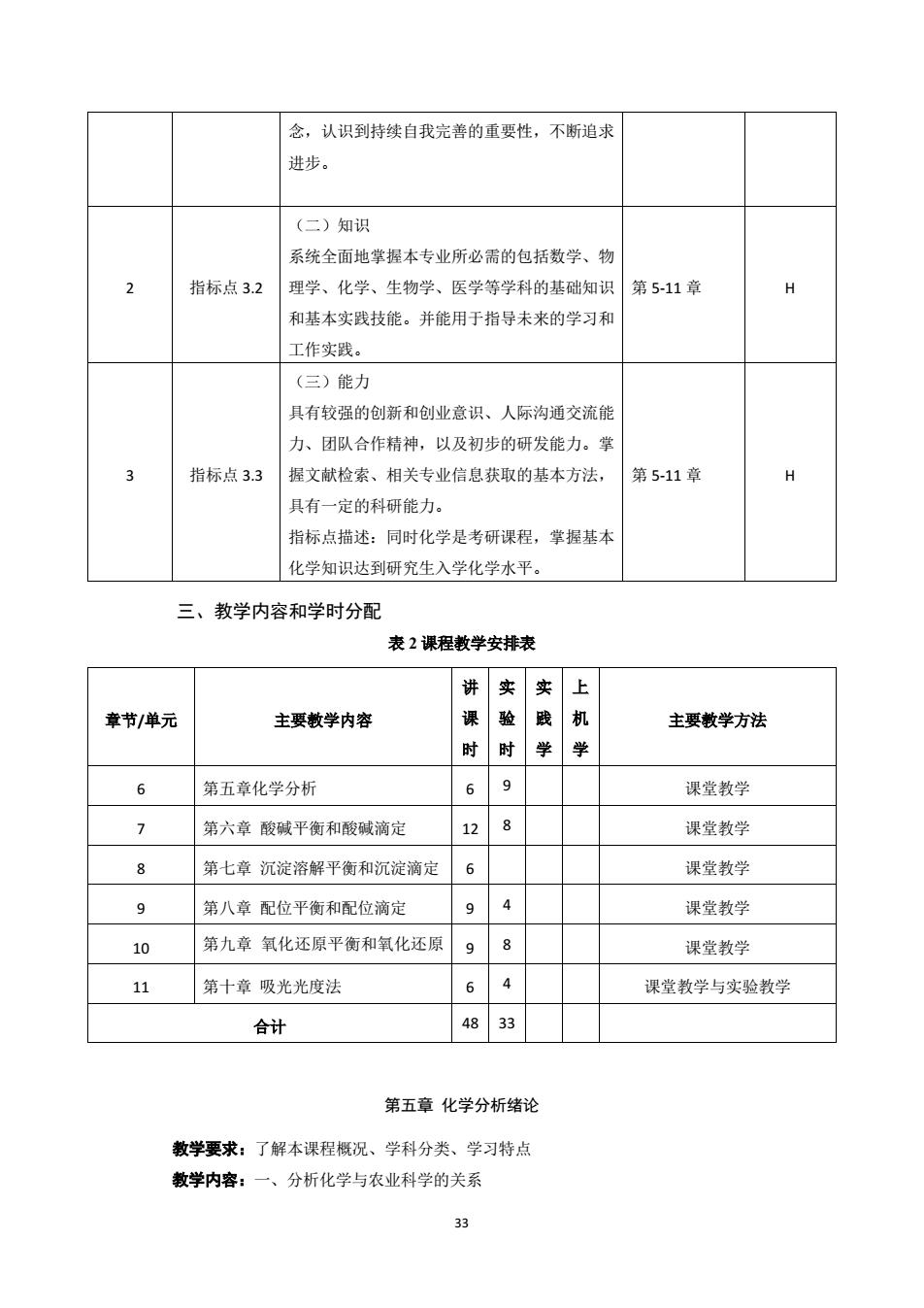
33 念,认识到持续自我完善的重要性,不断追求 进步。 2 指标点 3.2 (二)知识 系统全面地掌握本专业所必需的包括数学、物 理学、化学、生物学、医学等学科的基础知识 和基本实践技能。并能用于指导未来的学习和 工作实践。 第 5-11 章 H 3 指标点 3.3 (三)能力 具有较强的创新和创业意识、人际沟通交流能 力、团队合作精神,以及初步的研发能力。掌 握文献检索、相关专业信息获取的基本方法, 具有一定的科研能力。 指标点描述:同时化学是考研课程,掌握基本 化学知识达到研究生入学化学水平。 第 5-11 章 H 三、教学内容和学时分配 表 2 课程教学安排表 章节/单元 主要教学内容 讲 课 时 实 验 时 实 践 学 上 机 学 主要教学方法 6 第五章化学分析 6 9 课堂教学 7 第六章 酸碱平衡和酸碱滴定 12 8 课堂教学 8 第七章 沉淀溶解平衡和沉淀滴定 6 课堂教学 9 第八章 配位平衡和配位滴定 9 4 课堂教学 10 第九章 氧化还原平衡和氧化还原 9 8 课堂教学 11 第十章 吸光光度法 6 4 课堂教学与实验教学 合计 48 33 第五章 化学分析绪论 教学要求:了解本课程概况、学科分类、学习特点 教学内容:一、分析化学与农业科学的关系

二、分析化学的分类及普通化学课程的内容 三、有效数字及误差分析 重点难点:无 思政元素:科学思维、逻辑思维和辩证法,实际分问题解决问题的能力培养 第六章酸碱平衡和酸碱滴定 教学要求:酸碱平衡的理论知识及酸碱滴定的原理、计算和应用。 教学内容: 第一节酸碱质子理论 一、酸碱理论荷介 二、酸碱质子理论 第二节酸碱平衡的移动 一、水的离子积常数和溶液的H 二、弱酸弱碱的电离平衡 三、离子酸(碱)的电离平衡 第三节缓冲溶液 一、缓冲机制 二、缓冲体系的州 三、缓冲容量 四、缓冲溶液的配制 五、缓冲机制在生物学方面的意义 第四节酸碱指示剂 一、酸碱指示剂的作用原理 二、酸碱指示剂的变色范围 三、影响指示剂变色范围的因素 四、混合指示剂 第五节酸碱滴定法基本原理 一、强碱滴定强酸或强酸滴定强碱 二、强碱滴定弱酸 三、强酸滴定弱碱 四、多元酸(强)碱的滴定
34 二、分析化学的分类及普通化学课程的内容 三、有效数字及误差分析 重点难点:无 思政元素:科学思维、逻辑思维和辩证法,实际分问题解决问题的能力培养 第六章 酸碱平衡和酸碱滴定 教学要求:酸碱平衡的理论知识及酸碱滴定的原理、计算和应用。 教学内容: 第一节 酸碱质子理论 一、酸碱理论简介 二、酸碱质子理论 第二节 酸碱平衡的移动 一、水的离子积常数和溶液的 pH 二、弱酸弱碱的电离平衡 三、离子酸(碱)的电离平衡 第三节 缓冲溶液 一、缓冲机制 二、缓冲体系的 pH 三、缓冲容量 四、缓冲溶液的配制 五、缓冲机制在生物学方面的意义 第四节 酸碱指示剂 一、酸碱指示剂的作用原理 二、酸碱指示剂的变色范围 三、影响指示剂变色范围的因素 四、混合指示剂 第五节 酸碱滴定法基本原理 一、强碱滴定强酸或强酸滴定强碱 二、强碱滴定弱酸 三、强酸滴定弱碱 四、多元酸(强)碱的滴定

五、酸碱滴定中C0:的影响 第六节酸碱滴定法的应用 一、酸碱标准溶液的配制和标定 二、应用实例:铵盐中含氨量的测定及混合碱的分析 重点难点:缓冲溶液的配制、指示剂、滴定曲线的绘制、解读、酸碱滴定条件的判断和 实际应用。难点:多元酸的滴定。 思政元素:缓冲溶液的实际意义、酸碱滴定的应用,标准溶液,基准试剂,指示剂选择 的边界,K氏定氮法的漏洞与食品安全。 第七章沉淀平衡与沉淀滴定 教学要求:初步掌握沉淀平衡原理、基本概念及计算,沉淀滴定之银量法原理。 教学内容: 第一节溶度积 一、溶度积常数 二、溶度积和溶解度的关系 三、溶度积规则 第二节沉淀溶解平衡的移动 一、沉淀的生成 二、分步沉淀 三、沉淀的溶解和转化 第三节沉淀滴定法 一、莫尔法 二、佛尔哈德法 三、银量法的应用 重点难点:掌握溶解度和溶度积的概念及计算:掌握溶度积规则,掌握沉淀生成、溶解 及转化的规律,熟练进行有关计算,莫尔法的原理、酸度条件的选择:佛尔哈德法的原理及 佛尔哈德法返滴定测量C1的注意事项 难点:溶度积常数的灵活运用,两种银量法的酸度条件选择的原因,银量法的滴定曲线 指示剂指示滴定终点的变色原理和误差 思政元素:单方向写方程式的思维方式,分步计算的逻辑,佛尔哈德法返滴定的方法 意义
35 五、酸碱滴定中 CO2的影响 第六节 酸碱滴定法的应用 一、酸碱标准溶液的配制和标定 二、应用实例:铵盐中含氮量的测定及混合碱的分析 重点难点:缓冲溶液的配制、指示剂、滴定曲线的绘制、解读、酸碱滴定条件的判断和 实际应用。难点: 多元酸的滴定。 思政元素:缓冲溶液的实际意义、酸碱滴定的应用,标准溶液,基准试剂,指示剂选择 的边界,K 氏定氮法的漏洞与食品安全。 第七章 沉淀平衡与沉淀滴定 教学要求:初步掌握沉淀平衡原理、基本概念及计算,沉淀滴定之银量法原理。 教学内容: 第一节 溶度积 一、溶度积常数 二、溶度积和溶解度的关系 三、溶度积规则 第二节 沉淀溶解平衡的移动 一、沉淀的生成 二、分步沉淀 三、沉淀的溶解和转化 第三节 沉淀滴定法 一、莫尔法 二、佛尔哈德法 三、银量法的应用 重点难点:掌握溶解度和溶度积的概念及计算;掌握溶度积规则,掌握沉淀生成、溶解 及转化的规律,熟练进行有关计算,莫尔法的原理、酸度条件的选择;佛尔哈德法的原理及 佛尔哈德法返滴定测量 Cl- 的注意事项 难点:溶度积常数的灵活运用,两种银量法的酸度条件选择的原因,银量法的滴定曲线, 指示剂指示滴定终点的变色原理和误差 思政元素:单方向写方程式的思维方式,分步计算的逻辑,佛尔哈德法返滴定的方法 意义

第八章配位平衡和配位滴定 教学要求:初步掌握配位平衡概念、计算:配位滴定的原理、基本概念及计算 教学内容: 第一节配合物的基本概念 一、配位化合物的组成 二、配合物的命名 三、整合物 第二节配位化合物的价键理论 第三节配位平衡 、配位平衡常数 二、配位平衡的移动 第四节配位滴定法 一、EDTA配位剂 二、EDTA在溶液中各存在型体的分布 三、EDTA与金属离子形成整合物的特点 四、影响配位滴定的主要因素 五、滴定曲线 六、准确滴定金属离子的条件 第五节金属指示剂 一、金属指示剂作用原理 二、金属指示剂的选用原则 三、金属指示剂的封闭、僵化和氧化变质现象 四、常用金属指示剂 第六节提高配位滴定选择性的方法 一、控制溶液的酸度 二、利用掩蔽和解蔽作用 三、使用其他配位剂 第七节配位滴定法的应用 EDTA标准溶液的配制和标定
36 第八章 配位平衡和配位滴定 教学要求:初步掌握配位平衡概念、计算;配位滴定的原理、基本概念及计算 教学内容: 第一节 配合物的基本概念 一、配位化合物的组成 二、配合物的命名 三、螯合物 第二节 配位化合物的价键理论 第三节 配位平衡 一、配位平衡常数 二、配位平衡的移动 第四节 配位滴定法 一、EDTA 配位剂 二、EDTA 在溶液中各存在型体的分布 三、EDTA 与金属离子形成螯合物的特点 四、影响配位滴定的主要因素 五、滴定曲线 六、准确滴定金属离子的条件 第五节 金属指示剂 一、金属指示剂作用原理 二、金属指示剂的选用原则 三、金属指示剂的封闭、僵化和氧化变质现象 四、常用金属指示剂 第六节 提高配位滴定选择性的方法 一、控制溶液的酸度 二、利用掩蔽和解蔽作用 三、使用其他配位剂 第七节 配位滴定法的应用 一、EDTA 标准溶液的配制和标定

二、水中钙镁含量的测定 重点难点:掌握配合物的价健理论,并能联系dsp、sp入、d'sp、spd杂化轨道类型对 一些典型配离子(或配合物)的空间构型作一些简单的说明:熟练掌握配位平衡的原理、有 关计算、配位平衡的移动以及与其他平衡的关系。掌握酸效应系数、能进行配位滴定的有关 计算:掌握配位滴定法的基本原理,掌握影响配位滴定的因素,掌握提高配位滴定选择性的 方法 难点:配合物的价键理论:配位平衡的原理、有关计算、配位平衡的移动以及与其他平 衡的关系。酸效应系数、配位滴定的有关计算:影响配位滴定的因素,提高配位滴定选择性 的方法 思政元素:配合物的价键理论,配位滴定条件的迹择、水样采集与分析的意义,掩蔽剂 的原理,返滴定的逻辑。 第九章 氧化还原反应及氧化还原滴定 教学要求:掌握氧化还原平衡原理、概念、计算:氧化还原滴定的原理、基本概念及计 教学内容: 第一节氧化还原反应的基本概念 一、氧化数 二、氧化还原 三、自身氧化还原反应和歧化反应 第二节氧化还原反应方程式的配平 一、氧化数法 二、离子一电子法 第三节电极电势 一、原电池 二、电极电势 第四节电池电动势与影响电极电势的因素 一、电池电动势和吉布斯自由能变 二、电池电动势和化学反应的平衡常数 三、奈斯特方程式 四、奈斯特方程式的应用
37 二、水中钙镁含量的测定 重点难点:掌握配合物的价键理论,并能联系 dsp2 、sp3 、d 2 sp3 、sp3 d 2 杂化轨道类型对 一些典型配离子(或配合物)的空间构型作一些简单的说明;熟练掌握配位平衡的原理、有 关计算、配位平衡的移动以及与其他平衡的关系。掌握酸效应系数、能进行配位滴定的有关 计算;掌握配位滴定法的基本原理,掌握影响配位滴定的因素,掌握提高配位滴定选择性的 方法 难点:配合物的价键理论;配位平衡的原理、有关计算、配位平衡的移动以及与其他平 衡的关系。酸效应系数、配位滴定的有关计算;影响配位滴定的因素,提高配位滴定选择性 的方法 思政元素:配合物的价键理论,配位滴定条件的选择、水样采集与分析的意义,掩蔽剂 的原理,返滴定的逻辑。 第九章 氧化还原反应及氧化还原滴定 教学要求:掌握氧化还原平衡原理、概念、计算;氧化还原滴定的原理、基本概念及计 算 教学内容: 第一节 氧化还原反应的基本概念 一、氧化数 二、氧化还原 三、自身氧化还原反应和歧化反应 第二节 氧化还原反应方程式的配平 一、氧化数法 二、离子-电子法 第三节 电极电势 一、原电池 二、电极电势 第四节 电池电动势与影响电极电势的因素 一、电池电动势和吉布斯自由能变 二、电池电动势和化学反应的平衡常数 三、奈斯特方程式 四、奈斯特方程式的应用